Терапия №1 / 2022
Биомаркеры в кардиологии: микроРНК и сердечная недостаточность
1) ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва;
2) ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет);
3) ГБУЗ «Московский клинический научно-практический центр им. А.С. Логинова» Департамента здравоохранения города Москвы;
4) ФГБОУ ВО «Кабардино-Балкарский государственный университет им. Х.М. Бербекова» Министерства науки и высшего образования России, г. Нальчик
Аннотация. МикроРНК (miRNA) представляют собой небольшие некодирующие молекулы рибонуклеиновой кислоты. Они регулируют экспрессию генов на посттранскрипционном уровне с помощью связывания с 3’-нетранслируемыми участками miRNA-мишени. MiRNA были идентифицированы как ключевые регуляторы сложных биологических процессов, связанные с множественными сердечно-сосудистыми патологиями. MiRNA в кровотоке были исследованы в качестве новых биологических маркеров, особенно в контексте острого инфаркта миокарда и СН. Цель предлагаемого обзора – представить подробные данные о роли miRNA как биомаркера СН.
ВВЕДЕНИЕ
МикроРНК (miRNA) – это эндогенные, консервативные, одноцепочечные, небольшие (≈22 нуклеотида) некодирующие РНК [1]. Они играют роль в регуляции различных биологических процессов, включая эмбриогенез, пролиферацию и дифференциацию клеток, апоптоз и туморогенез [1, 2].
Первая miRNA, lin-4, была идентифицирована у свободно живущей нематоды (круглого червя) Caenorhabditis elegans в 1993 г. [3]. Lin-4 регулирует развитие C. elegans путем связывания с miRNA lin-14 и подавления экспрессии белка lin-14 [3]. Первая miRNA у человека (let-7) была обнаружена в 2000 г. [2]. В 2007 г. miRNA были впервые идентифицированы в периферической крови [4].
MiRNA регулируют экспрессию генов на посттранскрипционном уровне через связывание с 3’-нетранслируемыми участками miRNA-мишени [1]. Транскрипция miRNA начинается с формирования длинной молекулы первичной miRNA (pri-miRNA), из которой в дальнейшем при участии фермента Дроша в ядре образуется шпилечная структура – предшественник miRNA (pre-miRNA) [5]. После транспортировки в цитозоль pre-miRNA разрезается ферментом Дайсер-1, в результате чего образуются одноцепочечные зрелые miRNA. MiRNA ингибируют трансляцию и/или вызывают деградацию своей целевой miRNA в зависимости от степени комплементарности, а также количества и доступности связывающих участков [5]. Чем больше комплементарность между miRNA и его мишенью/мишенями, тем более вероятно, что miRNA приведет к их деградации (рис. 1) [1, 5].
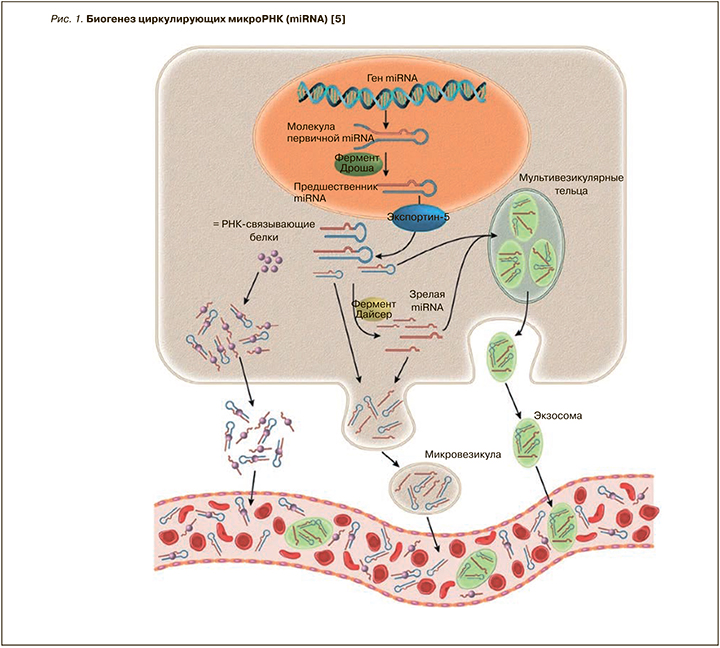
Доказано, что геном человека кодирует около 1000 miRNA. Из них более 100 были обнаружены в сыворотке крови здоровых людей [6]. Большая часть miRNA локализована внутри клетки; при этом незначительная доля miRNA найдена и во внеклеточном пространстве – слезной и семенной жидкостях, слюне, моче, спинномозговой жидкости и в грудном молоке [7].
MiRNA регулирует экспрессию около 30% генов, кодирующих структуру белка в организме человека. К настоящему времени мишени большинства miRNA неизвестны; возможно, это достаточно широкий диапазон – от одного до нескольких сотен генов [8]. В отличие от внутриклеточных miRNA, циркулирующие miRNA демонстрируют стабильность и устойчивость к деградации эндогенной RNA [1]. Циркулирующие miRNA защищены от RNAазы и других форм ферментов деградации за счет локализации в мембранных везикулах (экзосомах, микровезикулах). Также вне клетки miRNA связанны с транспортными белками (белками семейства Argonaute) и могут находиться внутри макромолекулярных комплексов, например в липопротеидах высокой плотности [1, 9, 10].
Экспрессия miRNA может наблюдаться как в образцах тканей, так и в бесклеточных биологических жидкостях, таких как сыворотка или плазма крови. Современные методологии, используемые для обнаружения miRNA, включают количественную полимеразную цепную реакцию (ПЦР, qPCR), гибридизацию in situ, микрочипы и секвенирование RNA [10, 11].
МикроРНК (miRNA) И СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ: ДАННЫЕ ИССЛЕДОВАНИЙ
Идеальный биологический маркер должен соответствовать следующим критериям: 1) доступность в качестве неинвазивного метода; 2) устойчивость к воздействиям извне (например, к ферментному расщеплению, замораживанию и разморозке, колебаниям водородного показателя среды); 3) высокая степень чувствительности и специфичности; 4) ранняя идентификация; 5) длительный период полураспада; 6) сопоставимость профилей в норме у женщин и мужчин, а также у людей разных возрастных категорий. MiRNA чрезвычайно стабильны в кровотоке и могут быть легко обнаружены с высокой чувствительностью и специфичностью при амплификации гена ERBB2 (HER2/neu) методом флуоресцентной гибридизации [5, 12].
В последние годы циркулирующие miRNA были исследованы как перспективные биомаркеры при сердечно-сосудистых заболеваниях (ССЗ) [5, 12].
В сердечной ткани эмбрионального и взрослого организма человека на всех этапах развития были идентифицированы miRNA (miR-21, miR- 29a, miR-129, miR-210, miR-211, miR-320, miR-423 и let-7c) [13]. Критическая роль miRNA во время эмбрионального и постнатального развития сердца была установлена в экспериментальных исследованиях, в которых удаляли фермент Дайсер. Это неспецифическое нарушение многих miRNA приводило к отеку перикарда, нарушению развития миокарда желудочков и ранней смерти мышей [14]. У здорового взрослого человека был выявлен ряд miRNA, которые экспрессируются в сердечной ткани и, таким образом, могут играть ключевую роль в функционировании сердца как в норме, так и при патологии. К ним относятся miR-1, miR-16, miR-27b, miR-30d, miR-126, miR-133, miR-143, miR-208 и семейство let-7 [13, 15].
Исследования, изучающие роль циркулирующих miRNA при сердечной недостаточности (СН), идентифицировали miRNA с измененными уровнями экспрессии у пациентов с этой патологией: miR-122, miR- 210, miR-423-5p, miR-499 и miR-622 [15].
В 2015 г. турецкими врачами (Cakmak Н.А. et al.) проведено исследование, в рамках которого было обследовано 20 пациентов с хронической сердечной недостаточностью (ХСН) I и II функционального класс...












