Фарматека №7 (220) / 2011
Клинический опыт использования бевацизумаба (Авастин) у больных метастатическим раком молочной железы с неустановленным HER2/neu и ER/PR-рецепторным статусом
ФГУ “Институт хирургии им. А.В. Вишневского”, Москва. 2ГУЗ МООД МЗ МО, Московская область. ФГУ “3-й ЦВКГ им. А.А. Вишневского” Минобороны России, Московская область.
В крупных рандомизированных исследованиях III фазы Е2100, AVADO и RIBBON-1 продемонстрирована высокая эффективность бевацизумаба (Авастин) в 1-й линии терапии распространенного рака молочной железы (РМЖ). Показана и его клиническая эффективность при добавлении к 2-й линии стандартной химиотерапии метастатического РМЖ в исследовании RIBBON-2. Данные об использовании препарата в повседневной клинической практике у больных с неустановленным HER2/new и ER/PR-рецепторным статусом ограничены, хотя эти пациенты могут рассматриваться в качестве кандидатов для проведения 1-й и 2-й линий химиотерапии в комбинации с бевацизумабом, поскольку назначение последнего не требует определения уровня VEGF (сосудистый эндотелиальный фактор роста) и рецепторов к VGRF. В статье приведен опыт успешного клинического применения бевацизумаба как в комбинации с таксанами, так и с режимами, не содержащими таксанов, у больных метастатическим РМЖ с неустановленным (по тем или иным причинам) HER2/new и ER/PR-рецепторным статусом.
Согласно опубликованным доклиническим данным, комбинация бевацизумаба (Авастин) с цитостатиками обладает синергизмом. Увеличение эффективности терапии при включении бевацизумаба в стандартные режимы 1-й и 2-й линий химиотерапии при HER2-негативном метастатическом раке молочной железы (мРМЖ) продемонстрировано в нескольких рандомизированных исследованиях III фазы: E2100, AVADO (бевацизумаб в комбинации с таксанами в качестве 1-й линии терапии) [1, 2], RIBBON-1 (бевацизумаб в комбинации с таксанами или капецитабином, или антрациклинами в качестве 1-й линии терапии) [3], RIBBON-2 (бевацизумаб + стандартная химиотерапия в качестве 2-й линии) [4].
При мета-анализе [5] результатов указанных исследований показано 36 %-ное снижение риска рецидива и смерти, увеличение времени без прогрессирования заболевания и частоты общего ответа во всех подгруппах больных с HER2-негативным мРМЖ, в 1-й линии терапии получавших цитостатики в комбинации с бевацизумабом, в отсутствие различий в общей выживаемости. Профиль безопасности бевацизумаба при этом соответствовал ранее полученным данным.
К сожалению, в повседневной клинической практике до настоящего времени существует группа больных мРМЖ с неустановленным (по тем или иным причинам) HER2/neu и ER/PR-рецепторным статусом. Эти пациентки не могут рассматриваться в качестве кандидаток для терапии трастузумабом (Герцептин), однако использование бевацизумаба у них вполне оправданно, поскольку не требует определения уровня VEGF в сыворотке крови и рецепторов к нему. При этом эффективность комбинации бевацизумаба с цитостатиками была четко показана в перечисленных выше исследованиях.
Приводим наш опыт использования бевацизумаба в 1-й и 2-й линиях химиотерапии у больных мРМЖ с неустановленным HER2/neu и ER/ PR-рецепторным статусом.
Клиническое наблюдение № 1
Больная 1947 г. р., менопауза, состояние по шкале ECOG-1.
В 2000 г. установлен диагноз: рак левой молочной железы (МЖ), стадия рT2N0M0 (IIа). Проведена резекция левой МЖ (11.07.2000) с последующей лучевой терапией (46 Гр). Гистологическое заключение: инвазивный рак без метастазов в лимфатические узлы. Определение статуса ER/PR/HER2 не выполнено.
Прогрессирование заболевания в декабре 2008 г. (длительность безрецидивного периода – 8 лет 5 месяцев).
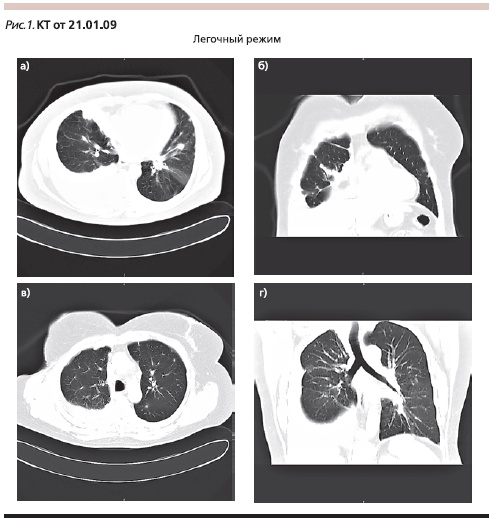
При осмотре жалобы на одышку, кашель; обнаружены правосторонний плеврит, дыхательная недостаточность II степени. По данным компьютерной томографии (КТ; 21.01.2009; рис. 1): правосторонний плеврит (1,5 л), в обоих легких множественные метастазы от 5 до 20 мм в диаметре, увеличение всех групп медиастинальных лимфатических узлов.
Из плевральной полости эвакуировано 1,5 л жидкости. Цитологическое заключение: железистый рак.
В 1-й линии терапии назначены паклитаксел 90 мг/м2 внутривенно в дни 1, 8, 15 + бевацизумаб 10 мг/кг внутривенно в дни 1 и 15. После двух циклов терапии, по данным КТ (25.03.2009; рис. 2), отмечено уменьшение числа (до 4–6) и размеров (до 5–7 мм) выявленных ранее очагов; медиастинальные лимфатические узлы не увеличены; незначительное количе...