Эпидемиология и Инфекционные болезни. Актуальные вопросы №4 / 2020
Молекулярно-генетические механизмы лекарственной резистентности Plasmodium falciparum
1) ФГБВОУ «Военно-медицинская академия им. С.М. Кирова» Министерства обороны Российской Федерации, Санкт-Петербург, Россия;
2) ФГБУ «Детский научно-клинический центр инфекционных болезней Федерального медико-биологического агентства», Санкт-Петербург, Россия;
3) ГБУЗ «Клиническая инфекционная больница им. С. П. Боткина», Санкт-Петербург, Россия
Цель исследования. Изучение особенностей метаболизма P. falciparum, фармакологического действия противомалярийных препаратов и молекулярно-генетических механизмов формирования лекарственной резистентности возбудителей малярии, вызванной P. falciparum.
Материалы и методы. Проведен анализ данных о современных противомалярийных лекарственных средствах, геноме малярийных плазмодиев и механизмах формирования лекарственной резистентности P. falciparum.
Результаты. Показано, что противомалярийные препараты могут блокировать или конкурентно замещать транспортные белки, а также ключевые паразитарные ферменты, катализирующие основные метаболические пути пластического и энергетического обмена. Мишенями могут служить метаболиты поглощаемого плазмодиями гемоглобина, ферменты электронно-транспортной цепи, а также такие паразитарные ферменты, как цитохром b, дигидроптероатсинтаза, дигидрофолатредуктаза, кальций-зависимая АТФ-синтаза, фосфатидилинозитол-3-киназа, дигидрооротатдегидрогеназа и другие. Основные механизмы лекарственной устойчивости связаны с генетической гетерогенностью возбудителей инфекции. В формировании устойчивости важное значение имеют SNP мутации по локусам генов PfCRT, PfMDR1, PfATP6, PfDHPS, PfDHFR, PfCYTB, а также рекомбинация генетического материала плазмодиев в ходе эритроцитарной шизогонии. Формированию резистентных штаммов и отбору мутаций лекарственной устойчивости способствует длительное персистирование паразитов в крови на фоне приема противомалярийных препаратов.
Заключение. Основными принципами этиотропного лечения малярии должны служить раннее начало лечения, а также комбинированная терапия с использованием наиболее эффективных противомалярийных препаратов разных фармакологических групп в дозировках, обеспечивающих быструю элиминацию возбудителей из организма больного.
Малярия – одна из наиболее широко распространенных и опасных инфекций [1, 2]. По данным ВОЗ, малярией ежегодно болеют около 660 000 человек, около 330 000 погибают [3, 4]. Более 99% случаев смерти от малярии приходится на долю тропической формы заболевания, вызываемой Plasmodium falciparum (P. falciparum). Эта инфекция представляет серьезную проблему для жителей развитых стран, по служебной или личной необходимости выезжающих в эндемичные регионы [5]. В РФ ежегодно регистрируются случаи гибели лиц, заразившихся малярией, вызванной P. falciparum, при посещении стран Африки, Юго-Восточной Азии, Южной Америки, островов Океании [3, 5]. Причинами этого служит высокая вирулентность P. falciparum, а также интенсивное формирование у паразитов устойчивости к действию противомалярийных препаратов [3, 6]. Если осложненное течение малярии, вызванной высоковирулентными возбудителями, может быть предупреждено своевременной диагностикой и ранним началом этиотропной терапии, то лекарственная резистентность плазмодиев до настоящего времени остается нерешенной проблемой для практической медицины [3, 5, 7]. Ситуация осложняется ограниченным перечнем противомалярийных препаратов, прошедших государственную регистрацию в РФ. Нередко больным малярией, вызванной P. falciparum, вынужденно назначают лишь 1 этиотропный препарат, недостаточно эффективный в отношении лекарственноустойчивых паразитов, в то время как отход от практики монотерапии низкоэффективными средствами стал общемировой нормой лечения малярии [6–9].
Цель работы – изучение и обобщение данных об особенностях метаболизма P. falciparum, фармакологическом действии противомалярийных препаратов и молекулярно-генетических механизмах формирования лекарственной резистентности возбудителей малярии, вызванной P. falciparum, и определение современных тенденций научных исследований в этой области.
Такое положение во многом объясняется недостатком у врачей и организаторов системы здравоохранения знаний в области фармакологии малярии и лекарственной резистентности возбудителей. В этой ситуации становится актуальным формирование у медицинских специалистов современных представлений о механизмах действия лекарственных препаратов, а также молекулярно-генетических механизмах, лежащих в основе формирования лекарственной резистентности малярийных плазмодиев.
Были использованы материалы базы данных PlasmoDB (Plasmodium Data Base), содержащей сведения о геноме малярийных плазмодиев.
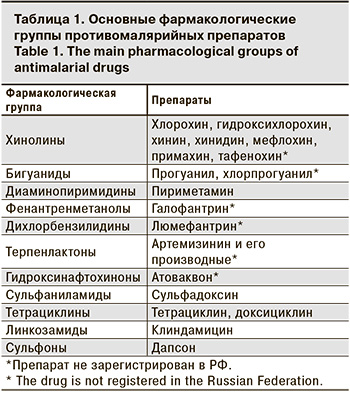
Арсенал этиотропных средств для лечения малярийной инфекции насчитывает более 20 препаратов, которые относятся к разным фармакологическим группам, отличающимся избирательностью воздействия на основные метаболические пути паразитарной клетки (табл. 1).
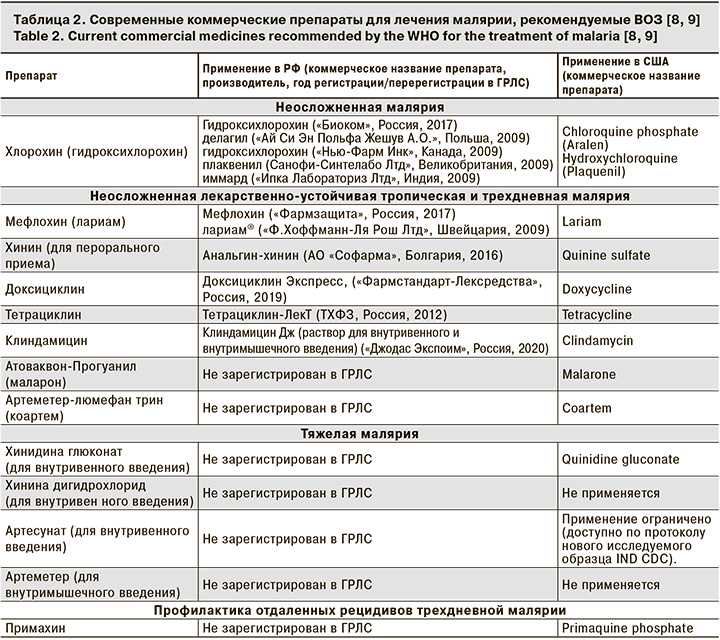
В настоящее время перечень препаратов, рекомендованных ВОЗ, ограничен и включает высокоэффективные, а также хорошо переносимые лекарственные средства с различным механизмом лекарственного воздействия на возбудителей (табл. 2).
Противомалярийные препараты могут блокировать или конкурентно замещать транспортные белки, а также ключевые паразитарные ферменты, катализирующие основные метаболические пути пластического и энергетического обмена [2, 10] (табл. 3).
Действие противомалярийных препаратов в основном направлено на эритроцитарные стадии развития паразитов. Интенсивное циклическое размножение плазмодиев предполагает высокую активность метаболических процессов, разобщение которых приводит к гибели паразитов [2]. Интенсивные обменные процессы обеспечиваются за счет поглощения паразитом гемоглобина из цитоплазмы пораженного эритроцита [8]. В пищеваритальной вакуоли плазмодия кровяной пигмент подвергается деградации. Питательным субстратом служит его белковая фракция. Железосодержащие компоненты пигмента (гематин, порфирин) токсичны для паразитов и метаболизируются их ферментными системами в нетоксичный гемозин, который откладывается в виде зернистости Маурэра и Шюфнера [11]. Разобщение этого метаболического пути с помощью химиопрепаратов приводит к накоплению токсичных продуктов и гибели плазмодиев. Трофозоит развивается внутри эритроцита, защищенный от цитоплазмы клетки хозяина мембраной паразитофорной вакуоли. В ее формировании участвует апикопласт паразита (видоизмененный аналог пластид), в строме которого происходит метаболизм жирных кислот ...












