Фарматека №7 / 2020
Перспективы применения иммунотерапии при лечении плоскоклеточного рака головы и шеи
1) Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова, Санкт-Петербург, Россия;
2) Северо-Западный государственный медицинский университет им. И.И. Мечникова, Санкт-Петербург, Россия;
3) Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова, Санкт-Петербург, Россия
Плоскоклеточный рак органов головы и шеи (ПРГШ) занимает шестое место в структуре заболеваемости и восьмое место в структуре смертности больных злокачественными новообразованиями во всем мире. Потенциально новым терапевтическим подходом к лечению рецидивирующим и/или метастатическим ПРГШ является иммунотерапия, нацеленная на иммунные контрольные точки, такие как рецептор программируемой смерти 1-го типа (PD-1). В обзоре представлены результаты исследований эффективности и безопасности препаратов для иммунотерапии рецидивирующего и/или метастатического ПРГШ (пембролизумаб, ниволумаб и др.). Обсуждаются перспективы неоадъювантной иммунотерапии распространенного ПРГШ. Последние исследования иммунотерапии ингибиторами точек иммунного контроля подтверждают целесообразность применения данного подхода, основанного на значимо более высоких показателях контроля над опухолью и продолжительности жизни по сравнению со стандартными методами лечения пациентов с ПРГШ.
Введение
Плоскоклеточный рак органов головы и шеи (ПРГШ) занимает шестое место в структуре заболеваемости и восьмое место в структуре смертности больных злокачественными новообразованиями во всем мире. Ежегодно в мире 550 тыс. случаев первичных опухолей приходится на опухоли головы и шеи (ОГШ), также зарегистрировано 380 тыс. случаев смерти от рака данной локализации [1]. В России за 2018 г. впервые выявлено около 23 тыс. случаев ОГШ [2].
Злокачественные ОГШ по гистологическому варианту представлены в основном плоскоклеточным раком (95%), чаще всего возникают они в полости рта и глотке. Злоупотребление алкоголем, курение табака и инфицирование вирусом папилломы человека (ВПЧ) – основные факторы риска развития ПРГШ [3–5]. Нарушение в работе иммунной системы является одним из важнейших факторов развития и увеличения частоты заболеваемости ОГШ [6].
Цель лечения больных рецидивирующим и/или метастатическим (р/м) ПРГШ в основном направлена на поддержание качества жизни. Медиана общей выживаемости (ОВ) больных р/мПРГШ обычно не превышает одного года [7, 8]. Возможность хирургического лечения и повторной лучевой терапии рассматривается лишь у ограниченного числа больных рецидивирующим местнораспространенным ПРГШ. Платиносодержащая полихимиотерапия, таргетная терапия цетуксимабом в настоящий момент являются стандартом первой линии лекарственной терапии р/мПРГШ [9].
Потенциально новым терапевтическим подходом к лечению ПРГШ является иммунотерапия, нацеленная на иммунные контрольные точки, такие как рецептор программируемой смерти 1-го типа (Programmed cell death, PD-1) [10]. В нормальных условиях иммунная система использует пути ингибирования контрольных точек PD-1, чтобы регулировать целевую активацию T-лимфоцитов и иммунный ответ против патогенов, одновременно предотвращая развитие аутоиммунных реакций. Опухолевые клетки (ОК) используют эти пути для создания иммуносупрессивной микросреды, в которой они могут «скрываться» от иммунной системы [11]. Для ухода от надзора иммунной системы ОК используют механизмы, которые в норме контролируют выраженность и длительность иммунного ответа [12]. Блокирование иммуносупрессивного эффекта PD-1 и -L1 заново «обучает» иммунную систему организма бороться со злокачественной опухолью, лишая возможности ОК «ускользать» от иммунного надзора, что приводит к потенциальной гибели опухоли [13].
Пембролизумаб
Одним из перспективных препаратов в области иммунотерапии является пембролизумаб – человеческое моноклональное антитело, селективно блокирующее взаимодействие между PD-1 и его лигандами PD-L1 и -L2.
В 2016 г. T.Y. Seiwert et al. представили результаты Ib-фазы многокогортного многоцентрового открытого исследования KEYNOTE-012 по оценке безопасности и эффективности пембролизумаба, назначаемого в дозе 10 мг/кг каждые 2 недели больным р/мПРГШ [14]. Представлены данные о больных позитивным PD-L-статусом опухоли р/мПРГШ (n=60), из которых 23 (38%) были ВПЧ-позитивными и 37 (62%) ВПЧ-негативными. Необходимо отметить, что в данном исследовании экспрессию PD-L1 определяли как на опухолевых, так и на иммунных клетках (показатель CPS), что является важным именно при ОГШ, т.к. ранее было продемонстрировано, что экспрессия PD-L1 на иммунных клетках имеет большее прогностическое значение в отношении ОВ и выживаемости без прогрессирования (ВБП), чем на опухолевых. Объективный ответ (ОО) опухоли (по критериям RECIST 1.1 по оценке независимых экспертов; n=45) на лечение у всей популяции больных составил 18% (8 из 45 пациентов; 95% доверительный интервал [ДИ] – 8–32), 25% у пациентов с ВПЧ+ статусом (4 из 16; 95% ДИ – 7–52) и 14% с ВПЧ- статусом (4 из 29; 95% ДИ: 4–32) [14]. В расширенной когорте больных исследования KEYNOTE-012 132 пациента получали фиксированную дозу пембролизумаба 200 мг каждые 3 недели независимо от статуса CPS. Частота ОО составила 18% (95% ДИ: 12–26) по данным исследователей и 20% по оценке независимых экспертов (95% ДИ: 13–28). Медиана продолжительности ответа не была достигнута (диапазон ≥2–11 месяцев). Шестимесячные ВБП и ОВ составили 23 и 59% соответственно. У пациентов с положительным CPS-статусом наблюдалось статистически значимое увеличение частоты ОО (22 против 4%; p=0,021) [15] (см. таблицу). Также в одной из когорт исследования KEYNOTE-012 сообщается о результатах из Азиатско-Тихоокеанского региона. Частота ОО составила 19% (95% ДИ: 7–39). При медиане наблюдения 12 месяцев (диапазон от 2 до 21 месяца) медиана длительности ответа не достигнута (диапазон от 6 до 17+ месяцев) [16].
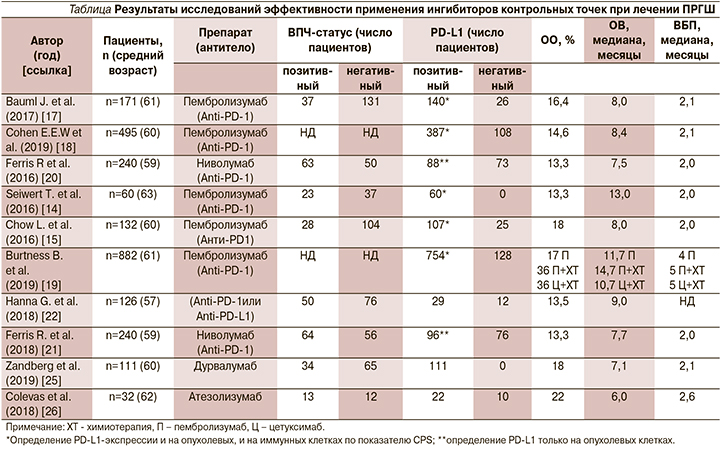
В 2017 г. представлены результаты многоцентрового исследования II фазы (KEYNOTE-055), проведенного J. Bauml et al., в которое включались пациенты с...












