Кардиология №2 / 2017
Предикторы перехода доклинической диастолической дисфункции левого желудочка в сердечную недостаточность с сохраненной фракцией выброса у пациентов с метаболическим синдромом
1НИИ кардиологии, Ереван, Армения; 2Ереванский государственный медицинский университет, Ереван, Армения
Исследованы эхокардиографические показатели 325 пациентов с доклинической диастолической дисфункцией (ДДД) и сердечной недостаточностью с сохраненной фракцией выброса (СНСФВ) левого желудочка (ЛЖ), а также 50 здоровых лиц с целью выявления различий по параметрам между пациентами обеих групп и определения независимых предикторов перехода ДДД в СНСФВ. ДДД и СНСФВ были диагностированы после нагрузочной пробы с определением показателей диастолы ЛЖ с помощью тканевой допплерографии и наличия симптомов СН. Исследование выявило, что индекс массы миокарда ЛЖ, систолическое артериальное давление, параметры продольной деформации ЛЖ и левого предсердия (ЛП) достоверно различаются в обеих группах по сравнению с контрольной, а также между группами. Пациенты с ДДД с последующим развитием СНСФВ имели высокие показатели жесткости ЛП и межпредсердной механической асинхронии. Кроме того, перечисленные показатели являлись независимыми предикторами перехода ДДД в СНСФВ. Результаты исследования могут способствовать раннему выявлению пациентов с ДДД и высоким риском развития СНСФВ.
Доклиническая диастолическая дисфункция (ДДД) левого желудочка (ЛЖ) является частой находкой у лиц пожилого возраста, а также пациентов с различными хроническими заболеваниями без симптомов сердечной недостаточности с сохраненной фракцией выброса (СНСФВ) ЛЖ [1]. Несмотря на свое большое клиническое значение, а именно возможность ее перехода в СНСФВ, резко ухудшающую прогноз, ДДД мало исследована. Предикторы ее перехода в СНСФВ неизвестны. ДДД охватывает большой контингент лиц с различными степенями диастолической дисфункции (ДД) в покое и/или при физической нагрузке с неизвестным течением и прогнозом [2]. ДДД может ухудшить качество жизни пациентов и быть связанной со структурными изменениями сердца, повышающими риск развития сердечно-сосудистых осложнений (ССО) [3]. Несмотря на кажущуюся простую логическую связь между ДДД и СНСФВ как стадиями одного и того процесса, взаимоотношения между этими патологиями являются сложными [4]. Хотя у многих лиц ДДД прогрессирует до СНСФВ, до сих пор неизвестно, является ли взаимосвязь линейной. У одних лиц с выраженной ДД ЛЖ отсутствуют симптомы СН, а у других с умеренной ДД ЛЖ имеется СНСФВ [4]. Не каждая ДДД прогрессирует, и пациенты с одинаковой степенью ДД ЛЖ могут иметь очень разные симптомы. Кроме того, диастолическая функция ЛЖ может различаться у одного и того же пациента в покое и при физической нагрузке [5], причем диастолические параметры при нагрузочных тестах теснее коррелируют с выраженностью ДД [6, 7], поэтому диастолический нагрузочный тест должен быть важным составляющим в диагностике ДДД. В исследованиях показано, что, несмотря на сохраненную фракцию выброса ЛЖ, другие показатели систолической функции, в частности продольная деформация миокарда, могут быть снижены [8]. В немногочисленных исследованиях использовались параметры тканевой допплерографии (ТДГ) предсердий для характеристики патофизиологических процессов при СНСФВ. Однако комплексного динамического исследования параметров ДДД и определения их как предикторов дальнейшей трансформации ДДД в СНСФВ по данным изучаемой нами литературы не проводилось. Настоящее исследование предпринято для выявления различий между систолическими и диастолическими показателями камер сердца у пациентов с ДДД и СНСФВ, а также попытки определения предикторов развития СНСФВ.
Материал и методы
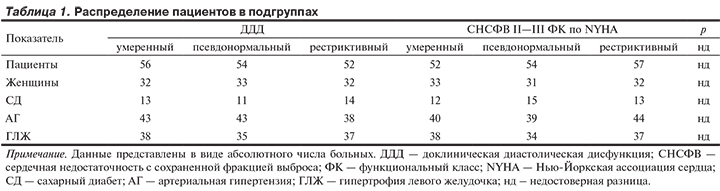
В исследование включены 325 пациентов (193 женщин) с метаболическим синдромом (МС) в возрасте 63±12 лет с ДДД и СФВ и СНСФВ ЛЖ II—III функционального класса (ФК) по классификации Нью-Йоркской ассоциации сердца (NYHA). МС был диагностирован в соответствии с критериями NCEP-ATP III 2001 г. при наличии по крайней мере трех показателей: низкого уровня холестерина липопротеинов высокой плотности (<40 мг>130/85 мм рт.ст. или наличия артериальной гипертензии (АГ), требующей лечения, увеличенной окружности талии (>102 см у мужчин и >88 см у женщин), высоких уровней триглицеридов (≥150 мг/дл) и глюкозы натощак (>100 мг/дл). Пациенты с высокими уровнями АД и глюкозы в крови натощак получали лечение по крайней мере в течение 1 года. Разделение пациентов на группы ДДД и СНСФВ проведено по данным эхокардиографии (ЭхоКГ) в покое и после диастолического нагрузочного эхокардиографического теста. Контрольную группу составили 50 здоровых лиц того же возраста без ДД ЛЖ. В пределах каждой группы пациенты были разделены на 3 подгруппы в зависимости от типа ДД ЛЖ по данным ЭхоКГ в покое: нарушение реласации ЛЖ (Е/А < 0,75, время замедления пика Е>250 мс), псевдонормальный тип (Е/А >1, время замедления пика Е ≤ 160 мс), рестриктивный тип (Е/А >2, время замедления пика Е <160 мс). Однако для выявления ДДД и СНСФВ мы применяли диастолический стресс-тест и не опирались на данные трансмитрального кровотока в покое — ненадежного признака диагностики ДДД или СНСФВ. Число пациентов с АГ или сахарным диабетом (СД), а также количество мужчин и женщин достоверно не различались в группах и подгруппах, как и наличие гипертрофии ЛЖ (табл. 1). Пациенты не имели дисфункции клапанного аппарата или нарушения функции почек.
Критериями исключения являлись «легочное сердце», значительные клапанные поражения, нестабильная стенокардия, болезни печени и почек, констриктивный перикардит, рестриктивная или гипертрофическая кардиомиопатия.
ЭхоКГ проводили по рекомендациям Американского общества эхокардиографии [9] на аппарате Vingmed Vivid 7 Dimension с датчиками M4S и 3V с частотой кадров минимум 50 в секунду. При получении апикальных срезов обращали внимание на полную визуализацию верхушки и предсердий без их укорочения. Все изображения получены и сохранены при задержке дыхания в конце выдоха. Видеоизображения и данные допплерографии из 5 циклов сохранены для последующего просмотра с использованием пакета программ EchoPack, GEHealthcare. ФВ ЛЖ измеряли в 3-мерном режиме с помощью программы TomTec. Максимальный объем левого предсердия (ОЛПмакс) в...40>












