Урология №3 / 2018
Прогностическое значение простатспецифического антигена при определении показаний к первичной биопсии предстательной железы
СПбГБУЗ «Клиническая больница Святителя Луки», Санкт-Петербург, Россия; ФГБУ ГНЦ ФМБЦ им. А. И. Бурназяна ФМБА России, Москва
В настоящее время биопсия предстательной железы остается основным методом дифференциальной диагностики доброкачественных и злокачественных заболеваний простаты. Показанием к процедуре является повышение в сыворотке крови уровня общего простатспецифического антигена (ПСА), однако низкая канцероспецифичность последнего может послужить причиной неоправданной биопсии с риском развития осложнений. Для повышения диагностических возможностей ПСА-тестирования разработаны методы определения дополнительных показателей – свободной фракции ПСА, -2проПСА, а также расчетных индексов плотности ПСА, PHI, f/t ПСА.
Цель исследования: изучить степень соответствия результатов определения показателей ПСА и выявляемости доброкачественных и злокачественных поражений предстательной железы при ее первичной биопсии.
Материалы и методы. В процессе работы был выполнен анализ 65 первичных биопсий, назначенных на основании повышенного сывороточного уровня ПСА по сравнению с результатами расширенного ПСА-тестирования с определением дополнительных параметров ПСА.
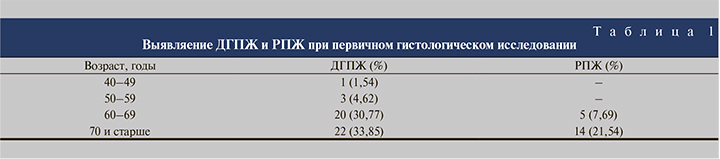
Результаты. Гистологические признаки рака предстательной железы (РПЖ) при первичном биопсическом исследовании, выполненном в связи с повышением сывороточного уровня общего ПСА, выявлены примерно в 30% случаев. Диагностирование гистологически подтвержденного РПЖ увеличивается с возрастом и у 70–79-летних мужчин превышает таковую для пациентов 60–69 лет. Плотность ПСА в 85% случаев РПЖ превышает значение данного показателя при доброкачественной гиперплазии предстательной железы (ДГПЖ). В условиях РПЖ у всех пациентов без исключения уровни PHI и f/t ПСА были больше 25 и меньше 0,15 соответственно. У большинства больных ДГПЖ значения PHI и f/t ПСА не превышали 25 и были больше 0,15.
Выводы. 1. При первичном гистологическом исследовании, выполненном в связи с повышением в сыворотке крови уровня общего ПСА, РПЖ выявляется примерно в 30% случаев. 2. Возраст мужчин от 60 лет и старше следует расценивать как фактор риска злокачественного перерождения ткани простаты. Вероятность малигнизации эпителиоцитов предстательной железы у мужчин старше 70 лет, чем у 60–69-летних. 3. Плотность ПСА при морфологически верифицированном РПЖ статистически значимо превышает таковую у мужчин с ДГПЖ и пороговое значение показателя в 85% случаев. 4. Определение PHI и f/t ПСА позволяет повышать точность прогнозирования злокачественного поражения простаты, корректировать показания к гистологическому исследованию, снижать частоту неоправданных биопсий. 5. Для уточнения показаний к первичной биопсии предстательной железы в случаях с варьированием концентрации ПСА в сыворотке крови от 2 до 10 нг/мл требуется определение дополнительных расчетных показателей – плотности ПСА, индекса здоровья простаты, отношения свободного и общего ПСА.
Введение. С болезнями предстательной железы (БПЖ) ассоциировано существенное ухудшение физического и психоэмоционального состояния заболевших мужчин, а также снижение качества их жизни. Согласно данным статистики, за период с 2003 по 2013 г. число мужчин, страдающих БПЖ, увеличилось на 72,4% (с 774 687 до 1 335 188 человек), а количество впервые выявленных случаев БПЖ – на 28,5% (с 214 815 до 276 039). В целом БПЖ составляют 15,3% от всех заболеваний мочеполовой системы [1].
Рак предстательной железы (РПЖ) – одно из наиболее часто регистрируемых злокачественных новообразований у мужчин среднего и пожилого возраста. Ежегодно во всех странах мира суммарное количество новых случаев РПЖ достигает 550–600 тыс. [2]. В России абсолютное количество случаев РПЖ, впервые выявленных в течение 2016 г., составило 34 955, суммарная численность пациентов, которые находились на учете по данному поводу в конце 2016 г., была равной 202 604, т.е. почти в 2 раза больше, нежели в 2010 г. [3].
При ДГПЖ наблюдается повышенная фокальная пролиферация стромальных и эпителиальных периуретральных клеток простаты, что приводит к увеличению объема органа, сдавлению простатического отдела уретры и неповрежденной ткани предстательной железы, появлению и постепенному нарастанию клинической симптоматики заболевания. Субъективные и объективные признаки ДГПЖ неспецифичны и связаны с инфравезикальной обструкцией. Реализация механического и динамического компонентов последней обусловливает нарушение мочеиспускания, ишемизацию и снижение силы сокращений гладкой мускулатуры стенки мочевого пузыря, застой мочи и ее инфицирование, формирование пузырно-мочеточникового рефлюкса. Таким образом, существенно повышается риск инфекционно-воспалительного поражения почечных структур, нарушений мочеобразования, острой задержки мочи [4].
Причиной инфравезикальной обструкции может быть не только доброкачественная пролиферация стромальных клеток простаты, но и ряд других форм патологии, приводящих к подпузырному уменьшению диаметра просвета уретры, например РПЖ, особенно на ранних стадиях его развития. Сходство симптоматики затрудняет дифференциальную диагностику в подобных случаях.
Наличие или отсутствие злокачественного перерождения паренхимы предстательной железы устанавливается в процессе гистологического исследования образцов паренхимы органа, полученных при биопсии. При обнаружении в биопсийном материале признаков РПЖ выполняются патоморфологическое стадирование опухоли, количественная оценка злокачественного поражения простаты, идентификация признаков периневральной инвазии малигнизированных клеток и инвазии семенных пузырьков [2]. Для патоморфологического стадирования РПЖ применяется шкала Глисона [5], детализированная и усовершенствованная на Конференции согласия ISUP (International Society of Urological Pathology) патологов и урологов США и Канады, которая состоялась в Сан-Антонио в 2005 г. В результате была создана модифицированная версия шкалы Глисона, используемая в настоящее время [6].
Для количественной оценки степени злокачественного поражения предстательной железы также необходим биопсийный материал, в котором учитывают общую численность позитивных проб, относительное количество малигнизированной ткани в отдельных столбиках биоптата и всем биопсийном материале в целом, максимальное процентное содержание злокачественно перерожденной паренхимы, абсолютную длину (мм) участка опухолевой ткани в каждом из столбиков.
Полученные данные коррелируют с объемом разрастания, степенью вероятности экстракорпоральной инвазии злокачественных клеток, положительного хирургического края при радикальном оперативном лечении РПЖ и биохимического рецидива после вмешательства [7].

В настоящее время результаты гистологического исследования полученного при биопсии материала предстательной железы остаются главным критерием дифференциальной диагностики доброкачественных и злокачественных поражений паренхимы простаты.
Первичная биопсия...












