Фарматека №17 (330) / 2016
Возможности новых антиангиогенных препаратов во второй линии лекарственной терапии немелкоклеточного рака легкого
ФГБУ «НИИ онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург
Ведущая роль ангиогенеза в процессах пролиферации и прогрессирования немелкоклеточного рака легкого (НМРЛ) обусловливает повышенный интерес к развитию лекарственных подходов, направленных на подавление этого важнейшего аспекта туморогенеза. Бевацизумаб, продемонстрировавший в комбинации с цитостатиками способность увеличивать выживаемость без прогрессирования и общую выживаемость больных НМРЛ, был первым ингибитором ангиогенеза, одобренным для клинического применения. В настоящее время продолжаются активный поиск и изучение новых лекарственных агентов, подавляющих ангиогенез посредством блокирования различных сигнальных путей. Одним из таких перспективных препаратов является нинтеданиб, представляющий собой мощный тройной ингибитор ангиокиназы, действие которого реализуется в результате блокады не только VEGFR, но и FGFR и PDGFR, участвующих в развитии резистентности опухоли к бевацизумабу. В настоящем обзоре обсуждаются перспективы подобного лекарственного воздействия и анализируются результаты основных клинических исследований III фазы в этой области.
Современные подходы к лекарственной терапии местнораспространенного и метастатического немелкоклеточного рака легкого
Рак легкого является наиболее часто диагностируемым злокачественным новообразованием в мире [1]. В 2012 г. этот диагноз был установлен 1,8 млн больных и составил 12,9% в структуре всех впервые выявленных злокачественных опухолей. Кроме того, рак легкого занимает лидирующую позицию среди причин онкологической смертности в мире, обусловливая пятилетнюю выживаемость, не превышающую 15% [2].
Немелкоклеточный рак легкого (НМРЛ) представляет собой наиболее частый его морфологический тип, частота которого достигает 85–90%. Благодаря достижениям молекулярной онкологии представление о НМРЛ в последние годы претерпело существенные изменения. В настоящее время НМРЛ рассматривается как совокупность различных опухолевых вариантов, идентифицируемых с помощью гистологического субтипирования или молекулярно-генетического анализа [3, 4]. Несмотря на многообразие НМРЛ, принципиальным этапом для выбора оптимальной лечебной тактики является определение его принадлежности к одному из двух патоморфологических типов – плоскоклеточному или неплоскоклеточному раку [5].
Большинство больных НМРЛ нуждаются в проведении лекарственной терапии как на этапе первичной диагностики местнораспространенной или метастатической формы заболевания, так и в случае прогрессирования опухолевого процесса после проведенного ранее радикального лечения [6].
Стандартом современной лекарственной терапии распространенного НМРЛ, не имеющего драйверных онкогенных мутаций, является назначение от четырех до шести циклов платиносодержащих комбинаций цитостатиков [7]. Однако у подавляющего большинства больных в течение полугода развивается прогрессирование злокачественного процесса, а у каждого четвертого пациента какой-либо эффект химиотерапии полностью отсутствует [8].
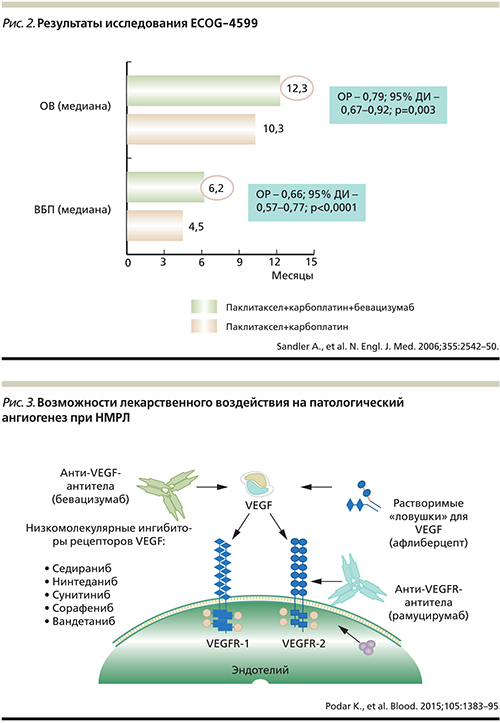
За последние десятилетия было проведено более 15 рандомизированных клинических исследований, посвященных второй линии лекарственной терапии НМРЛ [9]. Однако практически ни в одном из них не было продемонстрировано значимого улучшения общей выживаемости (ОВ) как в общей популяции пациентов, так и в подгруппах основных гистологических типов: аденокарциномы или плоскоклеточного рака. Исключение составляют исследования BR.21 (сравнение эрлотиниба, ингибитора тирозинкиназы EGFR [Epidermal Growth Factor Receptor], с плацебо) и TAX317 (сравнение доцетаксела с наилучшей симптоматической терапией) [10]. Таким образом, к препаратам, рекомендуемым в настоящее время в качестве второй линии терапии НМРЛ, относятся цитостатики доцетаксел и пеметрексед (последний – для пациентов с неплоскоклеточным раком) и эрлотиниб [11, 12]. Поскольку пеметрексед – один из препаратов выбора в терапии первой линии больных неплоскоклеточным НМРЛ, доцетакселу принадлежит ведущая роль в последующем лекарственном лечении [13]. Клиническая эффективность лекарственной терапии второй линии представляется абсолютно недостаточной: частота объективного ответа не превышает 10%, медианы выживаемости без прогрессирования (ВБП) и ОВ – 3–4 и 7–9 месяцев соответственно [12].
Антиангиогенные препараты в лекарственной терапии местнораспространенного и метастатического НМРЛ
Неудовлетворенная потребность в эффективном и безопасном лекарственном лечении больных распространенным НМРЛ диктует необходимость создания новых препаратов, способных контролировать конкретные молекулярные мишени, ответственные за основные механизмы патологической жизнедеятельности. Одними из важнейших и, как оказалось, эффективных с точки зрения возможностей терапевтического воздействия мишеней являются проангиогенные сигнальные пути, необходимые для роста, развития и метастазирования злокачественной опухоли [14]. Патологический ангиогенез представляет собой процесс образования новых капиллярных кровеносных сосудов опухоли из уже существующей сосудистой сети (рис. 1).
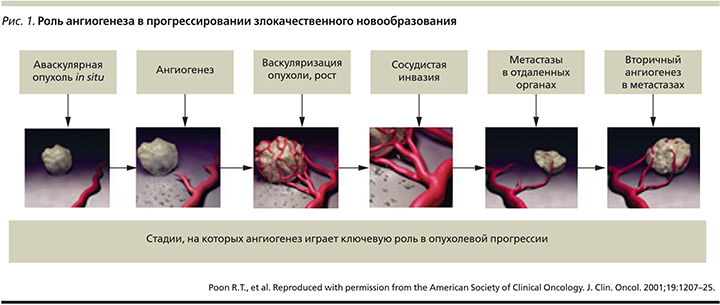
В этом сложном механизме взаимодействует масса различных факторов опухолевых клеток и клеток микроокружения, включая таковые эндотелия и гладкой мускулатуры, перициты и фибробласты. Ключевым фактором ангиогенеза является гипоксия, т.н. включатель ангиогенеза, приводящий к дисбалансу между про- и антиангиогенными факторами. Наиболее хорошо изученным путем, участвующим в опухолевом ангиогенезе, является сигнальный путь VEGF (Vascular Endothelial Growth Factor), включающий 6 факторов роста эндотелия сосудов (от VEGF-A до VEGF-D) и 3 рецептора (VEGFR-1, -2 и -3). Большинство применяемых в настоящее время антиангиогенных препаратов направлены в первую очередь на сигнальный путь VEGF и представляют собой либо моноклональные антитела, либо низкомолекулярные пероральные ингибиторы тирозинкиназ [15, 16].