STROKE №1 (37) / 2015
Эффективность антидепрессантов на моделях ишемического инсульта у животных. Систематический обзор и мета-анализ
Florey Institute of Neuroscience and Mental Health, University of Melbourne, Melbourne, Australia (S.K.M., E.S.S., D.W.H.); and Department of Clinical Neurosciences, University of Edinburgh, Edinburgh, United Kingdom (C.I., G.E.M., E.S.S., G.L.C., K.E.E., M.R.M). Приглашенныйредактор: C. Iadecola
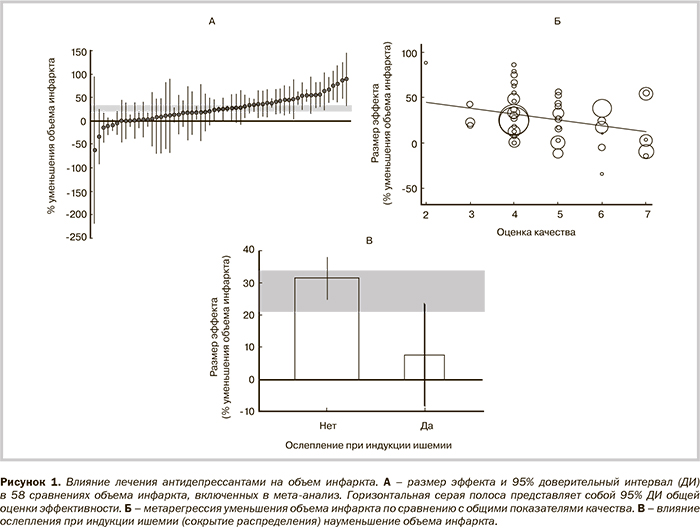
Предпосылки и цель исследования. Депрессия является распространенным осложнением инсульта с неясным патогенезом. Эффективность антидепрессантов в этом контексте и их роль в восстановлении после инсульта кроме влияния на настроение четко не определены, хотя в некоторых исследованиях продемонстрирована их эффективность в отношении улучшения функциональных исходов у пациентов после инсульта с депрессией и без депрессии. Нами были проанализированы данные доклинических исследований на животных и проведенное лечение антидепрессантами в модели очаговой церебральной ишемии с или без депрессии, что облегчило разработку дизайна клинического испытания. Методы. Был проведен систематический обзор и мета-анализ данных экспериментальных исследований эффективности применения антидепрессантов по сравнению с отсутствием лечения в отношении уменьшения объема инфаркта или улучшения нейроповедения или нейрогенеза в модели инсульта у животных. Для оценки влияния качества исследования и особенностей дизайна использовалась метарегрессия случайных эффектов, а для оценки наличия систематической ошибки – анализ trim and fill. Результаты. Мы выявили 44 публикации, описывающие эффекты 22 антидепрессантов. Медиана оценки по контрольному перечню для проверки качества составила 5 из 10 возможных баллов (межквартильный размах 4–7). В целом, назначение антидепрессантов приводило к уменьшению объема инфаркта на 27,3% (95% доверительный интервал от 20,7 до 33,8%) и улучшению нейроповеденческих исходов на 53,7% (46,4–61,1%). Выявили мало доказательств влияния селективных ингибиторов обратного захвата серотонина на объем инфаркта. В отношении нейроповеденческих исходов присутствовали признаки наличия систематической ошибки публикации. Селективные ингибиторы обратного захвата серотонина были наиболее часто изучаемым подтипом антидепрессантов; их применение приводило к улучшению нейроповеденческих исходов на 51,8% (38,6–64,9%) и увеличению нейрогенезана 2,2 СО (1,3–3,0). Выводы. В соответствии с современными клиническими данными и, несмотря на некоторые ограничения, лечение антидепрессантами, по всей видимости, приводит к уменьшению объема инфаркта и улучшению нейроповеденеческих исходов на моделях ишемического инсульта у животных.
Антидепрессанты широко используются для лечения депрессии после инсульта, несмотря на ограниченные доказательства их эффективности в этом контексте [1, 2]. В некоторых сравнительно небольших исследованиях было высказано предположение, что профилактическое лечение антидепрессантами может предотвратить развитие депрессии у некоторых пациентов. В последнее время высказываются сомнения по поводу роли селективных ингибиторов обратного захвата серотонина (СИОЗС) в улучшении восстановления двигательных функций у пациентов без депрессии после инсульта. Испытание флуоксетина в восстановлении двигательных функций пациентов с острым ишемическим инсультом (FLAME) было двойным слепым плацебо-контролируемым многоцентровым исследованием, в котором 118 пациентов с ишемическим инсультом и односторонней двигательной слабостью рандомизировали для приема флуоксетина в дозе 20 мг/сут или плацебо в течение 3 месяцев [3]. Через 90 дней улучшение оценки по шкале Fugl Meyer для моторной функции по сравнению с исходным значением было более выражено в группе флуоксетина. Кроме того, частота развития функциональной независимости (оценка по модифицированной шкале Рэнкина 0–2 балла) была значительно выше в группе флуоксетина (29% против 9%, р=0,015), хотя не было никакого существенного различия при других пороговых значениях модифицированной шкалы Рэнкина.
Доказательства того, каким образом антидепрессанты опосредуют развитие исходов после инсульта, в настоящее время ограничены, и существует несколько подходов, объясняющих эффективность антидепрессантов. Было показано, что флуоксетин ослабляет постишемическое повреждение головного мозга путем усиления экспрессии нейропротективных и регенеративных белков, подавления воспаления и постинсультной возбудимости в непораженных отделах головного мозга [4, 5]. СИОЗС могут также стимулировать образование нейронов [6, 7], секрецию факторов роста, которые увеличивают нейропластичность [8, 9], синаптическую пластичность [10], экспрессию церебрального фосфорилированного цАМФ, ответного элемента аткивирующего белка [11] и ослаблять гиперактивность гипоталамо-гипофизарной оси [12]. Благодаря этому снижается содержание кортизола, который ассоциирован с развитием неблагоприятных исходов после инсульта [13].
Уровень отсева вмешательств, разработанных в исследованиях на животных, перед проведением испытаний в клинических исследованиях [14] позволяет предположить необходимость более систематического подхода к трансляционной медицине инсульта [15]. Этот подход позаимствован из испытания с EuroHYP-1 (европейское мультицентровое рандомизированное клиническое испытание гипотермии с медикаментозным лечением против лучшего моно медикаментозного лечения при остром ишемическом инсульте, фаза III) [16]. В связи с этим в контексте дизайна клинического исследования по изучению эффективности флуоксетина при инсульте (http://www.focustrial.org.uk/) мы провели систематический обзор и мета-анализ данных экспериментальных исследований эффективности антидепрессантов на моделях инсульта у животных.
В частности, мы хотели установить наличие различий в эффективности по структурным (объем инфаркта) и функциональным (нейроповеденческим) исходам. В этих исходах предполагается преобладающее воздействие на регенерацию и репарацию, а не на гибель нейронов, а также временную зависимость наблюдаемой эффективности и отличие эффективности у животных, подверженных стрессовым воздействиям (которые могут моделировать аспекты депрессии). В дополнение к этому проанализировано наличие данных, подтверждающих любой специфический механизм действия. Полученные данные можно использовать для уточнения стратегии лечения. Также мы оценили вероятность наличия систематической ошибки в представленных данных, обусловленной факторами дизайна эксперимента или систематической ошибкой публикации.
МЕТОДЫ
Все методы были заранее определены в протоколе исследования, который можно изучить on-line по ссылке http:// www.dcn.ed.ac.uk/camarades//research.html. Это исследование выполнено в соответствии со стандартами проведения систематических обзоров и мета-анализов исследований у животных, разработанных Sena и соавт. [17]. В качестве первичной конечной точки был выбран размер инфаркта как более сложный тест оценки эффективности возможного нейропротективного действия антидепрессантов, которые могут повлиять на принятие решений о сроках лечения в клинических испытаниях. Наблюдаемое влияние на нейроповеденческие показатели может быть замаскировано воздействием на внимание и беспокойство, влияющих на выполнение задач. Вторичными конечными точками были влияние антидепрессантов на нейроповеденческие показатели и нейрогенез.
Стратегия поиска
Поиск проводился в 4 on-line базах данных (PubMed, WebofScience, Biosis, и Embase) в мае 2013 г. с исполь...












