Клиническая Нефрология №4 / 2018
Эффективность и безопасность противовирусной терапии глекапревир+пибрентасвир для больных с хроническим гепатитом С и хронической болезнью почек
1 ФГБОУ ВО «Самарский государственный медицинский университет» МЗ РФ; Россия, Самара;
2 ГБУЗ «Самарский областной клинический центр профилактики и борьбы со СПИДом»; Самара, Россия
Цель. Оценить эффективность и безопасность терапии глекапревир+пибрентасвиром больных хроническим гепатитом С (ХГС) и хронической болезнью почек на основе оценки динамики клинико-лабораторных показателей.
Материал и методы. Обследованы 13 пациентов с ХГС и хронической болезнью почек, из них 8 мужчин и 5 женщин. Средний возраст – 48±3,14 года. Противовирусная терапия (ПВТ) проводилась в течение 8 и 12 недель. Выполнялись общеклинические и биохимические анализы крови, для пациентов с ко-инфекцией ВИЧ выполнялся контроль вирусной нагрузки РНК ВИЧ и уровень СD4+-лимфоцитов.
Результаты. Полностью завершили курс ПВТ 12 пациентов. У одного из них курс ПВТ составил 10 недель в связи с развитием побочных эффектов, не связанных с ПВТ, в виде инфекции сосудистого доступа для проведения программного гемодиализа, сопровождавшегося повышением температуры тела до 40°С. Тем не менее у всех 13 пациентов зафиксирован устойчивый вирусологический ответ (100%). У 10 пациентов произошла нормализация показателей аланинаминотрансферазы на фоне или после окончания ПВТ.
Заключение. Схема ПВТ «глекапревир+пибрентасвир» продемонстрировала 100%-ную эффективность для пациентов с вирусным гепатитом С и хронической болезнью почек III–V стадий, в т.ч. получавших программный гемодиализ, а также показала удовлетворительный профиль безопасности.
Введение
С момента открытия вируса гепатита С стала очевидной определенная связь между персистированием хронического вирусного гепатита С (ХГС) и поражением почек, которое относится к одному из наиболее значимых системных клинических проявлений течения ХГС и имеет существенное значение для клинической нефрологической практики [1–3]. Так, было показано явное преобладание антител к вирусному гепатиту С (ВГС) у лиц с патологией почек по сравнению с донорами крови в регионах как с высокой, так и с низкой распространенностью ХГС, а также у лиц с острыми и хроническими нефропатиями после трансплантации почки [3–5].
Кроме того, у пациентов с ХГС значительно чаще имеют место реакции отторжения почечного трансплантата, развитие мембранознопролиферативного гломерулонефрита и мембранозной нефропатии [4–6]. Имеются данные о большей распространенности и гломерулярных, и тубулоинтерстициальных повреждений у пациентов с ХГС ассоциированными формами гломерулопатий [6, 8, 9].
Явную ассоциацию ХГС с развитием гломерулопатий подтверждают морфологические исследования, указывающие на высокую распространенность поражений клубочков в этой популяции пациентов [5, 7, 9]. Наконец, связь между ХГС и поражением почек также подтверждается и наблюдениями о положительной динамике почечных симптомов на фоне успешной противовирусной терапии – ПВТ [10–12].
У пациентов отделений хронического гемодиализа отмечается низкий уровень иммунной защиты, что служит причиной стертого течения вирусных гепатитов В и С [1, 13, 14]. В связи с этим многие больные центров хронического гемодиализа переносят малосимптомные формы как острых, так и хронических форм заболевания. На высокую частоту хронизации вирусных гепатитов у больных в терминальной стадии хронической почечной недостаточности (ХПН) указывает большинство исследований (F. Fabrizi et al., 2000; F. Fabrizi, F. Lokatelli, 1999; K. Ocuda et al., 1998).
T. Morisava et al. (1999) объясняют малосимптомное течение ХГС у больных в терминальной стадии ХПН тем, что эти пациенты систематически получают лечение гемодиализом, в результате чего происходит регулярное удаление вирусов и продуктов их жизнедеятельности из кровеносного русла, а следовательно, снижается уровень виремии [15, 16].
Отдельной проблемой служит лечение больных ХПН, инфицированных вирусами гепатитов В и С. Большинство исследователей связывают эффективность ПВТ у больных ВГС с генотипом вируса (N.N. Zein, 2000; G. Ballardini et al., 1997; M.U. Mandelli et al., 1997).
Классические схемы ПВТ с использованием препаратов (ПЕГ)-интерферона и рибавирина сопряжены с множеством осложнений. Однако в связи с необходимостью дозировать рибавирин в зависимости от скорости клубочковой фильтрации (СКФ), риском необратимого ухудшения функции почек, а также побочными эффектами интерферона данный режим рекомендован в руководствах с оговорками [2, 8]. При этом частота достижения устойчивого вирусологического ответа (УВО) при данном лечении составляет примерно 40–60%. В связи с этим проведение безинтерфероновой ПВТ особенно обосновано для данной категории пациентов.
В отечественной литературе практически отсутствуют данные о применении препаратов интерферона больными вирусным гепатитом в терминальной стадии ХПН, находящимся на программном гемодиализе.
Материал и методы
Группа пациентов ВГС+хроническая болезнь почек (ХБП) включала 13 пациентов, преимущественно мужчин (8 человек). Средний возраст составил 48±3,14 года.
Характеристика пациентов представлена в табл. 1.
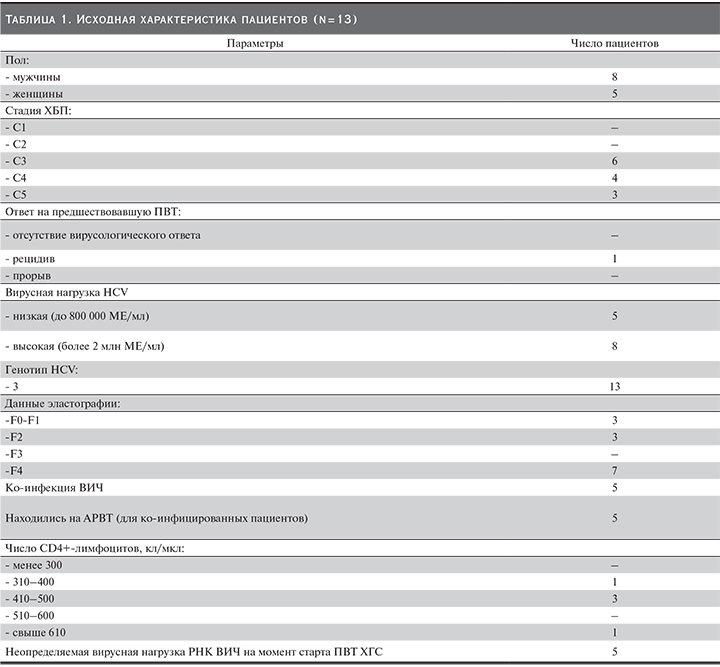
При объективном обследовании у наших пациентов до начала ПВТ в клинической картине преобладали признаки астеновегетативного синдрома, также отмечались жало...












