Кардиология №7 / 2013
Электрокардиографические изменения при метастатических опухолях предсердий
ГБОУ ДПО Иркутская государственная медицинская академия последипломного образования Минздрава РФ, 664049 Иркутск, микрорайон Юбилейный, 100; ГБУЗ Областной онкологический диспансер
Представлены 2 случая прижизненной диагностики вторичной опухоли левого предсердия при раке легкого и раке пищевода. Поражение миокарда было обусловлено инвазией первичной опухоли. В обоих наблюдениях на электрокардиограмме обнаружена депрессия сегмента PQ (PR), что может отражать опухолевое повреждение предсердия. Предложено рассматривать данный феномен в качестве электрокардиографического маркера вторичной неоплазии предсердий.
Вторичные злокачественные опухоли сердца встречаются значительно чаще первичных — у 0,4—18,3% от общего числа умерших онкологических больных [1—4]. Вероятность метастазирования в миокард наиболее высока при раке легкого, желудка, левой молочной железы, лимфоме [4—6]. Однако прижизненная диагностика вторичных неоплазий сердца затруднена и составляет лишь 8,5—10% от числа находок на аутопсии [4, 7]. Это объясняется преимущественно бессимптомным течением, отсутствием специфических клинических и инструментальных признаков. Вместе с тем в связи с широким использованием компьютерной и магнитно-резонансной томографии, с одной стороны, и увеличением продолжительности жизни больных раком — с другой, частота обнаружения вторичных опухолей сердца в последнее десятилетие увеличилась [3].
Приводим два клинических случая прижизненной диагностики опухолевого поражения миокарда предсердий, которое сопровождалось особыми изменениями на электрокардиограмме (ЭКГ).
Случай 1. Мужчина 49 лет, обратился в клинику в мае 1999 г. При поступлении предъявлял жалобы на умеренную одышку при ходьбе, сердцебиение, колющие длительные боли в области сердца, подъемы артериального давления (АД) до 180/110 мм рт.ст. Хронических заболеваний внутренних органов в анамнезе не отмечал. Курил в течение 20 лет. При аускультации легких справа дыхание везикулярное, слева — жесткое. Тоны сердца приглу шены, ритм правильный. Частота сердечных сокращений 90 уд/мин, АД 175/95 мм рт.ст.
У больного выявлены нормохромная анемия легкой степени, нейтрофильный лейкоцитоз (9,8×109/л), скорость оседания эритроцитов составила 58 мм/ч. На рент-генограмме грудной клетки определена картина центрального рака левого легкого с ателектазом. По данным фибробронхоскопии, левый главный бронх сужен инфильтративной опухолью. Гистологическое строение опухоли — плоскоклеточный рак без ороговения.
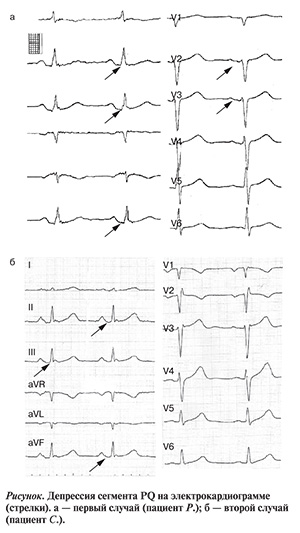
На ЭКГ от 22.05.99 синусовая тахикардия 94 в 1 минуту. Признаки перегрузки правых отделов. В отведениях II, III, aVF, V2—V4 отмечается депрессия сегмента PQ на 0,2 мВ, в aVL — его элевация на 0,1 мВ (см. рисунок, а). В этой связи для исключения перикардита и инфаркта предсердий у больного определена фракция МВ креатинфосфокиназы (КФК-МВ) крови, выполнена эхокардио-графия (ЭхоКГ). Уровень КФК-МВ составил 18 МЕ/л.