Терапия №3 / 2025
Ингибиторы натрий-глюкозного котранспортера 2-го типа: революция в лечении хронической сердечной недостаточности
ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России (Пироговский университет), г. Москва
Аннотация. Сахарный диабет 2-го типа (СД 2) и хроническая сердечная недостаточность (ХСН) – мультидисциплинарные заболевания, ассоциированные с чрезвычайно неблагоприятным прогнозом и высокой летальностью. При наличии СД 2 течение ХСН характеризуется большей тяжестью, ранней инвалидизацией и повышенной частотой госпитализаций. Крупные исследования по оценке сердечно-сосудистых исходов (CVOT) продемонстрировали значимые органопротективные свойства ингибиторов натрий-глюкозного котранспортера 2-го типа у пациентов с СД 2. Эти исследования впервые показали возможность снижения общей и сердечно-сосудистой смертности, а также частоты госпитализаций по причине ХСН как у пациентов с СД 2, так и без него. Расширение показаний к применению ингибиторов натрий-глюкозного котранспортера 2-го типа ознаменовало собой значительный прорыв в терапии сердечной недостаточности, что, в свою очередь, привело к формированию новой терапевтической парадигмы, охватывающей всех пациентов с ХСН, вне зависимости от этиологии, стадии заболевания и величины фракции выброса левого желудочка. Результатом этого стало достижение клинически значимого улучшения прогноза и повышение качества жизни пациентов, что в настоящее время нашло официальное отражение в обновленных клинических рекомендациях ведущих кардиологических сообществ мира, включая Европейское общество кардиологов, Американскую ассоциацию сердца и Российское кардиологическое общество.
ВВЕДЕНИЕ
Сахарный диабет 2-го типа (СД 2) в настоящее время признан социально значимой проблемой, приводящей к массовой инвалидизации населения и характеризующейся высоким бременем тяжелых осложнений. Известно, что в структуре смертности пациентов с СД 2 ведущие позиции занимают сердечно-сосудистые патологии, в частности хроническая сердечная недостаточность (ХСН) [1]. ХСН и СД 2 характеризуются высокой распространенностью в общей популяции, оказывают взаимное негативное влияние на течение друг друга и имеют тесную патофизиологическую связь, что обусловливает наличие ряда синергичных подходов к их лечению.
По официальным данным, ХСН страдают более 64 млн человек в мире, что составляет примерно 2% взрослого населения и делает это заболевание одной из главных неразрешенных проблем системы здравоохранения [2]. В исследовании Matsue Y. et al. распространенность ХСН у пациентов с СД 2 варьировала в пределах 25–40%. При этом у более чем трети пациентов, госпитализированных по поводу ХСН, впервые выявлялись нарушения уровня глюкозы натощак или нарушенная толерантность к глюкозе [3]. Прогноз пациентов с ХСН крайне неутешителен и, по некоторым данным, даже хуже, чем при отдельных видах злокачественных опухолей. Согласно результатам Фрамингемского исследования, средняя 5-летняя смертность у больных ХСН (с учетом начальных и умеренных стадий) составила 65% для мужчин и 47% для женщин, а на более тяжелых стадиях (3-я стадия) она превысила 70% [4]. Также в этом исследовании было показано, что СД 2 выступает значимым и независимым фактором риска развития ХСН, многократно увеличивающим вероятность ее возникновения. Повышение уровня гликированного гемоглобина на 1% ассоциировано с увеличением риска ХСН на 8–36%, а повышение уровня глюкозы на 1 ммоль/л – на 23%. Наличие диагноза СД 2 у больных ХСН связано с более тяжелым клиническим течением и высокой частотой госпитализаций, нередко приводящих к летальному исходу или тяжелой инвалидности. В крупном шведском исследовании с участием 404 480 пациентов, госпитализированных по поводу ХСН, трехлетняя летальность у пациентов с СД 2 была на 28% выше, чем в общей популяции (отношение рисков (ОР) 1,28, 95% доверительный интервал (ДИ): 1,26–1,29) [5]. Наличие ХСН ассоциировалось с двукратным возрастанием риска общей и сердечно-сосудистой смертности (ОР 2,05, 95% ДИ: 1,82–2,32 и ОР 2,02, 95% ДИ: 1,75–2,33 соответственно). Сочетание ХСН с хронической болезнью почек (ХБП) повышало этот риск почти в 4 раза (ОР 3,91, 95% ДИ: 3,02–5,07 и ОР 3,14, 95% ДИ: 2,90–3,40 соответственно) [5].
Таким образом, представленные данные подтверждают тесную взаимосвязь между СД 2 и ХСН, которая характеризуется высокой распространенностью, взаимно негативным влиянием и повышенным риском неблагоприятных исходов. Высокая сердечно-сосудистая смертность среди больных с СД 2 подчеркивает необходимость разработки и внедрения эффективных стратегий профилактики и лечения, направленных на снижение риска развития и прогрессирования ХСН в этой популяции.
ПАТОФИЗИОЛОГИЧЕСКИЕ АСПЕКТЫ РАЗВИТИЯ ХСН
ХСН – клинический синдром, характеризующийся симптомами и/или признаками, которые обусловлены структурными и/или функциональными нарушениями миокарда, подтвержденными повышенным уровнем натрийуретических пептидов и/или объективными признаками легочного или системного венозного застоя. В настоящее время выделяют 3 основных фенотипа ХСН: с сохраненной фракцией выброса левого желудочка (ФВ ЛЖ ≥ 50%), с умеренно сниженной ФВ ЛЖ (41–49%) и со сниженной ФВ ЛЖ (≤ 40%).
В развитии ХСН отмечают 2 основных патогенетических сценария (рис. 1).
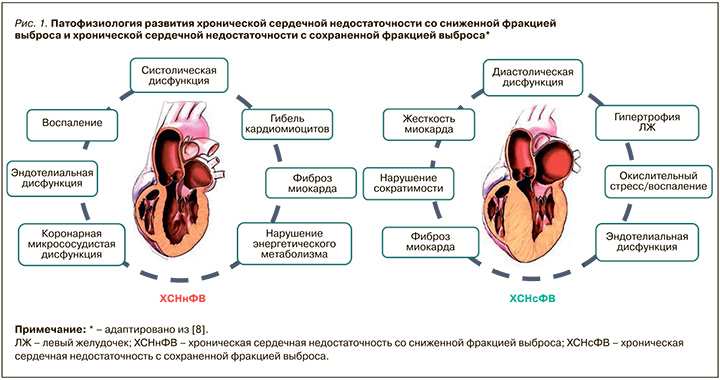
Первый сценарий связан со снижением функционирующих кардиомиоцитов в результате патологического воздействия (острого или хронического, например ишемического генеза). Снижение сердечного выброса активирует нейрогуморальные компенсаторные механизмы. Симпатическая нервная система, высвобождая адреналин и норадреналин, повышает общее периферическое сосудистое сопротивление и частоту сердечных сокращений, вызывая вазоконстрикцию. Снижение почечного кровотока и активация β1-адренорецепторов инициируют каскад реакций, опосредованных ренин-ангиотензин-альдостероновой системой (РААС). В юкстагломерулярном аппарате почек синтезируется ренин, катализирующий образование ангиотензина II. Последний вызывает вазоконстрикцию и стимулирует синтез альдостерона, который, в свою очередь, способствует задержке натрия и воды, повышая преднагрузку на сердце.
Таким образом, активируется механизм Франка – Старлинга: при увеличении венозного возврата стенки миокарда растягиваются, что приводит к изменению положения нитей актина, миозина и, как следствие, к увеличению силы сердечных сокращений. Компенсаторные механизмы вследствие гиперактивации нейрогуморальных систем нарушают передачу клеточных сигналов, приводят к воспалению, апоптозу и фиброзу, создавая условия...












