STROKE №4 (36) / 2014
Количество церебральных микрокровоизлияний и риск развития внутримозгового кровоизлияния после внутривенного тромболизиса
Klinik und Hochschulambulanz für Neurologie, Center for Stroke Research and Excellence Cluster NeuroCure, Charité–Universitätsmedizin Berlin, Berlin, Germany; Department of Brain Repair and Rehabilitation, UCL Institute of Neurology, London, United Kingdom; and The National Hospital for Neurology and Neurosurgery, London, United Kingdom.
В зависимости от типа формирования и характеристик выборки, приблизительно у 2–10% пациентов с ишемическим инсультом (ИИ) после проведения внутривенного тромболизиса (ВВТ) может развиться симптомное внутримозговое кровоизлияние (сВМК) [1]. Развитие сВМК резко снижает функциональное восстановление и независимо ассоциировано с более высоким уровнем смертности [2]. Таким образом, выявление предикторов развития сВМК является одним из основных направлений исследований при инсульте с целью улучшения оценки риска и пользы ВВТ.
Кроме клинических предикторов, таких как тяжесть инсульта и высокий уровень систолического артериального давления, появились визуализационные предикторы, включая выраженность лейкоареоза и наличие церебральных микрокровоизлияний (ЦМК), которые рассматривают в качестве возможных факторов риска развития сВМК [3, 4].
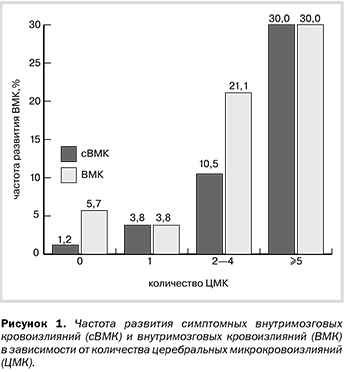 ЦМК представляют собой небольшие очаги периваскулярного скопления крови, которые можно обнаружить при магнитно-резонансной томографии (МРТ) с использованием последовательностей, чувствительных к кровоизлияниям [5, 6]. Они считаются маркером болезни мелких сосудов, для которой характерна предрасположенность к развитию кровоизлияний [5, 7], и ассоциированы с развитием внутримозговых кровоизлияний – ВМК [8]. Приблизительно у 12–39% пациентов с острым ИИ, которым показано проведение ВВТ, случайно обнаруживают ЦМК при проведении визуализации до начала лечения, и частота обнаружения зависит от характеристик выборки исследования (например, возраст и инсульт в анамнезе), силы магнитного поля томографа и применяемой МР-последовательности [4]. Влияние наличия ЦМК на риск развития ВМК после ВВТ до сих пор неизвестно [4, 9, 10]. До настоящего времени наличие ЦМК не считали противопоказанием для проведения ВВТ, но врачи, имеющие доступ к МРТ, сталкиваются с неопределенностью, особенно при наличии большого количества ЦМК. В последнем мета-анализе у лиц с ЦМК, обнаруженными до проведения ВВТ, частота развития сВМК составила 7,4% по сравнению с 3,6% у лиц без ЦМК, но различие не было статистически значимым (р=0,08) [4]. В ранее проведенных исследованиях не удалось четко установить, влияет ли число ЦМК на риск развития сВМК [10–17]. Недавно P.P. Gratz и соавт. [18]
ЦМК представляют собой небольшие очаги периваскулярного скопления крови, которые можно обнаружить при магнитно-резонансной томографии (МРТ) с использованием последовательностей, чувствительных к кровоизлияниям [5, 6]. Они считаются маркером болезни мелких сосудов, для которой характерна предрасположенность к развитию кровоизлияний [5, 7], и ассоциированы с развитием внутримозговых кровоизлияний – ВМК [8]. Приблизительно у 12–39% пациентов с острым ИИ, которым показано проведение ВВТ, случайно обнаруживают ЦМК при проведении визуализации до начала лечения, и частота обнаружения зависит от характеристик выборки исследования (например, возраст и инсульт в анамнезе), силы магнитного поля томографа и применяемой МР-последовательности [4]. Влияние наличия ЦМК на риск развития ВМК после ВВТ до сих пор неизвестно [4, 9, 10]. До настоящего времени наличие ЦМК не считали противопоказанием для проведения ВВТ, но врачи, имеющие доступ к МРТ, сталкиваются с неопределенностью, особенно при наличии большого количества ЦМК. В последнем мета-анализе у лиц с ЦМК, обнаруженными до проведения ВВТ, частота развития сВМК составила 7,4% по сравнению с 3,6% у лиц без ЦМК, но различие не было статистически значимым (р=0,08) [4]. В ранее проведенных исследованиях не удалось четко установить, влияет ли число ЦМК на риск развития сВМК [10–17]. Недавно P.P. Gratz и соавт. [18]
не обнаружили доказательств того, что большое количество ЦМК оказывает влияние на риск развития сВМК у пациентов, в лечении которых использовали различные методы реваскуляризации. Следует отметить, что <50% пациентов провели только ВВТ.
Это может иметь большое значение, поскольку разные методы реваскуляризации несут за собой разные риски развития кровоизлияния.
Цель настоящего исследования заключалась в изучении влияния числа ЦМК на исходной МРТ на риск развития сВМК, ВМК и функциональный исход в однородной группе пациентов с ИИ, получавших ВВТ.
МЕТОДЫ
Выборка исследования и сбор данных
В период с января 2008 по август 2013 г. данные всех пациентов, поступающих с острым ИИ, которым проводили ВВТ, регистрировали в постоянно действующем проспективном реестре [19]. Рекомбинантный тканевой активатор плазминогена (альтеплазу) вводили внутривенно в первые 4,5 часа от момента появления симптомов инсульта. Пациентам с неизвестным временем появления симптомов проводили ВВТ на основании отрицательных результатов МРТ в режиме с подавлением сигнала свободной воды [20].
Критериями включения в настоящее исследование были проведение ВВТ на основе результатов МРТ и выполнение повторной МРТ или компьютерной томографии (КТ) в течение 36 часов после ВВТ. Решение о проведении МРТ или КТ принимали в соответствии с наличием противопоказаний к МРТ и доступности метода визуализации. МРТ можно было провести только в рабочее время (с 8:00 утра до 5:00 вечера по будням). Пациентов исключали из анализа, если качество T2* изображений до начала лечения не позволяло точно оценить наличие ЦМК из-за артефактов движения или если при лечении использовали дополнительные эндоваскулярные методы реваскуляризации в связи с различными протоколами лечения и, возможно, более высоким риском развития кровоизлияний.
Как было описано ранее [19], исходные характеристики пациентов получали из историй болезни; регистрировали возраст, пол и анамнез заболевания, в т.ч. наличие артериальной гипертензии, гиперлипидемии, сахарного диабета, перенесенного инсульта, фибрилляции предсердий и прием препаратов, применяемых до поступления в стационар. Тяжесть инсульта оценивали опытные эксперты с использованием шкалы тяжести инсульта Национальных институтов здравоохранения (NIHSS). Степень лейкоареоза оценивали по валидизированной шкале возрастных изменений белого вещества головного мозга (ARWMC) [21].
Протокол визуализации
Все МР-исследования выполняли на сканере 3Т Tim Trio Siemens. Получали T2*-взвешенные (TR 620 мс; TE 20 мс; FOV 220 мм; матрица 256×192; толщина среза 5 мм) и диффузионно-взвешенные изоб...
50%>












