Урология №3 / 2018
Компьютер-ассистированные лапароскопические операции при хирургическом лечении рака почки
ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова», НИИ уронефрологии и репродуктивного здоровья человека Минздрава России (Сеченовский Университет), Москва, Россия
Цель исследования: оценить эффективность и преимущества использования 3D-планирования и виртуального осуществления операций при хирургическом лечении пациентов с локализованным раком паренхимы почки из лапароскопического доступа.
Материалы и методы. В ретроспективный анализ были включены данные 558 пациентов с почечно-клеточным раком (ПКР), подвергнутых хирургическому лечению в клинике урологии Первого МГМУ
им. И. М. Сеченова с января 2012 по май 2017 г. В 244 (43,7%) наблюдениях выполнена лапароскопическая радикальная нефрэктомия (ЛРН), в 314 (56,3%) – лапароскопическая резекция почки (ЛРП). Из дополнительных методов обследования 248 (44,4%) больным на основании выполненной мультиспиральной компьютерной томографии (МСКТ) проведено 3D-моделирование и виртуальное осуществление операций при помощи программы 3D-моделирования «Amira». Из каждой группы больных с выполненным 3D-планированием и без него были подобраны сопоставимые пары по основным признакам: однородность операторов и их опыта при выполнении операции, размер и локализация опухоли (отношение к сегменту, передней и задней поверхности), вариант хирургического доступа. По итогам было сформировано по две однородные подгруппы больных с выполненной ЛРН (по 22 пациента) и с выполненной ЛРП (по 53 пациента), которым 3D-планирование проводилось и нет.
Результаты. Пациенты с ПКР, прооперированные в объеме ЛРП, которым проведено 3D-планирование, имели статистически значимое преимущество перед больными без виртуального планирования: по времени тепловой ишемии – 12,0±6,4 мин (р=0,010), времени выполнения операции – 113,4±39,4 мин (р=0,0001), по величине кровопотери – 102,8±98,2 мл (р=0,001). При анализе пациентов с ПКР, перенесших операцию ЛРН, подгруппа с 3D-планированием также имела преимущество по времени выполнения операций -135,2±27 и 202,9±55,5 мин (р=0,0001), величине кровопотери – 143,2±137,4 и 472,0±395,4 мл (р=0,014), по частоте развития интра- (р=0,017) и послеоперационных (р=0,017) осложнений.
Заключение. Применение компьютер-ассистированных технологий в объеме 3D-планирования и виртуального осуществления операций позволяет улучшать непосредственные результаты оперативных пособий для пациентов с ПКР при выполнении органосохраняющих и органоуносящих операций из лапароскопического доступа.
Введение. Рак почки в настоящее время занимает 9-е место по частоте развития среди всех злокачественных новообразований у мужчин и 14-е – у женщин во всем мире [1, 2]. Среди новообразований почки на почечно-клеточный рак (ПКР) приходится 90% всех видов опухолей почки в мире [3]. По данным ракового регистра, в США за последнее десятилетие тенденции роста выявления ПКР стабилизировались с середины 2000 г. по сравнению с ежегодным приростом с уровня 1995 г. на протяжении 10 лет за счет улучшения визуализации и более частого выявления образований почки. Уровень смертности от рака почки с 1995 по 2005 г. с каждым годом имеет тенденцию к падению на 1% в год. Две трети образований почки диагностируются на ранней стадии, для данной категории пациентов 5-летняя относительная выживаемость составляет 93%[4].
 В настоящее время основным радикальным методом лечения рака паренхимы почки считается хирургический. По данным рекомендаций РОУ (Российское общество урологов), EAU (European Association of Urology) и АUА (American urological Association), «золотым» стандартом в лечении ПКР стадии Т1а являются органосохраняющие операции (ОСО), при стадии Т1b и Т2 ОСО выполняются при наличии технической возможности проведения оперативного пособия [5–7]. В текущем десятилетии предпочтение в хирургическом лечении ПКР отдают ОСО [8, 9]. Основанием послужили результаты ряда мировых исследований, где было установлено, что пациенты, подвергшиеся ОСО, имеют лучшие функциональные и онкологические результаты лечения [10]. Успех ОСО напрямую зависит от знания и понимания хирургом топографо-анатомических и патологоанатомических характеристик образований почки на этапе предоперационного планирования и в ходе оперативного вмешательства. В настоящее время выполняемые в предоперационном периоде обследования с помощью визуализирующих методов диагностики: мультиспиральная компьютерная (МСКТ), магнитно-резонансная томографии (МРТ) в режиме 2D, не всегда обеспечивают хирурга полной информацией об области оперативного вмешательства. Для решения данной проблемы в большинстве ведущих урологических клиник мира используется 3D-моделирование и планирование оперативного вмешательства [11–14]. В клинике урологии Первого МГМУ им. И. М. Сеченова метод предоперационного виртуального планирования на основании 3D-моделирования патологического процесса используется с 2009 г. Ранее в клинике проводились исследования по определению эффективности 3D-моделирования при выполнении оперативных вмешательств в отношении пациентов с ПКР из открытого доступа [15]. В настоящее время при выборе операционного доступа предпочтение отдается высокотехнологичным видам оперативных пособий-лапароскопическому и робот-ассистированному [16, 17].
В настоящее время основным радикальным методом лечения рака паренхимы почки считается хирургический. По данным рекомендаций РОУ (Российское общество урологов), EAU (European Association of Urology) и АUА (American urological Association), «золотым» стандартом в лечении ПКР стадии Т1а являются органосохраняющие операции (ОСО), при стадии Т1b и Т2 ОСО выполняются при наличии технической возможности проведения оперативного пособия [5–7]. В текущем десятилетии предпочтение в хирургическом лечении ПКР отдают ОСО [8, 9]. Основанием послужили результаты ряда мировых исследований, где было установлено, что пациенты, подвергшиеся ОСО, имеют лучшие функциональные и онкологические результаты лечения [10]. Успех ОСО напрямую зависит от знания и понимания хирургом топографо-анатомических и патологоанатомических характеристик образований почки на этапе предоперационного планирования и в ходе оперативного вмешательства. В настоящее время выполняемые в предоперационном периоде обследования с помощью визуализирующих методов диагностики: мультиспиральная компьютерная (МСКТ), магнитно-резонансная томографии (МРТ) в режиме 2D, не всегда обеспечивают хирурга полной информацией об области оперативного вмешательства. Для решения данной проблемы в большинстве ведущих урологических клиник мира используется 3D-моделирование и планирование оперативного вмешательства [11–14]. В клинике урологии Первого МГМУ им. И. М. Сеченова метод предоперационного виртуального планирования на основании 3D-моделирования патологического процесса используется с 2009 г. Ранее в клинике проводились исследования по определению эффективности 3D-моделирования при выполнении оперативных вмешательств в отношении пациентов с ПКР из открытого доступа [15]. В настоящее время при выборе операционного доступа предпочтение отдается высокотехнологичным видам оперативных пособий-лапароскопическому и робот-ассистированному [16, 17].
Цель исследования: оценить эффективность и преимущества использования 3D-планирования и виртуального осуществления операций при хирургическом лечении пациентов с локализованным раком паренхимы почки из лапароскопического доступа.

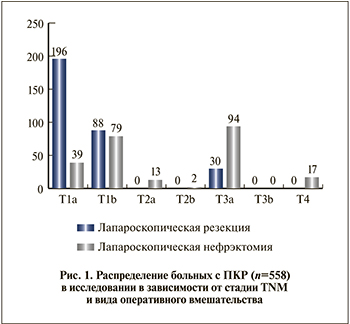
Материалы и методы. В ретроспективный анализ включены данные 558 пациентов с ПКР, подвергнутых хирургическому лечению в клинике урологии Первого МГМУ им. И. М. Сеченова с января 2012 по май 2017 г. В 244 (43,7%) наблюдениях выполнялась лапароскопическая радикальная нефрэктомия (ЛРН), в 314 (56,3%) – лапароскопическая резекция почки (ЛРП) (рис. 1).
Средний возраст больных составил 55,85±10,5 (25–78) лет. Мужчин было 307 (55%), женщин – 251(45%). Всем пациентам в предоперационном периоде проведены стандартные физикальное и инструментальное обследования. Из дополнительных методов обследования 248 (44,4%) больным на основании данных МСКТ проведено 3D-моделирование и виртуальное осуществление операций при помощи программы 3D-моделирования «Amira». Распределение больных в зависимости от стадии TNM и вида оперативного вмешательства представлено в табл. 1.
Виртуальное планирование и осуществление операций выполнялись на основании алгоритма, разработанного в нашей клинике (рис. 2).

Виртуальное осуществление оперативных вмешательств по алгоритму выполнялось хирургом накануне оперативного вмешательства, а также с целью навигации на этапе проведения операции в самой операционной с использованием ноутбука, на котором хирурги имели возможность сопоставлять данны...












