Терапевтический справочник. Путеводитель врачебных назначений №1 (6) / 2018
ОСТЕОАРТРОЗ
Кафедра факультетской терапии им. акад. А.И. Нестерова, ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава РФ
Ревматические заболевания и, в частности, болезни опорно-двигательного аппарата занимают первые места по обращаемости к врачу среди хронических неинфекционных заболеваний. По данным ВОЗ, свыше 4% населения земного шара страдают различными заболеваниями суставов и позвоночника.
Более чем в 30% случаев временная нетрудоспособность и в 10% инвалидизация больных связаны именно с ревматическими заболеваниями. В России болезни опорно-двигательного аппарата являются социально отягощающим фактором, занимая 3-е по случаям временной нетрудоспособности среди всех классов болезней. О глобальной значимости заболеваний костно-мышечной системы наглядно говорит тот факт, что первое десятилетие XXI в. было объявлено ВОЗ Международной декадой костей и суставов (The Bone and Joint Decade 2000—2010), которая проходила под эгидой борьбы с болезнями суставов, остеопороза, болей в спине, тяжелых травм конечностей, детских мышечно-скелетных нарушений.
ЭТИОЛОГИЯ
Исследования, инициированные в рамках Международной декады костей и, суставов дали много нового в понимании патогенеза многих заболеваний, в том числе и остеоартроза (ОА). В настоящее время, описывая ОА, говорят о трех основных патогенетических процессах, характеризующих заболевание:
- увеличенный катаболизм матрикса суставного хряща;
- увеличенное ремоделирование костной ткани, приводящее на ранних стадиях заболевания к разрежению, а затем к утолщению кости и ухудшению ее качества;
- синовиальное воспаление, при котором выявляется увеличение экспрессии провоспалительных медиаторов.
В развитии ОА большое значение придают воспалению, которое затрагивает практически все структуры сустава с формированием хондрита, синовита и остеита. Хронический воспалительный процесс в синовиальной оболочке способствует изменению метаболизма хондроцитов с преобладанием катаболических (деструктивных) процессов над анаболическими (синтетическими). В основе нарушений метаболизма хряща лежат количественные и качественные изменения протеогликанов — белково-полисахаридных комплексов, обеспечивающих стабильность структуры коллагеновой сети, которая служит основой хрящевого матрикса. Немаловажную роль в этом играют цитокины (рис. 1), в частности интерлейкин-1 (ИЛ-1) и фактор некроза опухоли альфа (ФНО-α).
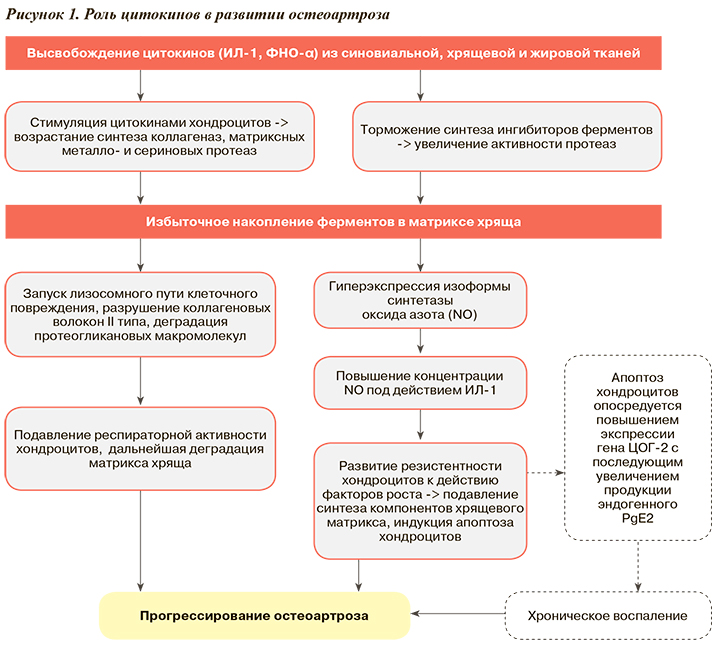
Высвобождение из хондроцитов и синовиальной ткани циклооксигеназы 2 типа (ЦОГ-2) и простагландинов E2 (PgЕ2) в значительной степени определяет интенсивность воспаления. Дегенерация хряща сопровождается поступлением в синовиальную жидкость продуктов деградации (фрагментов молекул протеогликанов и коллагена, мембран хондроцитов и др.), которые обладают антигенными свойствами и индуцируют выработку антител.
Морфологические изменения синовия при ОА сопоставимы с картиной синовита при хроническом артрите, включая развитие паннусподобных изменений. Секретируемые синовиальной оболочкой провоспалительные факторы могут не только усугублять деструкцию суставного хряща, но и активировать свертывающую систему крови, приводя к образованию микротромбов в сосудистом русле субхондральной кости. Повреждение сосудистой сети способствует развитию внутрикостной гипертензии с очаговой гипоксией и ишемией кости. Возникающие нарушения локального кровотока могут стать дополнительной причиной развития ишемических некрозов и усугубления болевого синдрома при ОА.
В настоящее время активно обсуждают роль изменений субхондральной кости в патогенезе ОА. С одной стороны, вследствие деструкции хряща субхондральная костная ткань подвергается значительным изменениям: возникают трабекулярные микротрещины и микропереломы, а нефизиологическое перераспределение физической нагрузки вызывает ее уплотнение, склероз и образование остеофитов. С другой стороны, субхондральная кость — метаболически активная ткань. Она продуцирует большое количество провоспалительных цитокинов и факторов роста, способных воздействовать на хрящевой матрикс. Установлено, что на ранних стадиях ОА происходит снижение минеральной плотности костной ткани (МПКТ) субхондральной кости. Кроме того, наибольшая степень деградации хряща наблюдается при большей выраженности и глубине изменений в архитектонике субхондральной кости. О важности изменений в субхондральной кости свидетельствует обратная зависимость между остеартрозом и заболеваниями, связанными с уменьшением минеральной плотности костной ткани, в т.ч. с остеопорозом.
В последние годы разрабатывается концепция вязкоэластической защиты сустава: упруговязкие свойства синовиальной жидкости и межклеточного матрикса хряща определяются содержанием в ней гиалуроната, а также влиянием жировой ткани в прогрессировании остеоартроза.
В целом изучение механизмов развития ОА показало, что это гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходом, подразделяемая на первичный (идиопатический) ОА и вторичный, возникающий на фоне различных заболеваний. На основании знаний фенотипа заболевания формируются основные принципы терапии.
ЛЕЧЕНИЕ
В соответствии с национальными рекомендациями лечение ОА должно быть комплексным и включать нефармакологические, фармакологические и хирургические методы. Терапевтическая тактика определяется основными целями:
- механическая раз...












