Фарматека №4 / 2019
Ожирение и ассоциированные заболевания. Современные возможности профилактики и лечения в условиях реальной клинической практики
1) Московский государственный медико-стоматологический университет им. А.И. Евдокимова, Москва, Россия;
2) Городская клиническая больница № 52 Департамента здравоохранения г. Москвы, Москва, Россия
Среди доказанных факторов риска развития неинфекционных заболеваний и смертности от них особую роль занимает ожирение, имеющее хронический рецидивирующий характер течения и высокую распространенность среди всех слоев населения независимо от пола и возраста. На сегодня к ассоциированным с ожирением заболеваниям относят более 10 нозологий, таких как сахарный диабет 2 типа (СД2), сердечно-сосудистые и онкологические заболевания, синдром поликистозных яичников, синдром обструктивного апноэ и многие другие, но, несомненно, лидирующее положение занимают заболевания сердечно-сосудистой системы и СД2. В настоящее время доказано, что терапия ожирения может замедлить развитие предиабета и являться одним из ключевых факторов в лечении СД2. Наряду с изменением образа жизни фармакотерапия является неотъемлемым этапом программы ведения больных ожирением. Убедительно доказано, что применение препаратов Редуксин® и Редуксин®Мет пациентами без противопоказаний эффективно и безопасно вне зависимости от наличия полиморбидной патологии и приема различной сопутствующей терапии.
Для цитирования: Маркова Т.Н. Ожирение и ассоциированные заболевания. Современные возможности профилактики и лечения в условиях реальной клинической практики. Фарматека. 2019;26(4):122–27. DOI: https://dx.doi.org/10.18565/pharmateca.2019.4.122-127
Введение
Глобальной проблемой современного здравоохранения является высокое распространение т.н. неинфекционных заболеваний (НИЗ). Ежегодно от них умирают более 40 млн человек. При этом 81% случаев смерти приходится на 4 группы заболеваний:
- Сердечно-сосудистые заболевания (инфаркт миокарда, инсульт и др.) служат основной причиной смерти от НИЗ – 17,7 млн человек ежегодно.
- Онкологические заболевания – 8,8 млн человек.
- Хронические респираторные болезни (хроническая обструктивная болезнь легких и бронхиальная астма) – 3,9 млн человек.
- Сахарный диабет – 1,6 млн человек [1, 2].
Ожирение как фактор риска НИЗ
Выявление модифицируемых факторов риска развития НИЗ и своевременная их коррекция должны лежать в основе комплексного подхода к решению рассматриваемой проблемы. Среди доказанных факторов риска развития НИЗ и смертности от них особую роль занимает ожирение, имеющее хронический рецидивирующий характер течения и высокую распространенность среди всех слоев населения независимо от пола и возраста. По данным многоцентрового (11 регионов РФ) наблюдательного исследования ЭССЕ-РФ (Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в регионах Российской Федерации) с участием 25 224 человек в возрасте 25–64 лет, распространенность ожирения в популяции составила 29,7% [3]. Причем с 2011 по 2015 г. заболеваемость ожирением среди взрослого населения возросла в 2,3 раза, а частота впервые поставленного диагноза с 2010 по 2016 г. возросла на 98,1% [4].
Роль ожирения как фактора риска хронических НИЗ рассматривается многими авторами [5–7]. Причинами формирования хронических НИЗ при ожирении являются наблюдаемое преимущественно при висцеральном ожирении хроническое воспаление; повышенное образование свободных жирных кислот, приводящее к липотоксичности; развитие резистентности к инсулину и ассоциированной гиперинсулинемии/глюкозотоксичности; избыток адипокинов и повышенная активность ароматазы, определяющие гормональные нарушения репродуктивной сферы; активация ренин-ангиотензин-альдостероновая системы (РААС) и другие факторы, связанные с накоплением избытка жировой ткани. Перечисленные патологические процессы в организме индуцируют развитие широкого спектра соматических заболеваний и состояний, значительно ухудшающих качество жизни больного и прогноз (рис. 1).
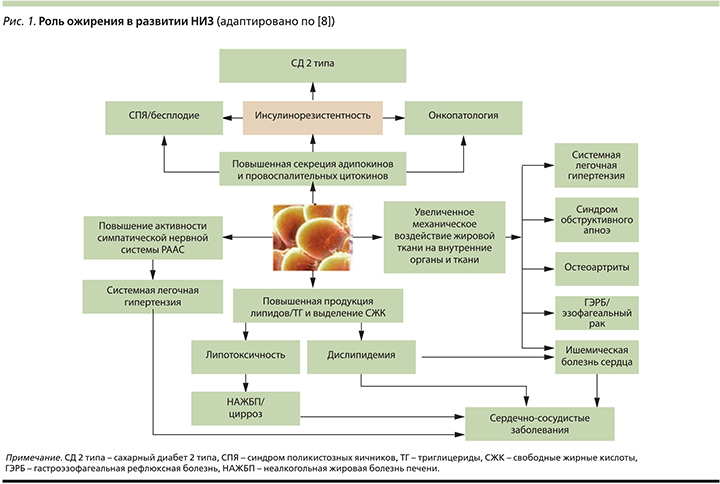
На сегодня к ассоциированным с ожирением заболеваниям относят более 10 нозологий, таких как СД2, сердечно-сосудистые и онкологические заболевания, синдром поликистозных яичников, синдром обструктивного апноэ и многие другие, но, несомненно, лидирующее положение занимают заболевания сердечно-сосудистой системы и СД2 [8].
В ряде исследований была доказана линейная зависимость между возрастанием массы тела и выраженностью артериальной гипертензии (АГ) [9, 10]. По материалам исследования ЭССЕ-РФ, частота АГ у лиц с абдоминальным ожирением в 2 раза превосходит таковую у лиц с нормальной массой тела, а у пациентов с ожирением градиентно возрастает с увеличением степени ожирения [11]. Патогенез развития АГ при ожирении многофакторный, включающий повышение активности РААС, задержку натрия в организме, нарушение эластичности сосудистой в стенке в условиях инсулинорезистентности. Одним из механизмов развития АГ при ожирении является увеличение тонуса симпатической нервной системы.
Lim S. et al. показали, что это достигается воздействием лептина и инсулина на гипоталамус [8, 12]. Связанный с этим повышенный тонус симпатической нервной системы способствует формированию и прогрессированию АГ, что дополнительно осложняет контроль АД [13].
Сахарный диабет 2 типа и ожирение
Хорошо известно, что ожирение и СД2 являются взаимосвязанными эпидемиями. При этом среди пациентов с ожирением повышается риск развития не только ранних нарушений углеводного обмена, но и СД2. В рамках национального эпидемиологического кросс-секционного исследования NATION, которое проводилось в 8 федеральных округах Российск...












