STROKE №2 / 2017
Оптимальный срок назначения антикоагулянтной терапии после внутримозгового кровоизлияния у пациентов с фибрилляцией предсердий
Department of Public Health and Clinical Medicine, Medicine and Department of Statistics, Umeå School of Business and Economics, Umeå University, Sweden; Department of Applied Mathematics, Computer Science and Statistics, Ghent University, Belgium.
Предпосылки и цель исследования. Цель настоящего исследования заключалась в предоставлении наблюдательных данных о связи между сроками назначения антитромботической терапии и конкурирующими рисками развития тяжелых тромботических и геморрагических событий в выборке шведских пациентов с фибрилляцией предсердий (ФП) и внутримозговым кровоизлиянием (ВМК). Методы.
В период с 2005 по 2012 г. в шведском реестре инсульта Riksstroke выявили пациентов с ФП и впервые развившимся ВМК. Изучали связь между реестром Riksstroke и другими национальными реестрами для получения информации о проводившемся лечении, наличии сопутствующих заболеваний и исходах. Оптимальные сроки назначения терапии у пациентов с низким и высоким рисками развития тромбоэмболических осложнений описали путем определения функций кумулятивной заболеваемости отдельно для тромботических и геморрагических событий и для комбинированной конечной точки в виде сосудистой смерти и нефатального инсульта. Результаты. В исследование включили 2619 пациентов, перенесших ВМК с ФП, период наблюдения составил 5759 человеко-лет. Назначение антикоагулянтной терапии было ассоциировано со снижением риска развития сосудистой смерти и нефатального инсульта у пациентов группы высокого риска, без значимого повышения риска развития тяжелых кровотечений. Наиболее эффективным было начало терапии через 7–8 недель после ВМК. У женщин группы высокого риска суммарный риск развития сосудистой смерти или повторного инсульта в течение 3 лет составил 17,0% на фоне антикоагулянтной терапии, начатой через 8 недель после ВМК, и 28,6% без назначения антикоагулянтов (95% доверительный интервал – ДИ для различия от 1,4 до 21,8%). У мужчин группы высокого риска соответствующие показатели составили 14,3 vs 23,6% (95% ДИ для различия от 0,4 до 18,2%). Выводы. По результатам настоящего обсервационного исследования можно сделать вывод, что для оптимизации эффективности терапии и минимизации риска антикоагулянтную терапию у пациентов с ФП следует начинать через 7–8 недель после ВМК.
За последние годы отмечается повышение заболеваемости фибрилляцией предсердий (ФП) и повышение частоты назначения оральных антикоагулянтов после внутримозгового кровоизлияния (ВМК) [1]. Тем не менее значительная доля таких пациентов не получают антикоагулянтной терапии, что отражает наличие противоречий в принятии решений о назначении терапии [2–5].
Существуют доказательства потенциальной эффективности антикоагулянтов у таких пациентов. В шведском популяционном исследовании частота развития повторных ишемических событий превышала частоту развития повторного ВМК у лиц, перенесших ВМК [6], и ВМК было независимым предиктором развития тромбоэмболических событий среди пациентов с ФП [7].
Результаты двух последних наблюдательных исследований, проведенных в Дании, подтверждают необходимость назначения оральных антикоагулянтов, т.к. такая терапия была ассоциирована со значительным снижением смертности от всех причин и риска развития ишемического инсульта – ИИ [8, 9].
Международные стандарты по оказанию медицинской помощи подчеркивают отсутствие доказательств в отношении необходимости назначения или возобновления антикоагулянтной терапии после ВМК [10, 11]. В крупнейшем ретроспективном исследовании, посвященном изучению оптимальных сроков для начала лечения, принимали участие 3 специализированных центра и 234 пациента с варфарин-ассоциированными ВМК. Пятьдесят девять пациентов возобновили прием антикоагулянтов и по результатам исследования пришли к выводу, что возобновление антикоагулянтной терапии следует отложить на срок от 10 до 30 недель во избежание повышения риска развития повторных кровоизлияний в раннем периоде после ВМК [12]. В отличие от этого, по данным систематического обзора, включавшего 492 пациентов, выдвинули предположение, что антикоагулянтную терапию у пациентов группы высокого риска можно возобновить через 3 дня после развития ВМК, но авторы подчеркнули наличие ограничений, свойственных проанализированным исследованиям [13].
Используя данные общенационального шведского реестра инсульта Riksstroke, мы изучили связь между сроками назначения антитромботической терапии и конкурирующими рисками развития серьезных тромботических событий, геморрагических событий и смерти от других причин у пациентов с ФП, перенесших ВМК.
МЕТОДЫ
Выборка исследования
В исследование включили всех пациентов с ФП, перенесших впервые развившееся ВМК (код по Международной классификации болезней 10-го пересмотра – МКБ-10: I61), зарегистрированных в реестре Riksstroke в период с 1 июля 2005 по 31 декабря 2012 г. Пациентов с травматическим ВМК, субдуральными гематомами и субарахноидальными кровоизлияниями не включали. Сведения о наличии ФП получали из реестра Riksstroke или шведского реестра стационарного лечения (МКБ-10: I48) за период с 1997 г. до даты развития ВМК.
Источники данных
Данные историй болезни пациентов были подробно отражены в нескольких базах данных Швеции, что позволяло получить информацию о характеристиках пациентов на момент развития ВМК, фактах назначения антитромботических препаратов после ВМК и дальнейшем развитии любых тяжелых клинических событий. Реестр Riksstroke был создан в 1994 г., и с 1998 г. в нем принимают участие все клиники, в которые поступают пациенты с острым инсультом в Швеции. Согласно оценкам, реестр охватывает >94% всех пациентов с острым инсультом [14]. Шведский реестр отпуска лекарств содержит общенациональную информацию обо всех выданных по рецепту в амбулаторном порядке медикаментах, и данные в него поступают из всех шведских аптек, начиная с 1 июля 2005 г. [15]. Шведский реестр стационарного лечения под управлением Национального совета здравоохранения и благосостояния характеризуется полным национальным охватом с 1987 г., и в нем регистрируются данные >99% всех выписок из стационара после лечения по поводу соматического заболевания. Диагностическая точность, согласно оценке положительной прогностической значимости, различается в зависимости от диагноза, но, как правило, составляет от 85 до 95% [16]. Информацию о социально-экономических факторах извлекали из базы данных продольной интеграции для исследований по медицинскому страхованию и рынку труда [17], контролируемой Статистическим управлением Швеции. Кроме того, провели изучение реестра причин смерти [18] под управлением Национального совета здравоохранения и благосостояния для получения информации о непосредственных и второстепенных причинах смерти.
Данное исследование было одобрено Советом по биомедицинской этике, Умео, Швеция (Dnr 2014-76-32M) в рамках расширения проекта EqualStroke Project (Dnr 2012-321-31M).
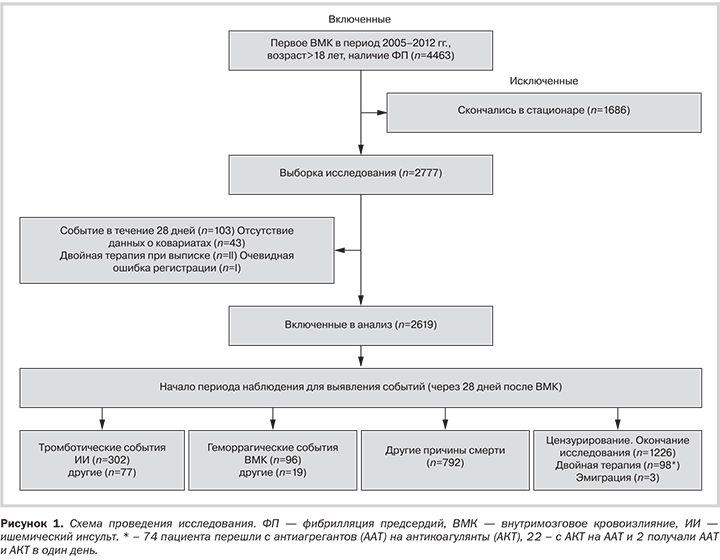
ОПРЕДЕЛЕНИЕ ПЕРЕМЕННЫХ
Переменные исхода
Определили два различных типа исходов. Во-первых, к тромботическим событиям отнесли случаи развития ИИ (фатального или нефатального) и все причины смерти,...












