Терапия №6 (16) / 2017
Особенности применения блокаторов ангиотензиновых рецепторов в клинической практике (фокус на кандесартан)
ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова, Москва
Современное лечение сердечно-сосудистых заболеваний включает назначение блокаторов рецепторов ангиотензина II. В настоящей статье представлен обзор литературных данных по эффективности, профилю безопасности кандесартана, высокой приверженности к данному препарату у больных с артериальной гипертонией, сахарным диабетом, хронической сердечной недостаточностью, хронической болезнью почек. Подчеркивается преимущества кандесартана в сравнении с другими представителями этой группы препаратов.
На сегодняшний день трудно представить лечение многих сердечно-сосудистых заболеваний без применения ингибиторов ренин-ангиотензин-альдостероновой системы (РААС): ингибиторов ангиотензинпревращающего фермента (иАПФ), блокаторов рецепторов ангиотензина ΙΙ (БРА). Появившиеся в конце 80-х гг. прошлого века БРА занимают лидирующие позиции в терапии таких распространенных заболеваний, как артериальная гипертензия (АГ), хроническая сердечная недостаточность (ХСН), хроническая болезнь почек (ХБП). Высокая клиническая эффективность первых лекарственных средств данного класса препаратов способствовала разработке новых представителей с улучшенными фармакологическими показателями. БРА являются самым назначаемым классом препаратов в мире с высокой приверженностью к лечению (рис. 1).
В нашей стране, согласно результатам исследования Пифагор IV, частота назначения БРА уступает частоте применения других антигипертензивных препаратов (иАПФ, диуретиков, бета-блокаторов, антагонистов кальция) и составляет 16 % [1].
Активация РААС лежит в основе большинства сердечно-сосудистых заболеваний, поэтому применение блокаторов РААС является патогенетически обоснованным [2].
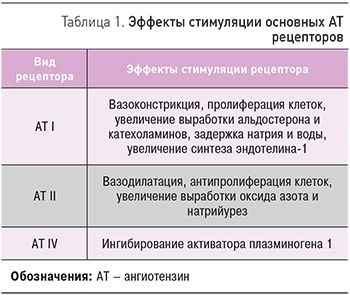
Ангиотензин (АТ) II образуется не только через механизм с участием ангиотензинпревращающего фермента. Применение иАПФ может приводить к активации альтернативных путей образования АТ II. АТ II реализует свое действие через специфические рецепторы. Наиболее изучены функции трех типов рецепторов к АТ II (табл. 1).
 АТ I рецепторы расположены в сосудах, сердце, почках и коре надпочечников. Действие БРА реализуется через снижение активности РААС на уровне рецепторов АТ II. БРА образуют с АТ I рецепторами прочную связь с последующей медленной диссоциацией, что предупреждает развитие или ослабляет эффекты АТ II. Косвенные механизмы действия БРА связаны со стимуляцией АТ II рецепторов. Препараты этой группы не влияют на метаболизм кининов и не приводят к появлению кашля. Частота развития кашля в плацебо-контролируемых клинических исследованиях составляет от 1 до 4,6%. Частота других побочных эффектов, таких как ангионевротический отек, кожные проявления, не превышает 1%. Они значительно реже вызывают гипотензию и коллаптоидные реакции. Эффект «первой дозы» (головокружение, слабость, постуральная гипотензия, обмороки) у антагонистов АТ I рецепторов менее выражен – частота гипотензии составляет менее 1%. В отличие от иАПФ, БРА не приводят к клинически значимой задержке калия. Гиперкалиемия развивается в менее 1,5% случаев. У этих лекарственных средств не регистрировался синдром отмены [2, 3]. Все препараты этой группы имеют общий механизм действия, но фармакологические свойства, различия во взаимодействии с рецепторами определяют особенности отдельных представителей и их разную клиническую эффективность.
АТ I рецепторы расположены в сосудах, сердце, почках и коре надпочечников. Действие БРА реализуется через снижение активности РААС на уровне рецепторов АТ II. БРА образуют с АТ I рецепторами прочную связь с последующей медленной диссоциацией, что предупреждает развитие или ослабляет эффекты АТ II. Косвенные механизмы действия БРА связаны со стимуляцией АТ II рецепторов. Препараты этой группы не влияют на метаболизм кининов и не приводят к появлению кашля. Частота развития кашля в плацебо-контролируемых клинических исследованиях составляет от 1 до 4,6%. Частота других побочных эффектов, таких как ангионевротический отек, кожные проявления, не превышает 1%. Они значительно реже вызывают гипотензию и коллаптоидные реакции. Эффект «первой дозы» (головокружение, слабость, постуральная гипотензия, обмороки) у антагонистов АТ I рецепторов менее выражен – частота гипотензии составляет менее 1%. В отличие от иАПФ, БРА не приводят к клинически значимой задержке калия. Гиперкалиемия развивается в менее 1,5% случаев. У этих лекарственных средств не регистрировался синдром отмены [2, 3]. Все препараты этой группы имеют общий механизм действия, но фармакологические свойства, различия во взаимодействии с рецепторами определяют особенности отдельных представителей и их разную клиническую эффективность.
 Одним из наиболее изученных представителей БРА является кандесартана цилексетил. Кандесартан так же, как и олмесартан, лозартан, ирбесартан, относится к бифениловым производным тетразола и представляет собой высокоселективный длительно действующий блокатор АТ II рецепторов первого типа. При всасывании из желудочно-кишечного тракта препарат гидролизуется до активного вещества кандесартана. Химическое название 1-[[(циклоксигексилокси) карбонил] окси] этил 2-этокси-1-[[2’(1Н-тетразол-5-ил)-1,1’-бифенил]-4-ил] метил]-1Н-бензимидазол-7-карбоновой кислоты. Основные фармакологические свойства кандесартана представлены в табл. 2.
Одним из наиболее изученных представителей БРА является кандесартана цилексетил. Кандесартан так же, как и олмесартан, лозартан, ирбесартан, относится к бифениловым производным тетразола и представляет собой высокоселективный длительно действующий блокатор АТ II рецепторов первого типа. При всасывании из желудочно-кишечного тракта препарат гидролизуется до активного вещества кандесартана. Химическое название 1-[[(циклоксигексилокси) карбонил] окси] этил 2-этокси-1-[[2’(1Н-тетразол-5-ил)-1,1’-бифенил]-4-ил] метил]-1Н-бензимидазол-7-карбоновой кислоты. Основные фармакологические свойства кандесартана представлены в табл. 2.
В отличие от других представителей БРА кандесартан характеризуется не только высокой селективностью к АТ ...












