Терапия №4 / 2019
Современный алгоритм диагностики хронической тромбоэмболический легочной гипертензии
1) Кафедра факультетской терапии им. акад. А.И. Нестерова ФГБОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва;
2) ГБУЗ «Городская клиническая больница № 1 им. Н.И. Пирогова» Департамента здравоохранения г. Москвы
В ряде случаев после перенесенной тромбоэмболии легочной артерии (ТЭЛА) полная реканализация легочного русла не происходит, эмболические массы лизируются частично и замещаются соединительной тканью. Это приводит к изменению просвета легочных сосудов и формированию хронической тромбоэмболической легочной гипертензии (ХТЭЛГ), которая является отдаленным осложнением ТЭЛА и встречается в 5–10 случаях на 1 млн населения. Более редкими причинами формирования этого вида легочной гипертензии могут быть сосудистые опухоли (чаще всего ангиосаркома), стеноз легочных артерий, некоторые паразитарные инфекции. Симптомы заболевания неспецифичны (одышка, боль в грудной клетке, кашель, кровохарканье), а упоминание в анамнезе на перенесенную ТЭЛА имеется не всегда, что затрудняет раннюю диагностику и своевременное лечение больных. Несмотря на имеющиеся рекомендации и проводимые исследования, не существует единых сроков и метода исследования для проведения скрининга пациентов с целью оценки формирования легочной гипертензии. В представленном обзоре освещены основные возможные методы диагностики ХТЭЛГ, рассмотрены их преимущества и недостатки, доступность в практике врача-клинициста. Сочетание нескольких диагностических исследований позволяет не только выявить это заболевание, но и выбрать дальнейшую тактику лечения – оперативное или медикаментозное.
Целью скрининга ряда заболеваний является выявление пациентов с доклинической или ранней стадией болезни для предотвращения или замедления прогрессирования его течения. Легочная гипертензия (ЛГ) представляет собой серьезное жизнеугрожающее состояние с высоким процентом летального исхода [1, 2]. Скрининговые программы для ранней диагностики ЛГ рекомендованы всем пациентам с системными заболеваниями (склеродермия, системная красная волчанка), при наличии ближайших родственников с подтвержденной идиопатической легочной артериальной гипертензией, перенесенной тромбоэмболией легочной артерии (ТЭЛА) в анамнезе и некоторыми другими патологиями. Ряд исследований продемонстрировал, что ранняя диагностика ЛГ, а соответственно и рано начатое лечение обеспечивали более высокие показатели выживаемости и отдаленного прогноза [1].
Хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) – это прекапиллярная форма ЛГ, при которой хроническая обструкция крупных и средних ветвей легочных артерий, а также вторичные изменения микроциркуляторного русла легких приводят к прогрессирующему повышению легочного сосудистого сопротивления и давления в легочной артерии с развитием тяжелой дисфункции правых отделов сердца и сердечной недостаточности [2]. Диагноз ХТЭЛГ может быть установлен как минимум после 3 мес адекватной антикоагулянтной терапии с момента эпизода острой ТЭЛА при наличии следующих критериев:
- среднего давления в легочной артерии (ДЛА) ≥25 мм рт.ст. и давления заклинивания в легочной артерии (ДЗЛА) ≤15 мм рт.ст.;
- несогласованных дефектов перфузии при сцинтиграфии легких и специфических диагностических признаках ХТЭЛГ, выявляемых по данным мультиспиральной компьютерной томографии (МСКТ) – ангиографии [3].
ОСОБЕННОСТИ ДИАГНОСТИКИ ХТЭЛГ
Ранняя диагностика ХТЭЛГ может иметь решающее значение для проведения эффективной терапии и во многом определять дальнейший исход заболевания. В Европейском регистре ХТЭЛГ было показано, что средняя продолжительность постановки диагноза с момента появления первых симптомов составляла около 14 мес, при этом 81% пациентов к этому времени имели III–IV функциональный класс (ФК) по NYHА [4]. Согласно имеющимся в настоящее время рекомендациям, нет четких сроков для дальнейшего наблюдения больных после эпизода перенесенной ТЭЛА. Кроме того, к группе риска по формированию ХТЭЛГ отнесены лишь те пациенты, у которых систолическое давление в легочной артерии (СДЛА) на момент острой ТЭЛА было высоким либо в дальнейшем сохранялись клинические симптомы [2, 3].
В одном из метаанализов было показано, что частота развития ХТЭЛГ после перенесенной острой ТЭЛА составляет от 0,57 до 1,3%. Эти статистические данные основывались на двух больших когортных исследованиях пациентов с анамнезом венозной тромбоэмболии и практически не имели критериев исключения. Авторами также было показано, что только 3% пациентов, выживших после эпизода острой ТЭЛА, попали в поле зрения врачей через 3–6 мес с момента этого эпизода [5, 6, 7, 8].
Основой патобиологических процессов при ХТЭЛГ выступает формирование тромботических масс, не подвергшихся лизису, которые позднее фиброзируются, что приводит к механической обструкции крупных и средних ветвей легочных артерий. Начальное повышение давления в легочной артерии вызывает развитие вторичных сосудистых изменений. Ремоделирование микроциркуляторного русла легких способствует прогрессированию ЛГ даже при отсутствии повторных тромбоэмболических событий. Финалом заболевания, как и при других формах ЛГ, становится тяжелая дисфункция правого желудочка (ПЖ) и сердечная недостаточность. Морфологическим субстратом ХТЭЛГ также служат генерализованный спазм артериол малого круга кровообращения вследствие высвобождения из тромбоцитов и эндотелия вазоконстриктивных субстанций, вторичное тромбообразование, прогрессивное ремоделирование мелких легочных артерий и артериол [2].
Можно выделить определенный алгоритм диагностики ХТЭЛГ, представленный ниже (рис.) [3]. Рассмотрим данный алгоритм более подробно.
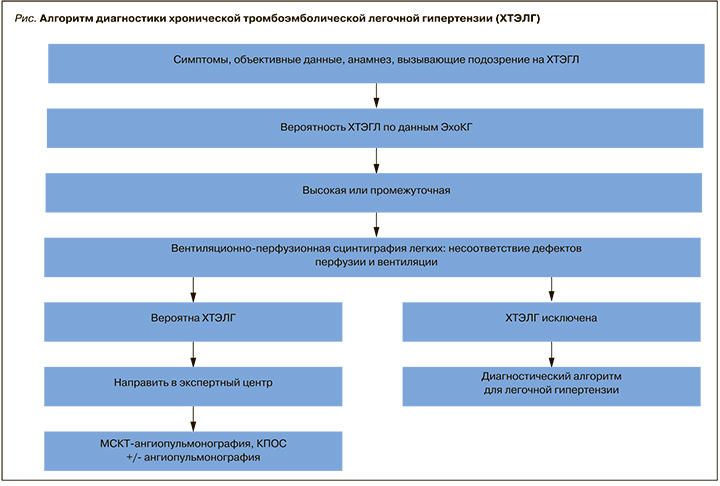
1. Клиническая картина
Сбор анамнеза и жалоб, объективный осмотр пациента – первый этап на пути диагностики ХТЭЛГ. Оценка клинических проявлений заболевания важна как для построения дальнейшего алгоритма обследования, так и определения эффективности проводимой терапии (уменьшение симптомов заболевания, повышение толерантности к физической ...












