Фарматека №5 / 2019
Тяжелая бронхиальная астма. Современные возможности диагностики и лечения
1) Уральский государственный медицинский университет, Екатеринбург, Россия;
2) Медицинское объединение «Новая больница», Екатеринбург, Россия
Статья содержит обзор литературных данных о критериях диагностики и современных подходах к лечению тяжелой бронхиальной астмы (ТБА), имеющей высокое медико-социальное значение. Для подтверждения диагноза необходима оценка аллергологического статуса, определение биологических маркеров заболевания. Рассматриваются существующие возможности терапии моноклональными антителами этой формы заболевания, а также наиболее изученные варианты будущего лечения ТБА.
Для цитирования: Лещенко И.В., Буладжова Т.З. Тяжелая бронхиальная астма. Современные возможности диагностики и лечения. Фарматека. 2019;26(5):110–20. DOI: https://dx.doi.org/10.18565/pharmateca.2019.5.110-120
Введение
Бронхиальная астма (БА) является гетерогенным заболеванием, характеризующимся хроническим воспалением дыхательных путей, наличием респираторных симптомов, таких как свистящие хрипы, одышка, заложенность в груди и кашель, которые варьируются по времени и интенсивности и проявляются вместе с вариабельной обструкцией дыхательных путей. Гетерогенность БА проявляется различными фенотипами заболевания, многие из которых возможно выделить в обычной клинической практике [1].
В клинической практике врача больные БА составляют значительную часть. Современное здравоохранение рассматривает БА, в частности тяжелую бронхиальную астму (ТБА), как глобальную проблему здравоохранения, охватившую весь мир.
В мире насчитывают около 300 млн человек, страдающих астмой, что составляет 5% населения планеты. Люди всех возрастов во всем мире страдают этим хроническим заболеванием дыхательных путей, которое при недостаточно эффективном лечении может значительно ограничивать повседневную жизнь пациентов и даже приводить к смерти [2].
Определено, что бронхиальная астма – многофакторное заболевание, на тяжесть течения которого влияют климат, расовая принадлежность, генетика, уровень развития общества, а также сопутствующая патология [2]. К ТБА относят пациентов, у которых контроль не достигается при использовании максимально высоких доз рекомендованных препаратов (рефрактерная астма, стероид-резистентная астма), а также больных, у которых контроль астмы достижим только при использовании максимальных доз лекарственных препаратов, включая системные глюкокортикостероиды (СГКС) [3].
Характеристика ТБА
Диагностика тяжелой терапевтически резистентной астмы требует тщательного уточнения и подтверждения диагноза, определения эндотипической и фенотипической характеристики заболевания и решения вопроса о назначении таргетной биологической терапии.
В зависимости от иммунологической характеристики воспаления выделяются Т2-эндотип и неТ2-эндотип [4].
- Т2-эндотип БА, реализуемый за счет преобладания Th2-ответа (аллергическая астма) или высокой активности врожденных лимфоидных клеток 2-го типа ILC – «innate lymphoid cells» (неаллергический и аллергический варианты БА) и проявляющиеся преимущественно эозинофильным воспалением. Т2-воспаление связано с высокими уровнями интерлейкина-5 (ИЛ-5) и ИЛ-13.
- НеТ2-эндотип БА, реализуемый, вероятно, через Тh1- и Th17-клетки и ассоциированный с преимущественно нейтрофильным воспалением в слизистой оболочке бронха. Характеристика фенотипов и эндотипов БА представлена в табл. 1 [2].
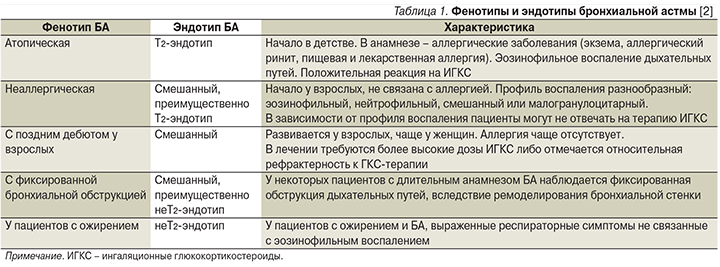
Фенотипы и эндотипы БА у одного и того же больного могут меняться. Неблагоприятная динамика заболевания чаще наблюдается у больных неаллергическим фенотипом БА под влиянием факторов окружающей среды, аллергенов, сезонных влияний, экологических факторов, инфекции органов дыхания, терапии ИГКС [5].
В табл. 2 дана клинико-иммунологическая характеристика фенотипов БА и особенно терапии [6].
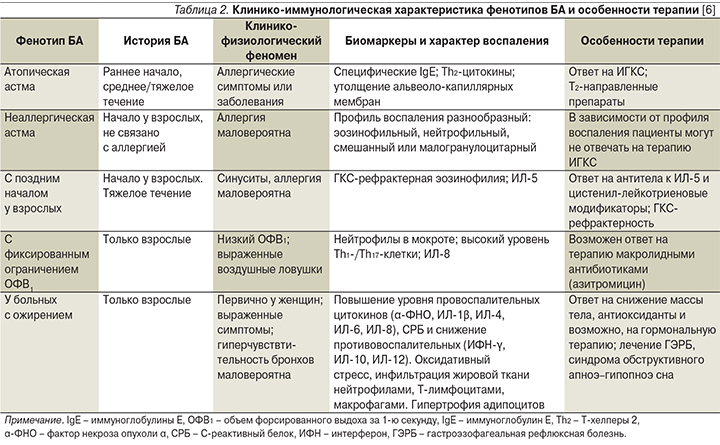
Определение фенотипа БА в клинической практике помогает врачу определять тактику ведения пациента, подбора дозировки ИГКС, прогнозировать эффективность лечения, а также проведения профилактических мероприятий.
Современные подходы к классификации БА основаны на выявлении специфических биомаркеров, лежащих в основе изменений бронхиального дерева. Биомаркеры, определяющие подходы к терапии БА, представлены в табл. 3 [7].
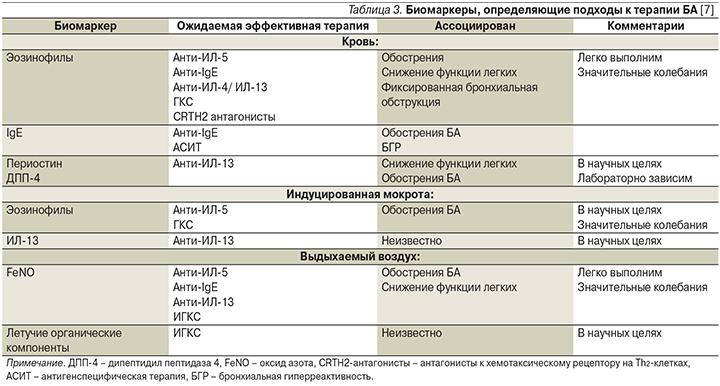
Эозинофилы индуцированной мокроты. Эозинофилы являются ключевыми игроками в клеточной кооперации бронхиального воспалительного иммунного ответа при T2-эндотипе БА. Как при аллергической, так и при неаллергической форме эозинофильного фенотипа астмы уровни эозинофилов в мокроте могут быть повышены и варьируются от 1 до 50%, что также сопровождается эозинофилией тканей и крови [8]. Уровень эозинофилов в индуцированной мокроте ≥2–3% у взрослых пациентов с БА позволяет диагностировать эозинофильную астму (более надежен уровень эозинофилии мокроты ≥3%) [9]. Анализ мокроты, характеризующийся чувствительностью >80% и специфичностью 95%, считается наиболее надежным способом определения эозинофильного воспаления при БА [10]. Однако в ряде случаев получение мокроты крайне затруднительно для больных БА, в связи с этим проводится поиск других потенциальных биомаркеров, характеризующихся достоверно высокой корреляцией с бронхиальной эозинофилией. В качестве одного из таких суррогатных биомаркеров в настоящее время рассматривается уровень эозинофилов периферической крови.
Эозинофилы периферической крови. Определение абсолютного числа эозинофилов в периферической крови может быть использовано в качестве прогностического биомаркера [11]. Рост числа эозинофилов в периферической крови коррелирует со степенью тяжести БА и обратно пропорционален ОФВ1 [12].
Высокие показатели чи...












