Терапия №4 / 2018
Ведение больных ревматоидным артритом: современные рекомендации и реальная клиническая практика
ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова»
В статье представлены рекомендации Европейской антиревматической лиги 2016 г. и национальные рекомендации 2017 г. по ведению больных ревматоидным артритом, приведены результаты лечения больных с ранней стадией заболевания в соответствии с данными рекомендациями. Цель исследования. Оценка эффективности и переносимости подкожной формы метотрексата при проспективном наблюдении больных с ранним ревматоидным артритом. Материал и методы. Подкожная форма метотрексата (15 мг/нед в комбинации с 1–2 мг фолиевой кислоты) была назначена 67 больным с достоверным диагнозом «ревматоидный артрит» по критериям ACR/EULAR 2010 г. В течение 12 мес пролечено 65 больных (97%), 24 мес – 47 больных, 36 мес – 22 пациента. Лечение проводилось в соответствии с принципами стратегии лечения РА «Лечение до достижения цели» (Treat to Target). Исходная активность РА по DAS28 у 43 больных (64%) была умеренной и у 24 (36%) – высокой. Результаты. Практически у всех больных (у 61 из 67 – 91%) первые симптомы улучшения отмечались через 4–5 нед использования метотрексата в дозе 15 мг/нед, к 8 нед терапии эффект отмечался у всех больных. Через 6 мес терапии высокой степени активности ревматоидного артрита не отмечено, умеренная степень активности имела место у 32 из 65 (49%) пациентов, низкая – у 33 (51%). Через 2 года лечения 43% больных достигли ремиссии, у остальных регистрировалась низкая активность РА; через 3 года ремиссия отмечалась у более половины пациентов. Заключение. Подкожная форма метотрексата обладает высокой эффективностью в отношении активности и прогрессирования при раннем ревматоидном артрите, длительной хорошей переносимостью и позволяет при использовании принципов контролируемого лечения, включая обучение больных, достичь цели у большинства пациентов через 6–12 мес терапии. При условии контролируемого лечения со своевременной коррекцией терапии при недостаточном противовоспалительном эффекте, обучении больных можно значительно улучшить результаты лечения ревматоидного артрита, добиться клинико-лабораторной ремиссии более чем у половины пациентов и предупредить деструкцию суставов.
ВВЕДЕНИЕ
Ревматоидный артрит (РА) – одно из самых тяжелых хронических заболеваний человека. Тяжесть заболевания связана со сложным многокомпонентным патогенезом хронического воспаления, развивающегося преимущественно в синовиальной оболочке суставов, что приводит к деструкции хряща суставных поверхностей и субхондральной кости с утратой функции опорно-двигательного аппарата.
 В недавнем прошлом лечение РА при отсутствии современного арсенала лекарственных средств и четкой стратегии терапии не давало возможности стабильного подавления активности и прогрессирования заболевания, что приводило к частой инвалидизации больных в первые 5 лет болезни [1]. На современном этапе результаты лечения РА при грамотном ведении больных позволяют контролировать течение болезни и сохранять работоспособность пациентов. Это стало возможным благодаря нескольким обстоятельствам.
В недавнем прошлом лечение РА при отсутствии современного арсенала лекарственных средств и четкой стратегии терапии не давало возможности стабильного подавления активности и прогрессирования заболевания, что приводило к частой инвалидизации больных в первые 5 лет болезни [1]. На современном этапе результаты лечения РА при грамотном ведении больных позволяют контролировать течение болезни и сохранять работоспособность пациентов. Это стало возможным благодаря нескольким обстоятельствам.
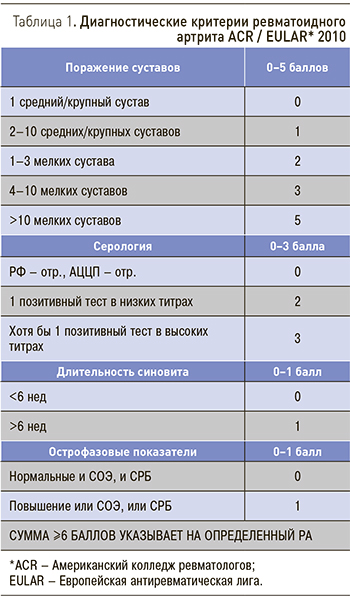
Во-первых, разработаны новые классификационные критерии РА 2010 г. [2], позволяющие устанавливать диагноз на ранних стадиях болезни (табл. 1). Во-вторых, сформулированы принципы стратегии лечения РА «Лечение до достижения цели» (Treat to Target) [3]. Согласно им лечение больных РА должно проводиться при постоянном взаимодействии врача и пациента, основная стратегическая цель лечения РА – максимальное сохранение качества жизни пациента, основной путь к достижению этой цели – подавление воспаления и постоянный контроль за достаточностью терапии. В соответствии со стратегией «Лечение до достижения цели» формулируются и современные международные (рекомендации Европейской антиревматической лиги – EULAR) [4] и национальные [5] рекомендации по ведению больных РА, в которых четко сформулирована тактика этого ведения. Лечение больных РА должно проводиться ревматологами.
В настоящее время для лечения РА используются, с одной стороны, симптоматические (стероидные и нестероидные) противовоспалительные препараты, которые бывают необходимы на ранних этапах проведения терапии, но не способны оказать влияние на течение РА, с другой – синтетические базисные противовоспалительные препараты (БПВП), задача которых надежно подавить воспаление и предотвратить развитие деструкции. В отсутствии достаточного эффекта при их использовании к лечению присоединяют генно-инженерные биологические препараты (ГИБП) или так называемый таргетный БПВП – блокатор янус-киназ тофацитиниб. Высокая стоимость ГИБП лимитирует их применение у всех больных РА, хотя ряд контролируемых исследований и показывает их более высокую эффективность у больных на ранней стадии и не получавших ранее БПВП [6, 7].
Лечение РА с применением синтетических БПВП начинают сразу после установления диагноза, не позднее чем через 3–6 мес от момента появления симптомов поражения суставов (уровень доказательности 1а) [3–5]. В связи с этим каждый врач общей практики должен уметь выделить среди пациентов с болями в суставах больных, у которых имеются признаки хронизации воспаления, и как можно раньше отправить их на консультацию к ревматологу.
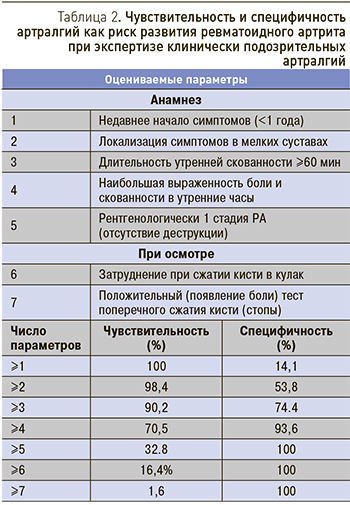
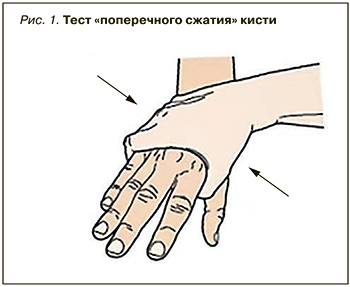 EULAR дано определение артралгий, позволяющих заподозрить развитие РА [8]. Врачу общей практику следует оценить 5 анамнестических параметров (табл. 2), а при осмотре оценить, есть ли затруднения при сжатии кисти в кулак и провести тест поперечного сжатия кисти (или стопы; рис. 1).
EULAR дано определение артралгий, позволяющих заподозрить развитие РА [8]. Врачу общей практику следует оценить 5 анамнестических параметров (табл. 2), а при осмотре оценить, есть ли затруднения при сжатии кисти в кулак и провести тест поперечного сжатия кисти (или стопы; рис. 1).
Как видно из табл. 2, при наличии 4 положительных ответов из 7 риск развития РА уже составляет почти 94%, а при наличии 5–7 положительных ответов он равен 100%, что должно служить основанием для направления больного к ревматологу. При раннем начале лечения (в первые 3–6 мес) у большинства пациентов можно добиться ремиссии или течения РА с низкой активностью, что и является критерием эффективного лечения РА.
Задержка с назначением синтетических БПВП приводит к уменьшению эффекта лечения. Согласно анализу данных 14 рандомизированных клинических исследований (1435 пациентов с РА, из которых 886 получали различные синтетические БПВП и 549 – плацебо) с учетом демографических факторов (пол, возраст), функционального класса по Steinbrocker и клинико-лабораторных параметров активности болезни (боль, число болезненных и припухших суставов, СОЭ, индекс оценки функции HAQ и др.), при любой длительности РА различие в частоте развития терапевтического эффекта между активным лечением и плацебо было примерно одинаковым – около 30% [9]. Однако по мере увеличения длительности РА эффективность синтетических БПВП снижалась с 52% «ответчиков» (в случае начала терапии при длительности РА 10 лет).
 Якорным препаратом в лечении РА считается метотрексат (МТ), который эффективен у большинст...
Якорным препаратом в лечении РА считается метотрексат (МТ), который эффективен у большинст...












