Клиническая Нефрология №3 / 2014
Возможности ранней диагностики нарушений нутритивного статуса у больных хронической болезнью почек на додиализных стадиях и регулярном гемодиализе
ГБОУ ВПО «Первый МГМУ им. И.М. Сеченова» Минздрава России, Москва
Цель. Определение диагностических возможностей традиционной антропометрии и биоэлектрического импедансного анализа для ранней диагностики нарушений нутритивного статуса у больных хронической болезнью почек (ХБП).
Материал и методы. В исследование включены 180 пациентов с ХБП, из них 80 – с ХБП III–IV стадий, 100 – с ХБП V стадии, из них 61 мужчина и 119 женщин; возраст – от 21 до 80 (в среднем 46,7 ± 10,8) лет. Наряду со стандартной антропометрией состав тела определяли с помощью биоэлектрического импедансного анализа.
Результаты. Соотношение тощей и жировой массы тела у больных ХБП с большей точностью можно определить с помощью биоэлектрического импедансного анализа. Более выраженные нарушения нутритивного статуса при ХБП ассоциированы в т.ч. с расчетной скоростью клубочковой фильтрации < 30 мл/мин/1,73 м2, анемией, гипальбуминемией, а также депрессией и непереносимостью определенных пищевых продуктов. Нарушения нутритивного статуса при ХБП корригируются малобелковой диетой с применением кетоаналогов аминокислот.
Заключение. Биоэлектрический импедансный анализ позволяет диагностировать у пациентов с ХБП нарушения нутритивного статуса.
Введение
Одной из актуальных проблем нефрологии является улучшение качества жизни и общей выживаемости больных хронической болезнью почек (ХБП), распространенность которой в мире неуклонно возрастает [1–4].
Несмотря на то что внедрение методов заместительной почечной терапии способствовало увеличению продолжительности жизни больных ХБП, появился ряд новых проблем, в т.ч. связанных с частотой нарушений нутритивного статуса (синоним белково-энергетической недостаточности – БЭН), особенно у больных на регулярном гемодиализе (ГД). Нарушения нутритивного статуса имеют важное прогностическое значение, поскольку оказывают значительное влияние на выживаемость и уровень реабилитации этих групп больных [3, 5–7]. Отмечено, что смертность больных в течение первого года диализной терапии составила 15 % среди больных с нормальным индексом массы тела – интегральным показателем оценки нутритивного статуса, и 39 % среди больных, у которых индекс массы тела менее 19 кг/м2 [2, 4, 8].
В настоящее время неинвазивными методами оценки степени нарушений нутритивного статуса, в т.ч. и у больных с наличием отеков, являются антропометрия и биоэлектрический импедансный анализ [2, 6]. Однако отсутствуют работы, в которых бы с помощью антропометрии и биоэлектрического импедансного анализа проводилась сравнительная оценка состояния нутритивного статуса у больных ХБП на додиализных стадиях ХБП и во время лечения регулярным ГД, а также изучение факторов риска развития нутритивных нарушений у этих больных.
В небольших по численности исследованиях показано, что ограничение суточной квоты белка в еде до 0,6 г/кг/сут предупреждает накопление токсических продуктов, уменьшает или отдаляет появление уремической диспепсии [9–15]. Вместе с тем результаты нескольких многоцентровых исследований, включивших множество пациентов, в т.ч. широко известного исследования MDRD (Modification of Diet in Renal Disease), не дают столь однозначного вывода [16–18]. Различие результатов объясняют сложностями в организации МБД (0,6 г/кг/сут), особенно массовой, и одновременно в обеспечении достаточной калорийности пищи (не менее 35 ккал/кг/сут) [19]. Насколько МБД может вызывать или усугублять нарушения питания, свойственные больным ХБП, остается предметом продолжающейся дискуссии в литературе. По мнению большинства авторов, состояние нутритивного статуса – один из главных факторов, определяющих выживаемость и степень реабилитации больных ХБП, находящихся на заместительной почечной терапии, а также эффективность диализного лечения [2, 3, 5].
Целью нашего исследования являлось определение диагностических возможностей традиционной антропометрии и биоэлектрического импедансного анализа для ранней диагностики нарушений нутритивного статуса у больных ХБП на додиализных стадиях и регулярном ГД, а также выявление наиболее значимых факторов их развития.
Материал и методы
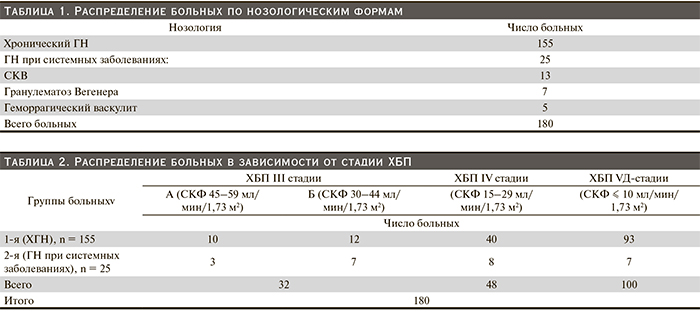
В исследование включены только 180 больных ГН, среди них 155 – хроническим ГН и 25 – ГН при системных заболеваниях: 13 системной красной волчанкой (СКВ) и 12 разными формами системного васкулита (табл. 1).
Среди 180 больных, включенных в исследование, у 80 диагностирована ХБП III–IV стадий (ХПН начальной и умеренной степени) и у 100 больных – ХБП VД стадии (ХПН тяжелая – диализная – стадия).
В зависимости от этиологии и стадии ХБП все больные, вошедшие в исследование, были рандомизированы в 2 группы (табл. 2).
Первую группу составили 155 больных хроническим ГН, среди них 22 с ХБП III стадии (СКФ – 30–59 мл/мин/ 1,73 м2), 40 – с ХБП IV стадии (СКФ – 15–29 мл/мин/ 1,73 м2) и 93 VД стадии (СКФ ≤ 10 мл/мин/ 1,73 м2). В группу 2 включены 25 больных системными заболеваниями: 10 больных III стадией ХБП, 8 – IV стадией ХБП и 7 – VД-стадией. Для более точной оценки роли степени почечной недостаточности в развитии нутритивных нарушений больные III стадии обеих групп были разделены на 2 подгруппы: в подгруппу IIIА включили больных с СКФ 45–59 мл/мин/1,73 м2, а в IIIБ – больных с СКФ 30–44 мл/мин/1,73 м2 (табл. 2).
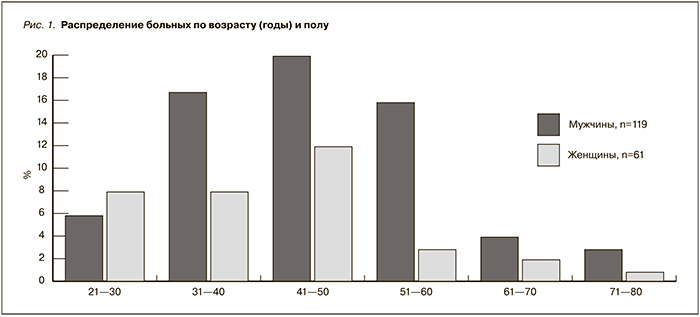
Возраст больных колебался от 21 до 80 (46,7 ± 10,8) лет, женщин было 61, мужчин – 119 (рис. 1). Продолжительность ХБП от начала нарушения функции почек составила 3,5–7,1 (5,2 ± 1,3) года
Диагноз ГН устанавливали по клинической картине, у 2/3 больных диагноз подтвержден морфологически при прижизненной биопсии почки.
У всех больных, вошедших в 1-ю группу, ГН был вне обострения. У 120 больных снижение СКФ и повышение уровня креатинина сочеталось с уменьшением размеров почек разной степени (сморщивание).

Системные заболевания диагностировали по критериям, принятым для каждой нозологической формы.
У больных этой группы наблюдалось рецидивирующее течение нефрита, у части больных (10 ...












