Клиническая Нефрология №1 / 2026
Фазовый угол как ранний маркер формирования саркопении
1) ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава РФ (Пироговский Университет), Москва, Россия;
2) Научно-исследовательский институт организации здравоохранения и медицинского менеджмента ДЗМ, Москва, Россия
Введение
Для пациентов с хронической сердечной недостаточностью (ХСН) саркопения имеет особую актуальность: хроническое воспаление, нейрогуморальная активация, снижение перфузии скелетных мышц, физическая декондиция и нутритивные нарушения формируют «порочный круг» снижения мышечной функции и толерантности к нагрузке [1].
По данным систематических обзоров и мета-анализов, саркопения у больных ХСН встречается часто (порядка трети пациентов, с широким разбросом в зависимости от критериев и контингента) и связана с худшими клиническими характеристиками [2, 3]. Хроническая болезнь почек (ХБП) также относится к состояниям с высоким риском саркопении: уремическая интоксикация, метаболический ацидоз, инсулинорезистентность, воспаление и снижение физической активности ускоряют потерю мышечной ткани и ее функционального потенциала [4]. Глобальные данные указывают на значимую распространенность нарушений мышечного статуса при ХБП, особенно у пациентов на диализе, а саркопения рассматривается как фактор неблагоприятных исходов и меньшей переносимости терапии [5]. На практике раннее выявление формирования саркопении у пациентов с сочетанием ХСН и ХБП затруднено: «эталонные» методы оценки состава тела (КТ – компьютерная томография/МРТ – магнитно-резонансная томография, DXA – Dual-energy X-ray Absorptiometry) ограничены доступностью, стоимостью и организационными барьерами, тогда как рутинные клинические маркеры нередко неспецифичны и зависят от гидратационного статуса [6, 7]. В связи с этим растет интерес к биоимпедансному анализу (BIA) и его параметрам, прежде всего, фазовому углу (ФУ), рассчитываемому из соотношения реактивного и активного сопротивления тканей. ФУ рассматривается как интегральный показатель, отражающий особенности распределения жидкости, клеточной массы и функционального состояния клеточных мембран, и потому потенциально может быть чувствительным ранним маркером ухудшения «мышечного качества» [8].
Цель: изучить взаимосвязь ФУ с показателями саркопении у пациентов с ХСН и ХБП.
Материал и методы
Исследование было выполнено на базе Городской клинической больницы №4 ДЗМ в период с сентября 2019 по декабрь 2021 г. В исследование были включены 144 пациента с ХСН и ХБП, из которых у 46 (32%) признаков саркопении не выявлено (группа 1), у 62 (43%) диагностирована пресаркопения (группа 2), и у 36 (25%) – сформированная саркопения (группа 3). В общей выборке средний возраст составил 68,04±9,72 года и статистически значимо не различался между группами (p>0,9). Женщины преобладали (84/144; 58%), при этом отмечалась тенденция к различиям распределения по полу между группами (p=0,059): доля женщин была выше в группе 2 (69%) по сравнению с группой 1 (48%) и группой 3 (53%). Диагноз саркопении верифицировался в соответствии с критериями Европейской рабочей группы по саркопении у пожилых людей, пересмотр 2 (EWGSOP2) [1]. Критерии включения и исключения пациентов приведены в табл. 1.
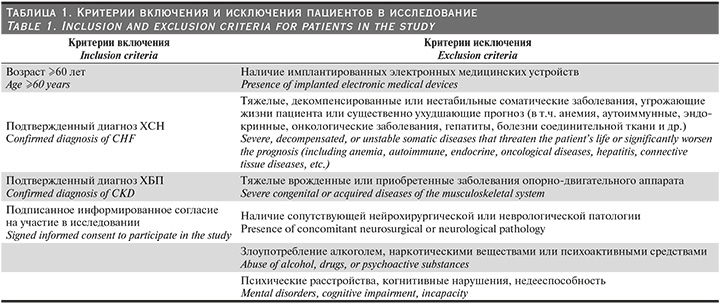
Все пациенты проходили комплексное клинико-лабораторное обследование, включавшее сбор анамнеза, физикальное исследование, инструментальные методы диагностики.
Масса скелетной мускулатуры определялась методом биоимпедансного анализа с использованием анализатора ABC-02 («Медасс», Россия) по стандартной методике, с подсчетом ФУ. Сила кистевого сжатия оценивалась при помощи ручного динамометра DK-25 с регистрацией максимального значения из трех попыток для каждой руки. Физическую работоспособность определяли с использова...












