Урология №2 (supplement) / 2017
Адъювантная антиоксидантная терапия у больных бесплодием при варикоцеле
1 Отделение андрологии и урологии ФГБУ «Научный центр акушерства, гинекологии и перинатологии им. академика
В. И. Кулакова» Минздрава России, Москва, Россия; 2 кафедра акушерства, гинекологии, перинатологии
и репродуктологии института профессионального образования ФГБОУ ВО «Первый Московский государственный медицинский университет им. И. М. Сеченова» Минздрава России, Москва, Россия; 3 кафедра акушерства, гинекологии, неонатологии, анестезиологии и реаниматологии ФГБУ «Научный центр акушерства, гинекологии и перинатологии
им. академика В. И. Кулакова» Минздрава России, Москва, Россия; 4 урологическое отделение ГБУ ГП № 180 Департамента здравоохранения г. Москвы, Россия; 5 ФГБУ «Научный центр акушерства, гинекологии и перинатологии им. академика В. И. Кулакова» Минздрава России, Москва, Россия
Введение. Распространенность бесплодия в паре составляет около 15%. Мужской фактор имеет место примерно в половине случаев. Около 40% мужчин с бесплодием имеет варикоцеле. Целью настоящего исследования было изучить эффективность и безопасность адъювантной антиоксидантной терапии после микрохирургической варикоцелэктомии (МВЭ) комплексом ацетил-L-карнитина, L-карнитина фумарата и α-липоевой кислоты (СпермАктин-форте®) (СА), оценить его влияние на уровень фрагментации ДНК сперматозоидов.
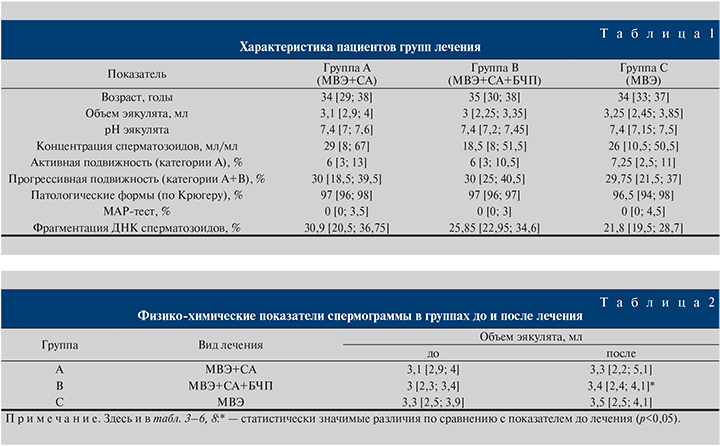
Материалы и методы. В открытом проспективном рандомизированном исследовании участвовали 114 мужчин после МВЭ в возрасте 25–45 лет: (средний возраст 34,1±12,1 года). Тридцать восемь мужчин адъювантно получали СА; 38 – СА в комбинации с витаминным комплексом (БЧП); 38 пациентов никакой адъювантной терапии не получали. Критериями оценки эффективности через 3 мес. являлись показатели спермограммы, уровень фрагментации ДНК сперматозоидов.
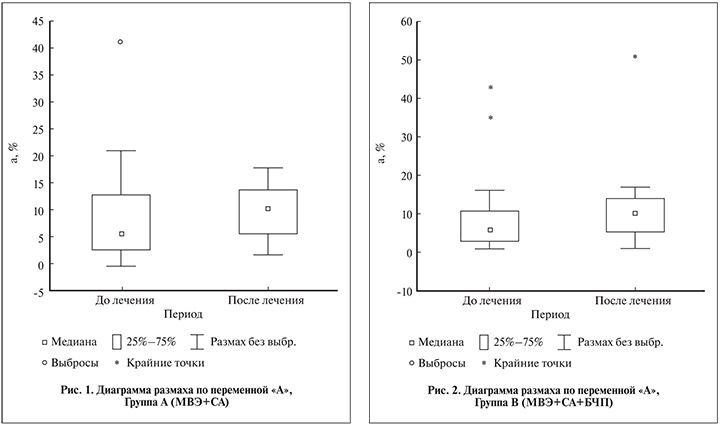
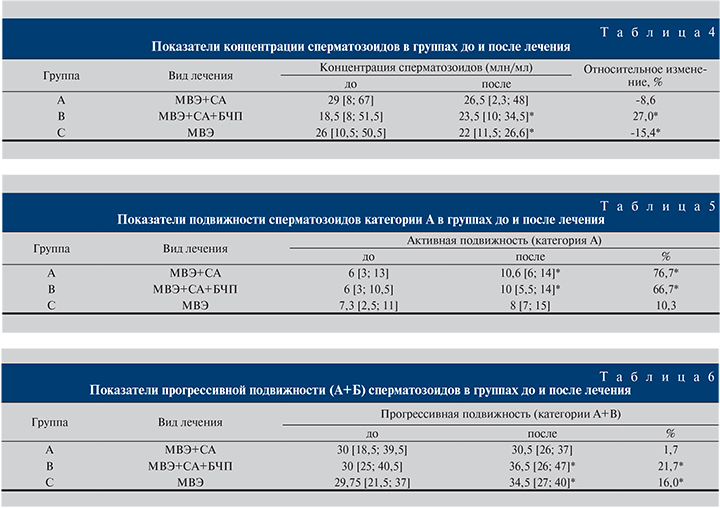
Результаты. Прогрессивная подвижность сперматозоидов возрастала после МВЭ на 21,7% от исходного уровня, причем на фоне приема СА это происходило за счет активной подвижности сперматозоидов (категории А) – на 76,7% к 3-му месяцу лечения. Назначение СА после МВЭ способствовало снижению уровня фрагментации ДНК сперматозоидов уже через 3 мес. лечения на 22,3%. При применении в послеоперационном периоде после МВЭ СА и БЧП концентрация сперматозоидов через 3 мес. возрастала на 27%. Побочных эффектов фармакотерапии зафиксировано не было. Статистическую значимость динамики показателей оценивали с помощью критерия Вилкоксона. Для всех критериев установлен критический уровень α=0,05.
Заключение. Назначение нутрицевтиков (СА) после МВЭ и является эффективным и безопасным методом адъювантной антиоксидантной терапии мужского бесплодия у больных варикоцеле, что приводит к улучшению основных показателей спермограммы (концентрации, подвижности сперматозоидов) и снижению уровня фрагментации ДНК сперматозоидов в ранние сроки. Адъювантная антиоксидантная терапия мужского бесплодия при варикоцеле потенцирует эффекты монотерапии (как консервативной, так и хирургической) и приводит к увеличению ее результативности и сокращению сроков наступления беременности. Требуется продолжение исследования в этой области для оценки отдаленных результатов лечения.
Введение. Термины «адъювантная и неоадъювантная терапия» (гормональная, лучевая, химиотерапия и пр.) в современной урологии используются в основном при обсуждении различных вариантов лечения онкологических заболеваний. В то же время адъювантная терапия – это вспомогательное, дополняющее радикальные методы лекарственное лечение. Употребление понятия «адъювантная терапия» применимо не только в онкологии, но и в любых других областях медицины при обозначении дополнительного (т.е. в составе комплексного) лечения.
Проблема бесплодия у мужчин с варикоцеле уже более 100 лет актуальна, и до сих пор нет единого общепризнанного мнения о путях ее решения. До сих пор не утихают споры между специалистами во всем мире, как правильно поступать, если мужчина с бесплодием страдает варикоцеле.
В настоящее время бесплодный брак – важная медико-социальная и демографическая проблема. Доля бесплодных пар составляет около 15%. При этом установлено, что мужской фактор имеет место в половине случаев [1, 2].
Известно, что оплодотворяющая способность сперматозоидов зависит от секреторной активности вспомогательных половых желез: придатков яичек, простаты и семенных пузырьков. Наиболее важным биохимическим маркером нормального созревания сперматозоидов является L-карнитин, продуцируемый придатком яичка [3].

Физиологическая роль придатка яичка заключается в создании условий для нормального развития сперматозоидов путем секреции ряда соединений, в том числе L-карнитина, участвующего в переносе ацил-группы и окислительного фосфорилирования жирных кислот в митохондриях и как следствие – в обеспечении энергией, используемой сперматозоидами для созревания и приобретения ими подвижности. Кроме того, установлено, что L-карнитин и ацетил-L-карнитин обладают антиоксидантной активностью за счет удаления токсичного внутриклеточного ацетил-кофермента А и стабилизации клеточной мембраны сперматозоидов под действием активных форм кислорода, гиперпродукция которых является важным патогенетическим фактором патоспермии у мужчин. Следует отметить, что существует прямая корреляция между концентрацией в сперме карнитина, с одной стороны, и количеством, общей и прогрессивной подвижностью, способностью сперматозоидов проникать в цервикальную слизь, с другой.
Появляется все больше доказательств того, что от пагубных эффектов свободных радикалов сперматозоиды защищают мощные антиоксиданты, содержащиеся в семенной плазме. Защитные способности семенной плазмы имеют значительные индивидуальные колебания. Оксидативный стресс (ОС), характеризующийся массивным образованием свободных радикалов, существенно ухудшает сперматогенез и функцию спермы, что может приводить к бесплодию [4, 5]. Кроме того, ОС может стать причиной нарушения денатурации ДНК в одноцепочечной ДНК и двунитевых разрывов ДНК [6].
Фрагментация ДНК сперматозоидов — нарушение целостности ДНК сперматозоидов, связанное с упаковкой патологического хроматина или дефицита протамина, негативно влияет на репродуктивные исходы при естественном зачатии или в программах ВРТ. У бесплодных мужчин доля сперматозоидов с нарушением целостности ДНК составляет более 30%, при этом у здоровых фертильных мужчин она не превышает 15%. При фрагментации ДНК сперматозоидов более 30% вероятность наступления берем...












