Фарматека №3 / 2023
Амиодарон-индуцированный тиреотоксикоз: современный взгляд на проблему
Военно-медицинская академия им. С.М. Кирова, Санкт-Петербург, Россия
В обзорной статье рассматриваются основные проблемные вопросы эпидемиологии, этиологии, патогенеза амиодарон-индуцированного тиреотоксикоза (АмИТ). Подробным образом описывается влияние йода на щитовидную железу (ЩЖ). Особое внимание уделяется патогенетическим аспектам развития данного вида тиреотоксикоза. Обсуждаются вопросы «типоспецифичности» дисфункции ЩЖ, вызванной приемом амиодарона. Рассматриваются сложные вопросы дифференциальной диагностики 1-го и 2-го типов АмИТ. Обсуждается проблема выявления т.н. смешанного типа. Сравниваются различные инновационные подходы к терапии, включая средства первой линии с учетом или без учета патогенетического типа АмИТ. Уточняются показания к радикальному лечению данного вида тиреоткосикоза. Обсуждаются вопросы отмены и повторного назначения амиодарона и алгоритма действий при возникновении данного вида тиреопатий.
Введение
Несмотря на развитие и эффективность интервенционной аритмологии отказ от применения лекарственных антиаритмических средств не может быть реализован в полном объеме [1]. В cовременной клинической практике целесообразным представляется назначение только тех антиаритмических препаратов, которые подтвердили свою безопасность и эффективность в хорошо организованных рандомизированных доказательных исследованиях. Вместе с тем не всегда представляется возможным в конкретной клинической ситуации оценить безопасность планируемой антиаритмической терапии для данного пациента [1].
Одним из антиаритмиков, вызывающих у эндокринологов наиболее противоречивые чувства, является препарат III класса по классификации антиаритмических средств Вогана–Вильямса амиодарон.
Амиодарон – производное бензофурана, по своему химическому строению сходный с молекулой тироксина [2, 3].
Патологическое воздействие препарата на тиреоциты имеет несколько причин. Одна из них заключается в том, что в 200 мг препарата содержится 75 мг (75 тыс. мкг) йода. Это составляет 50000% от суточной потребности в йоде взрослого человека. Даже при условии, что из 200 мг амиодарона усваивается только 6 мг (600 мкг), это составляет «всего» 400% от суточной потребности в йоде [4]. При пероральном приеме процесс выведения амиодарона носит двухфазный характер. В момент первой фазы препарат выводится за 4–21 час. Время выведения во 2-й фазе растягивается до 25–110 дней. Амиодарон метаболизируется в печени, превращаясь в активный метаболит дезэтиламиодарон, который вместе с амиодароном накапливается в тканях [4]. Когда прием амиодарона прекращен, последующее выведение препарата из организма может достигать нескольких месяцев [4]. К отягчающим факторам, еще более затрудняющим выведение препарата из организма, относятся ожирение (уменьшение выведения на 22%) и пожилой возраст (соответственно на 46%) [5].
Согласно клиническим рекомендациям Российского кардиологического общества, применение амиодарона при различных формах нарушения ритма обоснованно и в некоторых клинических ситуациях высокоэффективно. Вместе с тем, согласно инструкции к препарату, амиодарон абсолютно противопоказан при гипо- и гипертиреозе [4], наличие которых у пациента невозможно достоверно выявить в экстренном случае за ограниченное время. Перед началом терапии амиодароном необходимо определить исходный уровень тиреотропного гормона (ТТГ), антитиреоидные антитела и провести ультразвуковое исследование (УЗИ).
К сожалению, применение амиодарона обычно является решением в неотложной клинической ситуации, когда нет возможности выполнить исследование состояния щитовидной железы (ЩЖ). Таким пациентам следует его провести сразу после введения амиодарона при первой возможности [6].
В результате, несмотря на побочные эффекты, амиодарон все-таки остается одним из наиболее эффективных антиаритмических средств и широко применяется в клинической практике [6–9].
Влияние амиодарона на функционирование ЩЖ
Большинство пациентов, начавших терапию амиодароном, остаются в эутиреоидном состоянии, даже если используются высокие дозы препарата (400 мг в сутки) [10], частота возникновения амиодарон-индуцированного тиреотоксикоза (АмИТ), по разным статистическим данным, варьируется от 1 до 23% [11–13].
Тиреотоксикоз, вызванный применением амиодарона, разделяют на 3 типа: 1-й тип обусловлен повышенной продукцией гормонов ЩЖ, при 2-м типе тиреотоксикоз носит деструктивный характер (т.е. возникает вследствие разрушения ткани ЩЖ с выходом ее гормонов в кровь). Также выделяют наиболее сложный промежуточный тип: смешанный [2, 14].
При назначении амиодарона многие врачи хотят быть уверенными в преобладании пользы над риском.
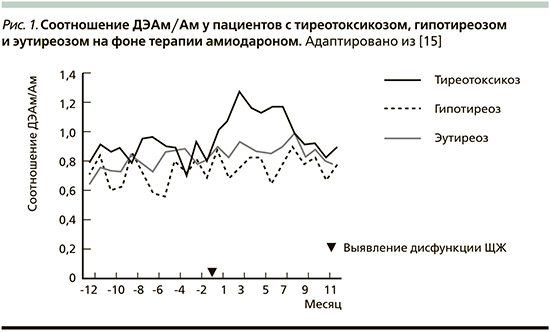
В различных рекомендациях обсуждаются предикторы развития дисфункции ЩЖ после старта терапии амиодароном. Так, определение соотношения концентрации активного метаболита амиодарона к его содержанию в крови (ДЭАм/Ам) может быть тем параметром, который позволит прогнозировать развитие АмИТ: при развитии данного состояния это соотношение повышается [2, 15].
Эти данные подтверждаются японским ретроспективным исследованием, в котором приняли участие 377 человек. Пациентам, получавшим амиодарон с января 2012 по апрель 2016 г., проводилось исследование тиреоидного статуса, определение концентрации амиодарона, дезэтиламиодарона и ДЭАм/Ам. Среди участников этого исследования частота АмИТ и гипотиреоза составила 14,3 и 15,9% соответственно. В результате повышение соотношения ДЭАм/Ам даже до начала возникновения АмИТ было обнаружено у 54 больных с выявленным в последующем тиреотоксикозом.
И при определении тиреотоксикоза эта концентрация значительно возросла (рис. 1) [15].
По данным других исследователей специфических предикторов возникновения дисфункции ЩЖ, связанной с приемом амиодарона, выявить не удалось [16, 17...












