Фарматека №3 (356) / 2018
«Амиодароновое» легкое: обзор литературы и собственные наблюдения
Кафедра клинической аллергологии и пульмонологии Иркутской государственной медицинской академии последипломного образования (ИГМАПО) – филиал РМАНПО Минздрава РФ, Иркутск, Россия
До настоящего времени амиодарон – широко используемый во всем мире антиаритмический препарат, что обусловлено его терапевтической эффективностью. Вместе с тем относительно высокая частота побочных эффектов затрудняет безопасное использование этого препарата в клинической практике. Пневмотоксичность с прогностической точки зрения является самым серьезным побочным эффектом терапии амиодароном. «Амиодароновая» пневмопатия относится к дозозависимому варианту и развивается в среднем через 18–24 месяца терапии. Наиболее частым вариантом считается интерстициальное поражение легких. Клинико-рентгенологическая картина неспецифична и требует тщательного анализа лекарственного анамнеза. «Амио- дароновая» пневмопатия – диагноз, требующий исключения инфекционных поражений легочной ткани и других возможных причин интерстициального заболевания легких (ИЗЛ). С целью ранней диагностики ИЗЛ у больных, получающих амиодарон, компьютерная томография должна быть выполнена до назначения препарата и регулярно проводиться каждые 6–12 месяцев. В случае развития «амиодаронового» легкого амиодарон должен быть отменен и назначена терапия преднизолоном. При ранней диагностике амиодарон-индуцированного поражения легких и своевременном терапевтическом вмешательстве в большинстве случаев прогноз благоприятный. Обзор литературы дополнен тремя собственными наблюдениями запоздалой диагностики «амиодаронового» легкого.
Лекарственно-индуцированные интерстициальные поражения легких (ЛИИПЛ) являются одной из наиболее частых форм лекарственных пневмопатий и составляют около 3% в структуре всех интерстициальных заболеваний легких (ИЗЛ) [1, 2]. Среди лекарственных средств амиодарон – один из самых частых причиннозначимых препаратов, ассоциированных с развитием ЛИИПЛ [1, 3].
Амиодарон был синтезирован и внедрен в клиническую практику в 1960-е гг. первоначально как антиангинальное средство, позже был обнаружен его антиаритмический потенциал. До настоящего времени амиодарон является широко используемым антиаритмическим препаратом во всем мире в силу его высокой эффективности в лечении суправентрикулярных и желудочковых аритмий по сравнению с другими антиаритмическими средствами [4]. Кроме того, амиодарон обладает крайне низкой отрицательной инотропной активностью и минимальным проаритмогенным желудочковым эффектом, что обусловливает его преимущество при использовании пациентами с сердечной недостаточностью [5]. Вместе с тем почти 50-летняя история применения амиодарона сопровождается относительно высокой частотой побочных эффектов и затрудняет безопасное использование этого препарата в клинической практике.
В основе амиодарон-индуцированного поражения легких (АИПЛ) лежат механизмы прямого токсического действия препарата на пневмоциты либо гиперчувствительность, опосредованная иммунологическими реакциями [1, 6]. Прямая токсичность амиодарона обусловлена его выраженной липофильностью и нарушением нормального метаболизма эндогенных фосфолипидов, которые на фоне длительного приема амиодарона накапливаются в различных органах-мишенях: легких, глазах, щитовидной железе, печени, коже, нервной системе [7]. Побочные эффекты амиодарона составляют около 15% в течение первого года примене-ния и могут увеличиваться до 50% при более длительном его приеме [5]. С прогностической точки зрения пневмотоксичность – самый серьезный побочный эффект терапии амиодароном [1, 8].
Патогенетическим синонимом АИПЛ является термин «фосфолипидоз легких», что обусловлено способностью метаболитов амиодарона связывать липиды лизосом альвеолярных макрофагов, вызывать нарушение катаболизма фосфолипидов, которые откладываются в виде пластинчатых телец в альвеолах, приводя к замедлению диффузии газов через альвеолярную мембрану. Исследования последних лет доказывают возможность развития фиброза при «амиодароновом» легком [1, 3, 9].
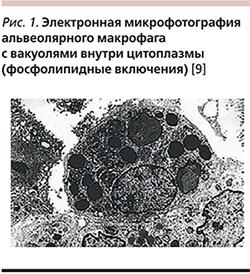 Характерным признаком АИПЛ слжит обнаружение пенистых альвеолярных макрофагов, содержащих два типа аномальных вакуолей, выявляемых при электронной микроскопии: маленькие пустые вакуоли и пластинчатые включения, представляющие собой крупные фаголизосомы, содержащие фосфолипиды – амиодаронфосфолипидный комплекс (рис. 1).
Характерным признаком АИПЛ слжит обнаружение пенистых альвеолярных макрофагов, содержащих два типа аномальных вакуолей, выявляемых при электронной микроскопии: маленькие пустые вакуоли и пластинчатые включения, представляющие собой крупные фаголизосомы, содержащие фосфолипиды – амиодаронфосфолипидный комплекс (рис. 1).
К особенностям фармакокинетики амиодарона можно отнести характерный для него профиль легочной токсичности, что во многом связано с очень длительным периодом полувыведения – в течение 6–12 месяцев. Поэтому для АИПЛ в большинстве случаев типично медленное начало, вялотекущее улучшение после отмены препарата, возможное развитие или рецидив симптомов после прекращения приема [1, 9, 10].
К факторам риска амиодароновой пневмотоксичности наиболее часто относят высокую кумулятивную дозу препарата, суточную дозу ≥200 мг, продолжительность терапии свыше 2 месяцев, пожилой возраст пациента, мужской пол, патологию легких, оксигенотерапию, любое серьезное хирургическое вмешательство и легочную ангиографию [11, 12]. Кроме того, амиодарон – это мощный ингибитор системы цитохрома, что следует учитывать при анализе лекарственных взаимодействий.
Хотя острое повреждение легких при приеме амиодарона в целом встречается редко, тем не менее оно может развиться через несколько дней после внутривенного введения высоких доз препарата. Случаи острого АИПЛ описаны после оперативных вмешательств на сердце или легких. Наркоз, оксигенотерапия и механическая вентиляция служат дополнительным фактором риска острого АИПЛ [1, 8, 9]. Оно манифестирует одышкой, тяжелой гипоксемией, картиной острого респираторного дистресс-синдрома (ОРДС), диффузными альвеолярными и интерстициальными затемнениями, выявляемыми при лучевой диагностике.
Хроническая форма «амиодаронового» легкого развивается примерно у 0,1% пациентов, получающих низкие дозы, и значительно чаще (до 50%) у больных, длительно использующих высокие дозы препарата [10].
Таким образом, АИПЛ относится к...












