Трудный диагноз в педиатрии №5 / 2017
Бронхиальная астма у ребенка с целиакией
Бронхиальная астма встречается в педиатрической практике достаточно часто. Четкие критерии диагноза и подходы к лечению четко определены в международных руководящих документах (GINA). Прошло 20 лет со времени появления приоритетного профессионального документа для педиатров, детских аллергологов и пульмонологов – первой Национальной программы «Бронхиальная астма у детей. Стратегия лечения и профилактика» (1997), ставшей основой для последующих четырех переизданий. В то же время установление диагноза, как и дальнейшее ведение больных бронхиальной астмой, иногда далеки от современных рекомендаций. Причинами этого обычно являются гиподиагностика заболевания, стероидофобия, недостаточная комплаентность в системе «врач–родители–ребенок», объективные сложности в работе детьми-астматиками раннего возраста, недооценка возможной гетерогенности астмы [1, 2]. Наличие у ребенка повторяющихся симптомов бронхиальной обструкции может осложнить диагностический поиск и в случае нередкого сочетания бронхиальнойастмысдругимзаболеванием. Приведенное ниже клиническое наблюдение ребенка с разнообразной коморбидной патологией, включающей поздно диагностированные целиакию и бронхиальную астму, демонстрирует особенности течения двух заболеваний у одного ребенка.
Согласно определению Европейского общества педиатрической гастроэнтерологии, гепатологии и нутрициологии ESPGHAN (European Society for Pediatric Gastroenterology, Hepatology and Nutritition, 2012), целиакия – это иммуноопосредованное системное заболевание, которое возникает в ответ на употребление глютена или соответствующих проламинов генетически предрасположенными индивидуумами и характеризуется наличием широкой комбинации глютен-зависимых клинических проявлений, специфических антител (к тканевой трансглутаминазе TG2, эндомизию, деамидированным пептидам), HLA-DQ2 или HLA-DQ8 гаплотипов и энтеропатии. Стойкая непереносимость специфических белков эндосперма зерна злаковых культур приводит к развитию атрофической энтеропатии и связанному с ней синдрому мальабсорбции [3].
Результаты масштабных зарубежных эпидемиологических исследований свидетельствуют, что на рубеже XX в. частота заболевания достигает 1% (1:100), но число мало симптомных и скрытых форм выше почти в 10 раз. Предполагаемая частота целиакии в России может составлять 1:100–1:250 [4]. Учитывая, что бронхиальной астмой страдает около 5–10% населения, можно предположить, что вероятность сочетания этих двух заболеваний у одного больного достаточно высока.
Диагноз типичной целиакии обычно не вызывает значительных затруднений. Первые проявления заболевания появляются уже на первом году жизни ребенка после введения глютенсодержащих продуктов: стеаторея, зловонный стул в большом количестве, метеоризм, увеличение живота, нарушение аппетита, потеря в весе, задержка нервнопсихического развития, негативизм.
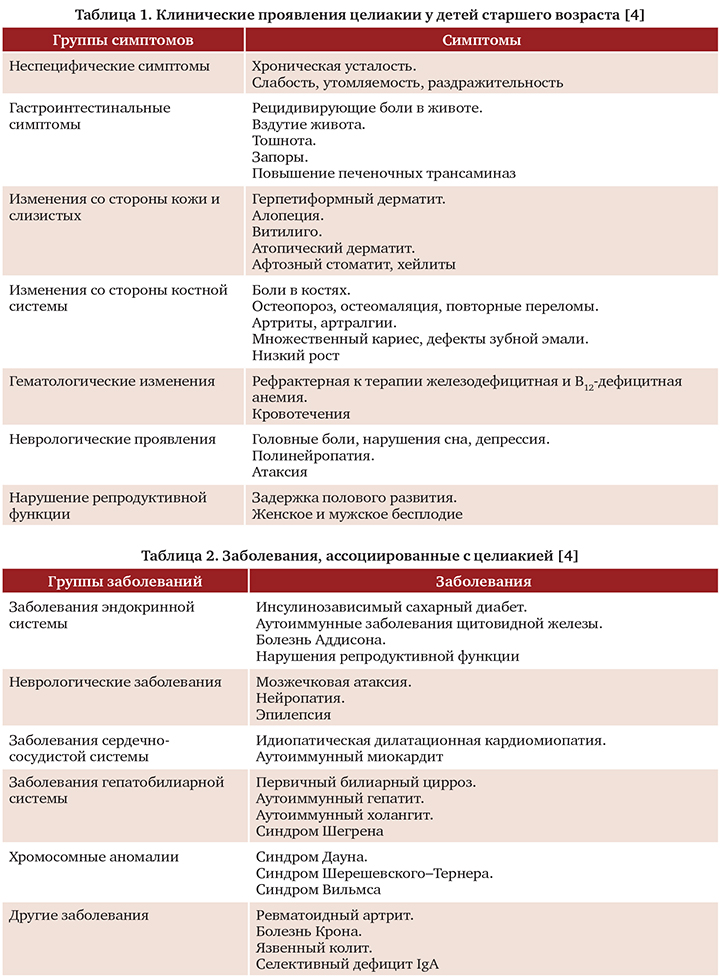
У детей старшего возраста клиническая картина изменяется (табл. 1), доминируют внекишечные проявления.
Внекишечные проявления целиакии важно отличать от заболеваний, ассоциированных с целиакией, которые касаются тех же систем организма (табл. 2).
Из представленных данных можно видеть, что, несмотря на разнообразие как внекишечных проявлений целиакии, так и ассоциированных с ней заболеваний, нарушения со стороны легких для нее не характерны. Более того, с точки зрения иммунопатогенеза сочетание целиакии и бронхиальной астмы представляется необычным, поскольку за развитие астмы и целиакии ответственны разные субпопуляции CD 4+ клеток Т-хелперов (Th), отличающихся секретируемыми цитокинами и активируемыми в результате этого клетками. Так, главными цитокинами Th1 являются провоспалительные цитокины: интерферон γ (INF-γ), интерлейкин-2 (IL-2). Главными цитокинами Th2 являются IL-3, -4, -5, -6. В настоящее время к заболеваниям, ассоциированным с Th1девиацией, относятся ревматоидный артрит, целиакия, сахарный диабет 1 типа, болезнь Крона, в то время как бронхиальная астма и другие атопические заболевания связаны с превалированием Th2 [5, 6].
При наличии легочных проявлений у больного с синдромом нарушенного кишечного всасывания в первую очередь следует думать о муковисцидозе. В очень редких случаях муковисцидоз может сочетаться с целиакией, но обычно требуется проведение дифференциальной диагностики между двумя заболеваниями, поскольку подходы к лечению будут принципиально различаться [7]. Взаимосвязи между целиакией и развитием аллергических заболеваний российские врачи традиционно придают большее значение, чем их зарубежные коллеги. Несмотря на общность некоторых элементов патогенеза и клинической симптоматики, целиакия и аллергическая энтеропатия – это два...












