Фарматека №8 (361) / 2018
Бронходилататоры в лечении хронической обструктивной болезни легких
Российская медицинская академия непрерывного профессионального образования, Москва, Россия
В представленном литературном обзоре рассмотрены исторические аспекты применения бронходилататоров (β2-адреноагонисты и холиноблокаторы) в терапии хронической обструктивной болезни легких (ХОБЛ). Обсуждаются механизмы действия β2-адреноагонистов и холиноблокаторов различных поколений, в т.ч. препаратов длительного действия (ДДБА и ДДХБ), возможности применения которых в последние годы существенно расширились. По мнению экспертов программы GOLD, фиксированные комбинации ДДБА/ДДХБ следует рассматривать как препараты «первой линии» для большинства больных симптоматическим течением ХОБЛ и практически для каждого, кто нуждается в регулярной поддерживающей терапии. Большие надежды связывают с внедрением в практику фармакотерапии ХОБЛ тройных фиксированных комбинаций (ДДБА, ДДХБ и ингаляционные глюкокортикоиды). Очевидно, накопление в ближайшей и среднесрочной перспективе данных из реальной клинической практики, дополненных результатами бóльшего числа прямых сравнительных исследований, облегчат врачу выбор «правильного препарата» для «правильного пациента» с ХОБЛ.
Введение
В последние годы благодаря более глубокому пониманию патологических процессов, лежащих в основе хронической обструктивной болезни легких (ХОБЛ), и обогащению терапевтического потенциала современного врача существенно изменились и подходы к ведения этой категории пациентов. Стратегия, предлагаемая экспертами GOLD, основана на учете трех основных переменных характеристик ХОБЛ: степени тяжести бронхиальной обструкции, выраженности клинических симптомов и частоте повторных обострений болезни [1]. Напротив, испанские эксперты в основу разработанного ими терапевтического алгоритма положили принцип клинической фенотипизации больных ХОБЛ [2], нашедший поддержку и в ряде других стран. Впрочем, знакомство с обновленными версиями этих документов [3, 4] свидетельствует, что, несмотря на имеющиеся различия, оба они объединены глобальной целью повышения индивидуализации лечения.
Здесь же следует указать и еще на одно положение, сплачивающее эти и другие документы [5–7]: основным «инструментом» в достижении симптоматического контроля и снижении риска таких событий, как обострения ХОБЛ, прогрессирующее падение легочной функции и смерть больного, остаются бронходилататоры, тем более что возможности этого направления терапии претерпели сегодня радикальные изменения.
Выбор бронходилататоров в качестве приоритетного направления лечения больных ХОБЛ аргументируется их многочисленными саногенетическими эффектами (табл. 1), достигаемыми главным образом прямым стимулирующим действием на β2-адренорецепторы (β2-агонисты) и непрямым – посредством блокады влияния ацетилхолина на мускариновые холинорецепторы (холиноблокаторы или антихолинергические препараты).

β2-агонисты
Краткая история создания и применения
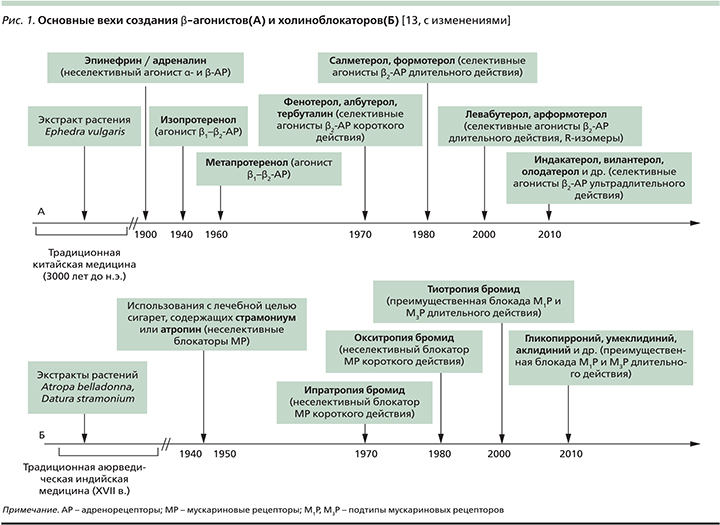
История применения симпатомиметиков с лечебной целью, продолжающаяся в наши дни созданием селективных β2-агонистов короткого, длительного и ультрадлительного действий, берет свое начала в недрах традиционной китайской медицины (3000 лет до н.э.). Уже в то время существовала практика использования экстракта растения Ephedra vulgaris (Ma Huang) в лечении больных одышкой [12] (рис. 1). Начало XIX в. ознаменовалось многочисленными усилиями по выделению экстракта надпочечников и использованию его в клинической практике. Первая успешная попытка подкожного введения эпинефрина (адреналина) с целью купирования астматического приступа датируется 1903 г., хотя бронходилатирующие свойства препарата будут установлены лишь через 4 года [14]. Инъекции водного раствора и суспензии эпинефрина в ургентной терапии острого бронхоспазма будут широко применяться вплоть до начала 1980-х гг. Менее популярным был опыт клинического использования препарата в форме аэрозоля [15].
В 1950-х гг. создаются первые неселективные β1/β2-агонисты в форме аэрозоля – изопротеренол и метапротеренол, которые на ближайшие несколько десятилетий станут «препаратами выбора» в лечении больных астмой [16]. Однако, несмотря на демонстративный бронходилатирующий эффект, эти препараты ввиду неселективности их β-агонистической активности, т.е. стимуляции β1-рецепторов сердечной мышцы, гладких мышц внутренних органов и др., характеризовались широким спектром серьезных нежелательных лекарственных реакций (табл. 2).

Начало 1980-х гг. было ознаменовано созданием прототипа селективных β2-агонистов – сальбутамола, характеризовавшегося быстрым началом и ограниченной продолжительностью (4–6 часов) бронходилатирующего эффекта. За этим последовала очередь β2-агонистов длительного действия (до 12 часов) – салметерола, формотерола, и наконец «венцом» эволюции этого класса лекарственных препаратов стали β2-агонисты ультрадлительного действия (до 24 часов) – индакатерол, олодатерол, вилантерол, кармотерол, абедитерол, PF-610355, AZD-3199 и др. [18].
Механизм действия
В основе механизма действия β-агонистов лежит их связывание с одной или несколькими цепочками ассоциированного с G-белком адренорецептора, следствием чего является стимуляция аденилатциклазы (рис. 2).

Аденилатциклаза, в свою очередь, стимулирует превращение аденозинтрифосфата в циклический 3’-5’-аденозинмонофосфат, активирующий протеинк...












