Фарматека №17 (350) / 2017
Деэскалация и эскалация лечения пациентов с HER2-позитивным раком молочной железы
1) ФГБУ «НИИ онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург;
2) Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова МЗ РФ, Санкт-Петербург;
3) Ташкентский педиатрический медицинский институт, Узбекистан
На прошедшей в марте 2017 г. 15-й St. Gallen Международной конференции по раку молочной железы (Вена) были рассмотрены спорные клинические вопросы с целью достичь согласия между 50 наиболее влиятельными в мире лидерами – членами панели. Также были рассмотрены результаты рандомизированных исследований с целью сузить или, наоборот, расширить стандарты местного и системного лечения. Внедрение в практику трастузумаба в комбинации с химиотерапией существенно улучшило результаты лечения HER2-позитивного рака молочной железы. Двойная ингибиция HER2 представляется многообещающей стратегией улучшения частоты pCR и выживаемости пациентов с раком молочной железы.
Стандарт адъювантной системной терапии пациентов с HER2-позитивным раком молочной железы (РМЖ) включает химиотерапию (ХТ) и 12 месяцев лечения трастузумабом. В нескольких рандомизированных исследованиях были изучены модификации стандартного лечения, которые были либо короче и менее затратны (деэскалация лечения), либо направлены на повышение эффективности с помощью двойной ингибиции HER2, или включали продолжительную (>12 месяцев) анти-HER2-таргетную терапию (эскалация лечения). На 15-й международной конференции по РМЖ (St. Gallen, 2017) были предоставлены данные рандомизированных исследований, в которых пытались либо сократить (деэскалировать), либо расширить (эскалировать) стандарты лечения HER2+РМЖ [1].
В 9 рандомизированных исследованиях сравнивали двойное ингибирование HER2+ХТ с трастузумабом+ХТ как неоадъювантное лечение раннего HER2-позитивного РМЖ. В этих исследованиях двойная таргетная HER2-терапия состояла из трастузумаба в комбинации с пертузумабом, нератинибом либо лапатинибом. Во всех 9 исследованиях двойное ингибирование HER2 совместно с ХТ приводило к значительному увеличению числа случаев полного патоморфологического ответа (pCR) по сравнению с одним трастузумабом+ХТ.
В адъювантной терапии 7 рандомизированных исследований рассматривали длительность назначения трастузумаба <12 месяцев. У пациентов, получавших адъювантную терапию трастузумабом <12 месяцев, не отмечено статистически значимого снижения безрецидивной или общей выживаемости (в 3 исследованиях, в которых были доступны данные по выживаемости, – E2198, PHARE, Hellenic trial), но в 2 из 3 исследований результаты при 12-месячной терапии были все же лучше.
В двух рандомизированных исследованиях оценивали продолжавшуюся более года адъювантную анти-HER2-таргетную терапию. В исследовании HERA годичная адъювантная терапия трастузумабом была так же эффективной, как и двугодичная, но ассоциировалась с меньшим числом побочных эффектов. В испытании ExteNET установлено, что годичная терапия нератинибом, назначавшаяся после первого года лечения трастузумабом, улучшила безрецидивную выживаемость в подгруппе пациентов с ER+/HER2+РМЖ, хотя продолжительность периода наблюдения за пациентами была короткой.
Таким образом, двойное ингибирование HER2 остается многообещающей стратегией и повышает частоту pCR. Результаты нескольких важных исследований, оценивавших двойное HER2-ингибирование и адъювантный режим трастузумаб–эмтансин (T–DM1), будут представлены в скором будущем. Они могут изменить современные стандарты лечения.
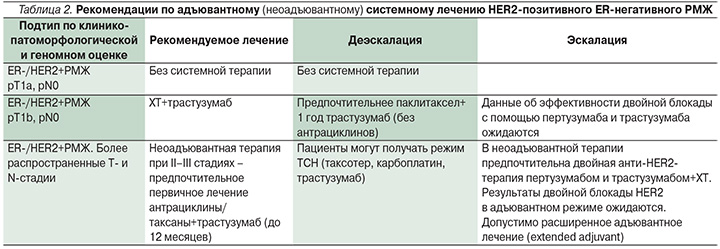
Панель экспертов St. Gallen, 2017, рекомендует адъювантную ХТ и анти-HER2-терапию при HER2-экспрессирующем РМЖ, начиная с pT1b pN0 и более высоких стадий. Не рекомендуется рутинное назначение адъювантной ХТ и анти-HER2-терапии при HER2-позитивном РМЖ стадии pT1a pN0. Схема паклитаксел+трастузумаб достаточна для большинства больных 1-й стадией HER2-экспрессирующего РМЖ, но при II– III стадиях заболевания рекомендуется двойная анти-HER2-терапия с комбинированной ХТ (табл. 1, 2).

Панель рекомендует стандартное адъювантное применение трастузумаба в течение года. У больных, получавших неоадъювантную анти-HER2-терапию путем двойной блокады пертузумабом и трастузумабом, рекомендуется завершить годичную терапию одним послеоперационным трастузумабом, но не рекомендуется адъювантное применение пертузумаба. Результаты оценки эффективности адъювантного применения пертузумаба ожидаются в 2018 г.
Панель одобрила использование биоаналогов трастузумаба в адъювантном режиме.
Данные одного рандомизированного исследования показали, что продленная адъювантная терапия нератинибом после завершения годичного применения трастузумаба может снизить частоту рецидивов при HER2-экспрессирующем РМЖ, особенно при гормонозависимых (ER+) HER2-положительных опухолях. Панель не рассматривала специфическую роль нератиниба, поскольку планируется дальнейшее изучение данного агента.
Неоадъювантная терапия и постнеоадъювантная терапия HER2-позитивного РМЖ
Панель поддержала использование неоадъювантной терапии при II или III стадии HER2-экспрессирующего РМЖ в качестве предпочтительного варианта начального лечения, особенно когда предполагается, что ответ на лечение может позволить уменьшить объем хирургического вмешательства или лучевой терапии. При HER2-экспрессирующем РМЖ панель одобрила двойную анти-HER2-неоадъювантную терапию пертузумабом и трастузумабом в комбинации с ХТ в качестве общепринятого варианта лечения....
12>12>











