Урология №5 / 2014
Диагностика и лечение локального рецидива рака предстательной железы с использованием гистосканирования и высокоинтенсивного фокусированного ультразвука у пациентов после радикальной простатэктомии
Кафедра урологии (зав. – д-р мед. наук, проф. Ю. Г. Аляев) ГБОУ ВПО «Первый МГМУ им. И. М. Сеченова»
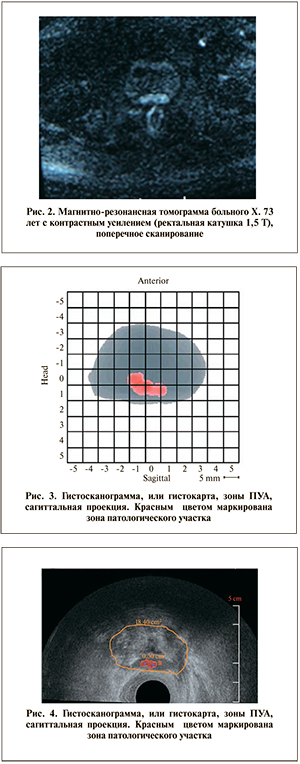
Целью работы стало улучшение диагностики и лечения пациентов, страдающих раком предстательной железы (РПЖ). В исследование включены 46 пациентов с рецидивом РПЖ после радикальной простатэктомии (РПЭ). В ходе обследования выполнены магнитно-резонансная томография с контрастным усилением (эндоректальная катушка 1,5Т) и гистосканирование. В отношении всех пациентов локальный рецидив был доказан морфологически по результатам трансректальной биопсии зоны пузырно-уретрального анастомоза. Лечение всем больным проводилось высокоинтенсивным фокусированным ультразвуком (ВИФУ).
Объем предстательной железы до РПЭ составил от 21 до 102 см3. Средний возраст – 62 (46–68) года. Уровень ПСА перед сеансом ВИФУ варьировался от 0,4 до 18,0 нг/мл. Nadir уровня ПСА спустя 3 мес наблюдения достиг 0,1 нг/мл. Пятилетняя безрецидивная выживаемость больных локальным рецидивом РПЖ после ВИФУ в группе низкого онкологического риска составила 10 (81%), умеренного – 18 (57%), высокого риска – 12 (42%). Магнитно-резонансная томография с контрастным усилением и гистосканирование служат высокоинформативными методами диагностики локального рецидива после РПЭ, а ВИФУ можно отнести к категории высокоэффективных методов лечения.
Введение. По данным ВОЗ, заболеваемость раком предстательной железы (РПЖ) во всем мире неуклонно растет. Россия не исключение – в структуре онкологической заболеваемости РПЖ занимает 3-е место после рака легких и желудка. Прирост заболеваемости за последние 10 лет составил 152,3%. Около 3% мужчин имеют шанс умереть от РПЖ [1].
«Золотым» стандартом в лечении локализованного РПЖ является радикальная простатэктомия (РПЭ) [2]. В 75–79% случаев пациентам с выявленной локализованной формой РПЖ выполняется лечение в объеме РПЭ. По данным мировой медицинской литературы, специфическая 5-летняя выживаемость достигает 95% [3]. Однако безрецидивная 5-летняя выживаемость этих пациентов варьируется в пределах 75–95% [4], а при местнораспространенных формах РПЖ снижается до 40%. Местный рецидив развивается не менее чем в 15% случаев лечения локализованного РПЖ независимо от выбранного метода лечения [5]. С учетом более активной хирургической активности при местнораспространенном РПЖ стадии T3a в ближайшее время стоит ожидать увеличения количества рецидивов РПЖ.
 К сожалению, до сих пор не существует единых критериев диагностики и выбора тактики лечения локального рецидива РПЖ после РПЭ. Методом лечения с доказанной эффективностью, но нежелательным влиянием на качество жизни является дистанционная лучевая терапия. Инновационными перспективными, но остающимися экспериментальными для этой группы больных считаются высокоинтенсивный фокусированный ультразвук (ВИФУ) и криодеструкция.
К сожалению, до сих пор не существует единых критериев диагностики и выбора тактики лечения локального рецидива РПЖ после РПЭ. Методом лечения с доказанной эффективностью, но нежелательным влиянием на качество жизни является дистанционная лучевая терапия. Инновационными перспективными, но остающимися экспериментальными для этой группы больных считаются высокоинтенсивный фокусированный ультразвук (ВИФУ) и криодеструкция.
В некоторых европейских странах (Франция, Германия) лечение ВИФУ служит методом выбора для пациентов с местным рецидивом после РПЭ. В исследовании Н. Azzouz (2006) общее число пациентов составило более 70 человек, средний уровень ПСА – 2,87 нг/мл до сеанса ВИФУ, надир ПСА – 0,21 нг/мл, безрецидивная выживаемость достигла 55%. В данном исследовании 84% контрольных биопсий были отрицательными, минимальный период наблюдения составил 7 мес, средний – 23 мес [6]. С учетом ограниченности выбора метода лечения такие результаты обнадеживают и позволяют надеяться на улучшение результатов лечения этих пациентов.
В России лечение больных РПЖ ВИФУ проводится с 2003 г. Одним из первых учреждений здраво- охранения, где начали выполнять подобные операции, стала клиника урологии Первого МГМУ им. И. М. Сеченова [7]. Накопленный опыт позволил применить данную методику к пациентам с локальным рецидивом РПЖ после РПЭ.
Материалы и методы. С октября 2004-го по февраль 2014 г. лечение локального рецидива РПЖ после РПЭ с применением ВИФУ проведено 46 пациентам. Объем предстательной железы до РПЭ составил в среднем 53 (от 21 до 102) см3, средний возраст – 62 (46–68) года. Уровень ПСА перед сеансом ВИФУ варьировался от 0,4 до 18 нг/мл.
В отношении всех пациентов местный рецидив РПЖ был доказан морфологически. Все больные до и после РПЭ были стратифицированы по стадиям (TNM) и степени онкологического риска (D'Amico), в ряде случаев послеоперационная оценка удаленной простаты изменяла стадию заболевания (рТ).
Локализованная стадия заболевания диагностирована 40 пациентам, из них низкий риск определен у 10 больных (Т и рТ совпали у всех пациентов), умеренный риск – у 18 (у 2 больных выявлена рТ3а, у 16 – Т=рТ), высокий риск – у 12 (у 4 пациентов выявлено рТ3а, у 8 – Т=рТ).
Местнораспространенная форма заболевания (стадия Т3а) до РПЭ была у 6 пациентов, из них рТ2b у 4 больных, рТ3а – у 2.
 Говоря о принципах воздействия ВИФУ, следует отметить эффект локальной гипертермии без повреждения окружающих тканей. Именно это позволило применить ВИФУ при местном рецидиве РПЖ после РПЭ.
Говоря о принципах воздействия ВИФУ, следует отметить эффект локальной гипертермии без повреждения окружающих тканей. Именно это позволило применить ВИФУ при местном рецидиве РПЖ после РПЭ.
В клинической практике при лечении методом ВИФУ используются аппараты Ablatherm® (EDAP TMS S.A., Франция) и Sonablate® (Focus Surgery Inc., США). Мы в своей работе применяем аппарат Ablatherm® robotic HiFu (EDAP, Франция).
В комплектацию аппарата Ablatherm® входят:
- лечебный модуль – операционный стол с электронными блоками внутри корпуса и приспособлениями для контроля за неподвижностью пациента;
- у...












