Урология №5 / 2013
Эффективность и безопасность цефиксима и амоксициллина/клавуланата при лечении бессимптомной бактериурии у беременных: многоцентровое рандомизированное проспективное исследование
ГБОУ ВПО «Смоленская государственная медицинская академия», ГБОУ ВПО «Кировская государственная медицинская академия», ГБОУ ВПО «Курский государственный медицинский университет»
Целью исследования было изучение эффективности и безопасности цефиксима и амоксициллина/клавуланата при лечении бессимптомной бактериурии у беременных. Выполнено проспективное многоцентровое рандомизированное исследование, в которое включили 112 беременных женщин с бессимптомной бактериурией. В 1-ю группу (цефиксим [супракс солютаб®] по 400 мг 1 раз в сутки
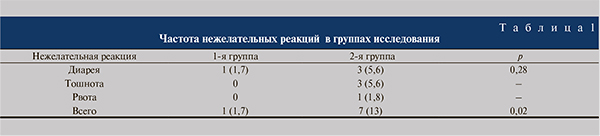
7 дней) были рандомизированы 58 женщин, 54 женщины были включены во 2-ю группу (амоксициллин/клавуланат [амоксиклав®] по 625 мг 3 раза в сутки 7 дней). Средний возраст пациенток 1-й группы составил 25,2±6,6; 2-й – 26,6±5,8 года. После включения в исследование на визитах 2 (день 10±1) и 3 (день 35±2) выполнили физикальное обследование, оценку жалоб, сбор сведений о нежелательных реакциях и бактериологический анализ мочи. Была выявлена сопоставимая эффективность цефиксима и амоксициллина/клавуланата при лечении бессимптомной бактериурии у беременных. Эрадикация возбудителя и стойкий бактериологический ответ отмечены соответственно у 94,8 и 92,7% женщин, получавших цефиксим, и у 98,2 и 92,5% женщин, получавших амоксициллин/клавуланат (p>0,05). При этом прием амоксициллина/клавуланата по сравнению с цефиксимом достоверно чаще (13 и 1,7% соответственно; p=0,02) сопровождался развитием нежелательных реакций. Семидневные курсы цефиксима в дозе 400 мг 1 раз в сутки и амоксициллина/клавуланата в дозе 625 мг 3 раза в сутки являются высокоэффективными режимами терапии бессимптомной бактериурии у беременных в России. Прием амоксициллина/клавуланата достоверно чаще сопровождается развитием нежелательных реакций по сравнению с цефиксимом.
Введение. Под бессимптомной бактериурией (ББ) понимают выделение одного и того же вида микроорганизма в титре ≥105 КОЕ/мл в двух последовательных образцах мочи у лиц, не имеющих симптомов инфекции мочевыводящих путей (ИМП) [1]. Бессимптомная бактериурия широко распространена в популяции, ее частота зависит от возраста, пола, наличия аномалий органов мочевого тракта и ряда других факторов [2]. Так, у здоровых женщин частота ББ значительно варьируется в зависимости от возраста: от 1% в 5–14 лет до 20% у женщин старше 80 лет [2]. На сегодняшний день доказано, что ББ в большинстве случаев не требует лечения; исключение составляют беременные и пациенты, которым планируется проведение оперативного вмешательства на органах мочевой системы [1].
Показатель распространенности ББ среди беременных колеблется в широких пределах – от 2,5 до 26,0% [3–5]. Необходимо отметить, что, несмотря на отсутствие какой-либо клинической симптоматики, ББ является одним из основных факторов риска возникновения ИМП у беременных [4]. Было показано, что на ранних сроках беременности ББ в 20–30 раз повышает риск развития пиелонефрита [1, 6]. Наряду с этим ББ сопровождается рядом серьезных акушерских осложнений, таких как преждевременные роды, рождение детей с низкой массой тела и инфекционные осложнения у родильницы [7]. Проведение адекватной противомикробной терапии позволяет уменьшить риск развития пиелонефрита у беременных с ББ с 20–35 до 1–4% [8]. Также в ряде клинических исследований и мета-анализов доказано, что назначение противомикробных препаратов беременным с ББ позволяет добиваться снижения риска рождения детей с низкой массой тела и преждевременных родов [9, 10]. Однако, несмотря на всю важность проблемы, число рандомизированных исследований, в которых бы изучалась эффективность и безопасность различных противомикробных препаратов при лечении ББ у беременных, ограничено [11].
Целью настоящей работы было сравнить эффективность и безопасность 7-дневных курсов цефиксима и амоксициллина/клавуланата при лечении ББ у беременных.
Материалы и методы. В 2009–2011 гг. на базе трех центров (женские консультации при ОГБУЗ КБ № 1 Смоленска, Курском государственном медицинском университете и Кировской государственной медицинской академии) было проведено многоцентровое проспективное рандомизированное исследование эффективности и безопасности 7-дневных курсов цефиксима (супракс солютаб®, «АстелласФармаЮроп Б.В.») и амоксициллина/клавуланата (амоксиклав®, «Сандоз/Лек»). В исследование включили беременных при наличии письменного информированного согласия, у которых в двух последовательных образцах мочи, собранных с интервалом 24 и более часов, был выделен один и тот же вид бактерий в титре ≥105 КОЕ/мл.
Критерии исключения...