Эпидемиология и Инфекционные болезни. Актуальные вопросы №5 / 2016
Эффективность и безопасность препарата элпивирин в составе схемы антиретровирусной терапии в течение 24–48 недель в сравнении со схемой, содержавшей эфавиренз
1Центральный НИИ эпидемиологии Роспотребнадзора, Москва;
2 Московский областной центр по профилактике и борьбе со СПИДом и ИЗ;
3 Инфекционная клиническая больница № 2 Департамента здравоохранения города Москвы;
4Волгоградский областной центр по профилактике и борьбе со СПИДом и инфекционными заболеваниями;
5Республиканский центр по профилактике и борьбе со СПИД и инфекционными заболеваниями Министерства здравоохранения Республики Татарстан, Казань;
6Центр по профилактике и борьбе со СПИД и инфекционными заболеваниями, Санкт-Петербург;
7Пермский краевой центр по профилактике и борьбе со СПИД и инфекционными заболеваниями;
8Областной клинический кожно-венерологический диспансер, Рязань;
9Тольяттинская городская клиническая больница № 5;
10Липецкий областной центр по профилактике и борьбе со СПИД инфекционными заболеваниями;
11Клиническая инфекционная больница им. С.П. Боткина, Санкт-Петербург;
12Республиканска клиническая инфекционная больница Министерства здравоохранения Удмуртской Республики, Ижевск;
13ООО «Вириом», г. Химки, Московская область;
14ООО «ИФАРМА» », г. Химки, Московская область
В статье представлены результаты исследования HIV-VM1500-04 через 24–48 недель лечения.
Материалы и методы. В исследование было включено 120 взрослых больных ВИЧ-инфекцией, рандомизированных в 2 группы (1:1). Больные основной группы получали TDF/FTC + элпивирин (VM-1500, Elpida®), больные контрольной группы – TDF/FTC + EFV. 91,7% больных основной и 80% больных контрольной группы завершили или продолжают исследование.
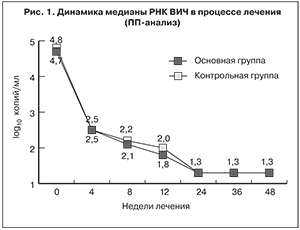
Результаты. Схема антиретровирусной терапии (АРТ), включавшая элпивирин в дозе 20 мг в сутки в комбинации с TDF/FTC, через 24–48 недель лечения была не менее эффективна, чем схема EFV + TDF/FTC, вне зависимости от исходного уровня вирусной нагрузки. Через 24 недели АРТ в основной группе, доля пациентов с уровнем РНК ВИЧ < 50 копий/мл была существенно выше, чем в контрольной: 84,5 и 66,7% (MITT-анализ; p = 0,031). Безопасность применения в течение 24–48 недель схемы АРТ, включавшей элпивирин, была выше, чем при использовании схемы, содержавшей EFV. Развитие НЯ «особого интереса» (нарушения со стороны ЦНС и психической деятельности) существенно реже выявляли в основной группе (30%), чем в контрольной (62,1%; р < 0,001).
Окончание исследования ожидается в ноябре 2016 г.
Применяемые в качестве стартовых режимов современные схемы антиретровирусной терапии (АРТ), как правило, содержат 2 препарата из группы нуклеозидных (нуклеотидных) ингибиторов обратной транскриптазы ВИЧ (НИОТ/НтИОТ), в сочетании с ненуклеозидным ингибитором обратной транскриптазы ВИЧ (ННИОТ), либо ингибитором протеазы или интегразы ВИЧ.
Комбинация, состоящая из тенофовира/эмтрицитабина/эфавиренза (TDF/FTC/EFV), была первым режимом, который применяли в виде 1 таблетки 1 раз в сутки. В настоящее время сочетание препаратов тенофовир/эмтрицитабин/рилпивирин (TDF/FTC/RPV) является единственной зарегистрированной в России схемой АРТ с приемом 1 таблетки 1 раз в сутки [1]. Вместе с тем на основании проведенных исследований комбинация TDF/FTC/RPV рекомендована в качестве режима первой линии (пациентам, ранее не получавшим лечения) больным с исходным уровнем РНК ВИЧ < 100 000 копий/мл, поскольку при более высоких уровнях вирусной нагрузки эффективность терапии по этой схеме может быть недостаточна [2–5]. Применение в режимах АРТ первой линии препарата EFV более чем у 60% пациентов сопровождается развитием нежелательных явлений (НЯ) со стороны центральной нервной системы, в результате чего схема TDF/FTC/EFV в рекомендациях специалистов США была переведена из приоритетных в альтернативные [3].
В августе 2014 г. было начато исследование № 219 (II–III фаза) – международное многоцентровое рандомизированное частично слепое клиническое исследование эффективности, безопасности и подбора оптимальной дозировки препарата элпивирин (VM-1500; Elpida®) в сравнении с EFV на фоне стандартной базисной АРТ, состоящей из 2 НИОТ/НтИОТ, у инфицированных ВИЧ-1 пациентов, ранее не получавших лечения [6].
 Исследование включало 2 этапа. Основной целью 1-го этапа был выбор оптимальной дозы элпивирина (20 или 40 мг в сутки) в сочетании с базисной терапией (2 НИОТ/НтИОТ) на основании эффективности (доля больных с РНК ВИЧ < 400 копий/мл через 12 недель лечения) в сравнении с EFV.
Исследование включало 2 этапа. Основной целью 1-го этапа был выбор оптимальной дозы элпивирина (20 или 40 мг в сутки) в сочетании с базисной терапией (2 НИОТ/НтИОТ) на основании эффективности (доля больных с РНК ВИЧ < 400 копий/мл через 12 недель лечения) в сравнении с EFV.
На 1-м этапе в исследование было включено 90 пациентов с ВИЧ-1-инфекцией, ранее не получавших АРТ, которые были рандомизированы в 3 группы: в 1-й 30 больных получали элпивирин в дозе 20 мг в сутки; во 2-й 30 больных получали элпивирин по 40 мг в сутки; в 3-й (группа сравнения) 30 больных получали EFV по 600 мг в сутки. Кроме того, все пациенты получали 2 НИОТ/НтНИОТ – TDF/FTC [6].
Через 12 недель лечения, по завершении 1-го этапа исследования, были получены результаты, доказавшие равную эффективность элпивирина в дозах 20 мг и 40 мг в сочетании с TDF/FTC и схемы EFV + TDF/FTC вне зависимости от исходного уровня вирусной нагрузки.
Наиболее безопасным режимом после 12 недель терапии оказалась схема, включавшая суточную дозу препарата 20 мг. Особо были проанализированы нарушения со стороны ЦНС и психической деятельности (так называемые НЯ «особого интереса»), которые достоверно реже наблюдали у пациентов 1-й группы (26,7%) по сравнению с пациентами 3-й группы (57,1%) [6].
На основании результатов, полученных на 1-м этапе, для проведения дальнейших исследований была одобрена доза элпивирина 20 мг в сутки.
Основной целью 2-го этапа исследования было сравнение эффективности (доля больных с РНК ВИЧ < 50 копий/мл через 24 недели лечения) выбранной дозы элпивирина (20 мг в сутки) и EFV в сочетании с 2 НИОТ/НтИОТ.
Помимо целей, которые были решены на 1-м этапе, в исследовании был сформулирован ряд дополнительных целей:
- вирусологических – среднее снижение РНК ВИЧ в течение 48 недель исследуемой терапии; доля пациентов, продолживших прием исследуемой терапии до 48 недели;
- иммунологических – изменение абсолютного числа СD4+- и СD8+-лимфоцитов в течение 48 недель терапии;
- оценка резистентности ВИЧ – доля пациентов, у которых в течение 48 недель развилась резистентность ВИЧ-1 к исследуемой терапии;
- оценка безопасности – частота развития НЯ различной степени тяжести по данным субъективных жалоб, физикального осмотра, жизненных показателей, лабораторных исследований; частота развития НЯ «особого интереса», в том числе нарушений со стороны ЦНС.
Материалы и методы
В исследование включали мужчин и женщин в возрасте 18 лет и старше с серологически подтвержденной ВИЧ-1-инфекцией (методами ИФА и иммунного блотинга), стабильным клиническим течением ВИЧ-инфекции (клинические стадии 1 или 2 по классификации ВОЗ), которым по решению Исследователя показано начало АРТ [согласно Сводному руководству ВОЗ по использованию антиретровирусных препаратов (АРП) для лечения и профилактики ВИЧ-инфекции от 2013 г.], с уровнем РНК ВИЧ-1 в плазме крови ≥ 5000 копий/мл и количеством СD4+-лимфоцитов > 200 клеток/мкл на скрининге. Перед проведеним скрининга все пациенты подписывали информационный листок пациента и форму информированного согласия на участие в исследовании. Кроме того, было получено согласие пациентов на использование в течение всего исследования адекватных методов контрацепции (презерватив со спермицидом).
 На 2-м этапе в исследовании приняли участие 120 больных ВИЧ-1-инфекцией, ранее не получавших АРТ. В основную группу были включены 30 больных, завершивших 1-й этап исследования и получавших выбранную дозу элпивирина (20 мг), а также дополнительно рандомизированы 30 новых пациентов с ВИЧ-инфекцией, соответствующих критериям включения. Контрольная группа состояла из 30 больных, получавших на 1-м этапе исследования EFV (600 мг в сутки) и продолживших терапию. В эту группу также было дополнительно рандомизировано 30 новых пациентов в соответствии с критериями включения.
На 2-м этапе в исследовании приняли участие 120 больных ВИЧ-1-инфекцией, ранее не получавших АРТ. В основную группу были включены 30 больных, завершивших 1-й этап исследования и получавших выбранную дозу элпивирина (20 мг), а также дополнительно рандомизированы 30 новых пациентов с ВИЧ-инфекцией, соответствующих критериям включения. Контрольная группа состояла из 30 больных, получавших на 1-м этапе исследования EFV (600 мг в сутки) и продолживших терапию. В эту группу также было дополнительно рандомизировано 30 новых пациентов в соответствии с критериями включения.
Таким образом, через 24 недели исследования (2-й этап) сравнивали результаты, полученные от пациентов основной и контрольной групп, каждая из которых на момент начала исследования включала 60 больных ВИЧ-инфекцией.
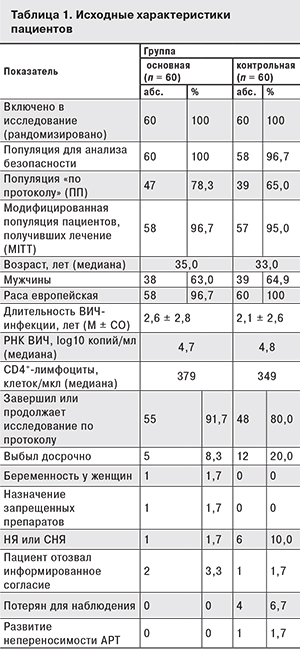
Исходные характеристики пациентов представлены в табл. 1. Существенных различий между группами пациентов в исходных показателях обнаружено не было. Среди вто...>
>>











