Фарматека №8 (281) / 2014
Эверолимус (Афинитор): новые возможности терапии злокачественных опухолей
ФГБУ «РОНЦ им. Н.Н. Блохина» РАМН, Москва
Представлены результаты клинического изучения эффектов ингибитора mTORэверолимуса (Афинитор) при различных злокачественных новообразованиях. Препарат связывает внутриклеточный протеин, что ведет к торможению mTOR-киназной активности. Дополнительно он тормозит экспрессию гипоксиюиндуцирующего фактора и уменьшает экспрессию эпидермального фактора роста (EGFR). Первоначально эверолимус был одобрен FDA США в качестве средства 2-й линии лечения распространенного почечноклеточного рака. Затем он был разрешен к лечению субэпендимальных гигантоклеточных астроцитом, ассоциированных с туберозным склерозом; прогрессирующих нейроэндокринных опухолей поджелудочной железы, почечной ангиолипомиомы в составе комплекса поражений при туберозном склерозе. Последним показанием к применениюэверолимуса (2012) стал HR+-, HER2-метастатический РМЖ, ранее леченный нестероидными ингибиторами ароматазы. Обсуждаются возможности расширения клинического применения эверолимуса.
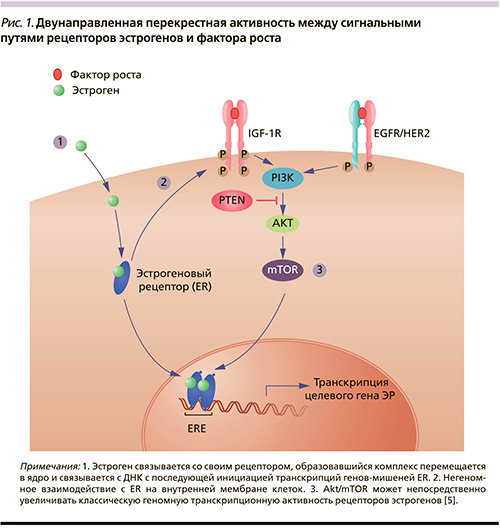
Эверолимус (Афинитор) является ингибитором mTOR. Внутриклеточный сигнальный путь PI3K/AKT/mTOR, регулирующий выживание, рост и пролиферацию, метаболизм и ангиогенез опухолевой клетки, – один из основных опухолевого развития или канцерогенеза. Кроме того, активация пути mTOR наблюдается при генетических онкологических (болезнь фон Гиппеля–Линдау, нейрофиброматоз I типа) и других (туберозный склероз) синдромах.
Внутриклеточные взаимодействия чрезвычайно многообразны. Однако некоторые механизмы этих взаимодействий между различными органами-мишенями уже известны и, более того, используются в клинической практике для комбинации таргетных препаратов.
Примером таких комбинаций считается применение эверолимуса в сочетании с гормонотерапией (ГТ) с целью восстановления чувствительности к последней при диссеминированном раке молочной железы (РМЖ) или с октреотидом при нейроэндокринных опухолях (НЭО).
По механизму действия эверолимус потенциально может быть эффективным при ряде опухолей; первым показанием к его клиническому использованию стал почечноклеточный рак (ПКР). Препарат входит в клинические рекомендации в качестве средства 2-й линии терапии при прогрессировании заболевания после терапии ингибиторами тирозинкиназ (сунитиниб, сорафениб, пазопаниб).
Наиболее полно эверолимус изучен при НЭО, при которых проведено три рандомизированных клинических исследования RADIANT.
В предварительном исследовании II фазы была показана эффективность комбинации эверолимуса с октреотидом при НЭО поджелудочной железы (ПЖ), и в первом рандомизированном сравнительном исследовании (RADIANT-1) была установлена более высокая, чем одного эверолимуса, эффективность комбинации: контроль роста опухоли – 84,4 против 77 %, медиана выживаемости без прогрессирования (МВБП) – 16,7 против 9,7 месяца [1].
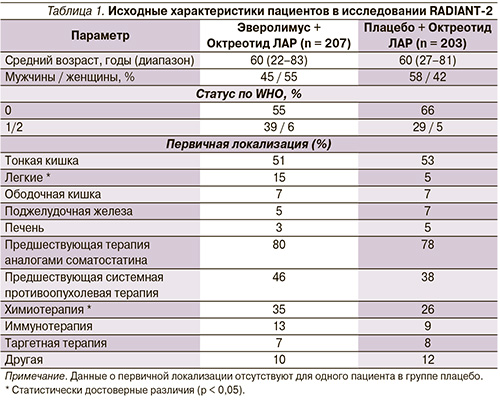
В рамках III фазы было проведено еще два исследования. Одно из них – RADIANT-2, двойное слепое плацебо контролируемое исследование, сравнивавшее комбинацию эверолимус + октреотид (Э + О) с плацебо в сочетании с октреотидом (Р + О) для пациентов с секретирующими опухолями. Характеристика больных представлена в табл. 1.
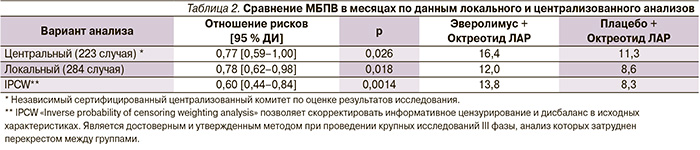
Основной целью исследования стала оценка ВБП. По данным централизованного анализа, медиана оказалась выше в группе с эверолимусом (16,4 против 11,3 месяца; р = 0,026). Пороговое значение показателя «р» по дизайну исследования должно было составить 0,0246. По данным исследователей, результаты были несколько другими: МВБП Э + О – 12,0 месяцев, П + О – 8,6 месяца (р = 0,018).
В связи с этим независимый комитет еще раз рассмотрел результаты и пришел к окончательному выводу о достоверном улучшении МВБП на 5,1 месяца при лечении комбинацией Э + О пациентов с НЭО с секреторной активностью (табл. 2) [2].
В исследовании это преимущество было подтверждено при подгрупповом анализе, также было показано улучшение контроля уровня 5-гидроксииндолуксусной кислоты, что является предпосылкой к предотвращению развития «карциноидного» сердца.
Подгруппа НЭО легких включила 44 из 429 больных, т.е. приблизительно 10 %. МВБП составила 13,6 против 5,5 месяцев в пользу комбинации Э + О. Отношение рисков (ОР) составило 0,72. В связи с этим указанная комбинация зарегистрирована в качестве лечебной для больных НЭО ПЖ и легких в Российской Федерации.
В исследовании RADIANT-3 сравнивали наилучшее для больных НЭО ПЖ низкой или умеренной степени злокачественности (Gr1 и Gr2), поддерживающее лечение (НПЛ), + эверолимус и НПЛ + плацебо. МВБП для эверолимуса составила 11 месяцев, для плацебо – 4,6 (р < 0,0001). Время лечения составило 8,79 месяца в группе эверолимуса и 3,70 – в группе плацебо; при прогрессировании 148 больных группы плацебо перешли в группу эверолимуса. При этом 18-месячная выживаемость в группе эверолимуса составила 57,3 %, двугодичная – 34,2. Наиболее частыми побочными явлениями при применении эверолимуса были стоматит (64 %), сыпь (49 %), диарея (34 %), утомляемость (31 %), инфекции (23 %).
Таким образом, программа исследований RADIANT, включившая 999 больных, показала эффективность эверолимуса в монотерапии НЭО ПЖ и в комбинации с октреотидом при секретирующих НЭО.
В отделении химиотерапии ФГБУ «РОНЦ им. Н.Н. Блохина» РАМН имеется опыт применения эверолимуса к 21 больному, у 11 из которых были НЭО ПЖ. Опухолями Gr2 страдали 11 больных, 18 – метастазами в печень. Ранее 9 больным проведены циторедуктивные операции, 19 ...












