Кардиология №10 / 2016
Факторы, ассоциированные с непосредственными результатами коронарного шунтирования у больных ишемической болезнью сердца при наличии сахарного диабета 2-го типа
ФГБНУ НИИ комплексных проблем сердечно-сосудистых заболеваний, Кемерово
Оценены факторы, связанные с сердечно-сосудистыми осложнениями (ССО) после коронарного шунтирования (КШ), в зависимости от наличия сахарного диабета (СД) 2-го типа. Проведен ретроспективный анализ историй болезни 667 пациентов, подвергшихся КШ в период с 2006 по 2009 г. в хирургической клинике ФГБУ «НИИ КПССЗ СО РАМН (317 пациентов с СД-2, 350 пациентов без СД и других нарушений углеводного обмена, сопоставимые по полу, возрасту, условиям проведения КШ). Связь возможных факторов с частотой развития ССО оценивали в модели логистической регрессии. Предикторы ССО в выделенных группах были различными в зависимости от наличия СД. Независимыми предикторами ССО у больных СД были наличие аневризмы левого желудочка (ЛЖ), митральной регургитации, снижение фракции выброса (ФВ) ЛЖ и увеличение уровня гликированного гемоглобина. У пациентов без СД таковыми являются увеличение возраста пациентов, КШ в условиях искусственного кровообращения, сочетанные операции, наличие митральной регургитации, снижение ФВ ЛЖ.
В последние годы отмечается повсеместное увеличение распространенности сахарного диабета (СД), часто встречается его сочетание с ишемической болезнью сердца (ИБС), что приводит к увеличению доли больных СД при операции коронарного шунтирования (КШ) до 30—35% [1, 2] и более. Наличие СД влияет на выбор тактики реваскуляризации миокарда при многососудистом поражении коронарных артерий (КА). В исследовании FREEDOM показано преимущество КШ по сравнению с использованием стентов с лекарственным покрытием [3]. Об этом же свидетельствуют и результаты нескольких мета-анализов, опубликованных недавно [4—7]. Данные литературы о влиянии СД на результаты КШ остаются противоречивыми. С одной стороны, появляется все больше свидетельств отсутствия негативного влияния СД на непосредственные результаты КШ [8—10]. С другой стороны, показано негативное влияние СД как на стоимость пребывания больных в стационаре при КШ, так и на его отдаленные результаты [2, 11]. Соответственно, остается актуальной задача поиска точек приложения для воздействий по улучшению результатов КШ у больных СД [5, 12—17]. Это и послужило основанием для проведения настоящего исследования, целью которого было изучение факторов, связанных с развитием сердечно-сосудистых осложнений (ССО) после КШ у больных СД и в его отсутствие.
Материал и методы
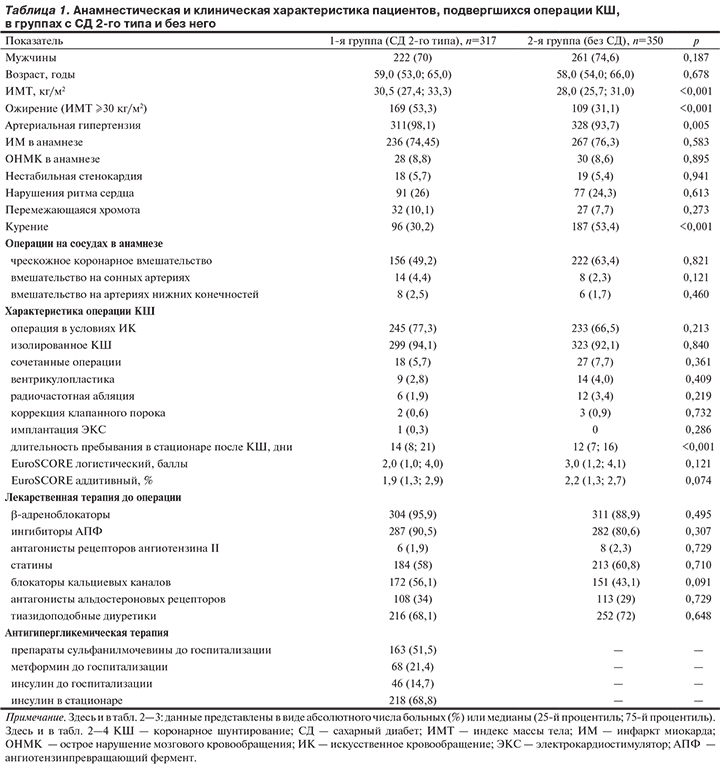
Проведен ретроспективный анализ базы данных 2411 пациентов с ИБС, подвергшихся КШ в период с января 2006 г. по ноябрь 2009 г. Среди них выделены 317 пациентов с СД 2-го типа (СД-2), затем отобраны 350 пациентов без документально подтвержденных нарушений углеводного обмена, сравнимые по полу, возрасту, сопутствующей патологии, получаемой терапии с больными СД. Проведен дополнительный анализ их историй болезни с формированием новой базы данных из 667 человек: 1-я группа — пациенты с СД-2 (n=317, медиана возраста 59 лет), 2-я группа — пациенты без СД и других нарушений углеводного обмена (n=350, медиана возраста 58 лет). Критерии исключения из исследования: наличие нарушений углеводного обмена, кроме СД-2 (нарушение уровня глюкозы в крови натощак, нарушение толерантности к углеводам, СД 1-го типа и др.). Диагноз СД-2 устанавливали в соответствии с критериями современной классификации СД. Предоперационная подготовка пациентов с СД включала достижение компенсации углеводного обмена под контролем эндокринолога, отмену пероральных антигипергликемических препаратов (АГП) и инсулина средней продолжительности действия перед операцией, назначение инсулина короткого действия (подкожно). Периоперационно у всех пациентов проводили контроль уровня глюкозы в крови в реанимационном отделении, при необходимости купирование гипергликемии с помощью инсулина короткого действия (внутривенно и подкожно) с последующим контролем эффективности терапии.
Проанализированы данные анамнеза, эхокардиографии (ЭхоКГ), коронарографии (КГ), ультразвукового и ангиографического исследования аорты, брахиоцефального и периферического артериальных бассейнов. Подтверждение наличия и оценку распространенности атеросклеротического поражения проводили с помощью цветового дуплексного сканирования (ЦДС) экстракраниальных отделов брахиоцефальных артерий (БЦА) и артерий нижних конечностей (АНК). По показаниям выполняли ангиографию БЦА с целью уточнения локализации и анатомических особенностей окклюзионно-стенотических изменений после ЦДС. Пациенты с поражением аорты и ее крупных ветвей, атеросклерозом АНК подвергались аортографии и/или селективной периферической ангиографии. Одновременно с исследованием некоронарных артериальных бассейнов или в предшествующий период времени (но не ранее, чем за 6 мес) пациентам проводили коронарографию. Гемодинамически значимыми считали стенозы магистральных КА 70% и более, для ствола левой КА (ЛКА) — 50% и более. Мультифокальным атеросклерозом (МФА) считали одновременное наличие стенозов, суживающих просвет артерий не менее 30%, в двух и более артериальных бассейнах. Лабораторные показатели оценивали перед операцией, дополнительно оценивали показатели гликемического профиля в течение 1-х суток после операции. В качестве осложнений КШ учитывали интра- и послеоперационный инфаркт миокарда (ИМ), который устанавливали при наличии «нового» зубца Q на электрокардиограмме, изменений сегмента ST—T, сопровождающихся снижением фракции выброса (ФВ) левого желудочка (ЛЖ) и/или повышением уровня тропонина I; сердечную недостаточность (СН), требующую длительной инотропной поддержки; пароксизмы фибрилляции предсердий (ФП); острое нарушение мозгового кровообращения (ОНМК); острую почечную недостаточность, полиорганную недостаточность; пневмонии; длительное пребывание на искусственной вентиляции легких — ИВЛ (>24 ч); экстракорпоральную коррекцию гомеостаза; внутриаортальную баллонную контрпульсацию (ВАБК); различные осложнения в области стернальной раны: длительную экссудацию, гнойные осложнения, диастаз груди...












