Кардиология №10 / 2015
Фармако-инвазивный подход, направленный на сохранение функции левого желудочка у пациентов со стабильной ишемической болезнью сердца на фоне нарушений углеводного обмена
ФГБУ Научно-исследовательский институт кардиологии, Томск
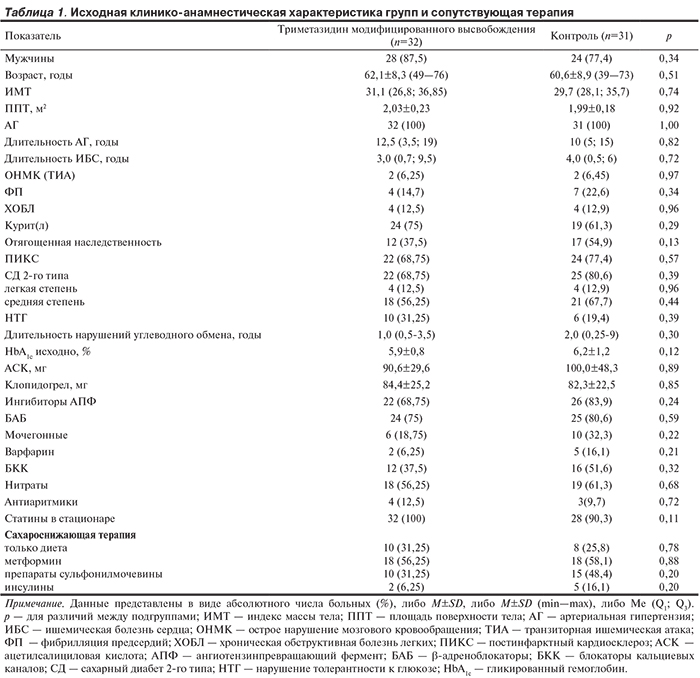
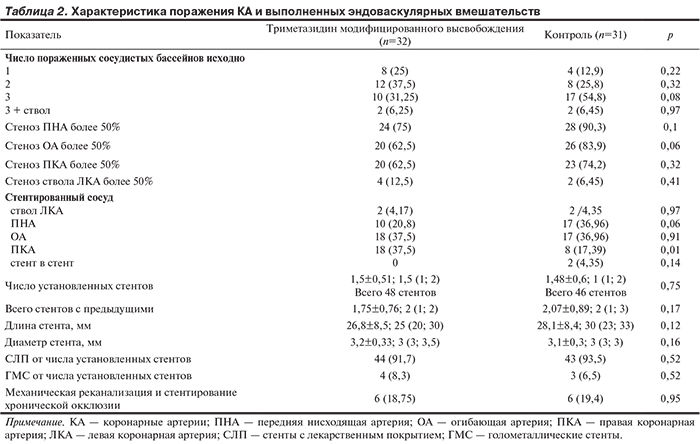
Проведено открытое проспективное рандомизированное контролируемое клиническое исследование, включившее 63 пациентов со стабильной формой ишемической болезни сердца на фоне нарушений углеводного обмена. Всем больным выполнено плановое стентирование коронарных артерий. Пациенты основной группы (n=32) в течение 2 нед перед вмешательством получали триметазидин модифицированного высвобождения 35 мг 2 раза в сутки в дополнение к стандартной терапии. Пациентам контрольной группы (n=31) чрескожное коронарное вмешательство и последующее наблюдение проводилось на фоне стандартной терапии без применения препаратов метаболического действия. Выявлено, что длительный прием миокардиального цитопротектора триметазидина модифицированного высвобождения приводит к достоверному улучшению сократительной функции миокарда левого желудочка в отдаленный период по данным эхокардиографии (снижение конечного диастолического индекса на 5,5%, снижение конечного систолического индекса на 4,4%, увеличение фракции выброса на 2,5% через 12 мес после эндоваскулярной реваскуляризации миокарда по сравнению с исходным значением).
Число пациентов с сахарным диабетом (СД) продолжает увеличиваться в индустриальном обществе в силу главным образом изменений в образе жизни (чрезмерное потребление калорий и жиров, снижение физической активности). Предполагается, что во всем мире число заболевших СД взрослых будет превышать 200 000 000 в течение ближайших 10 лет [1]. Неблагоприятный прогноз для больных СД в основном связан с развитием хронической сердечной недостаточности (ХСН) [2]. Более 1/3 больных СД 2-го типа умирают от сердечной недостаточности (СН), при этом наличие СД связано с 2—5-кратным увеличением риска развития СН, которая является наиболее распространенным диагнозом при госпитализации у пациентов с СД [3—5]. Сердечная и почечная недостаточность служат основными факторами, определяющими исход у пациентов с сочетанием СД и ишемической болезни сердца (ИБС) [6].
Хотя понятно, что существует ассоциация между СД и СН и худшим прогнозом для пациентов с СД и СН, патофизиологическое объяснение этой ассоциации менее ясно. Наиболее вероятным объяснением является наличие кардиотоксической триады: диабетическая кардиомиопатия (КМП), ИБС и артериальная гипертензия (АГ) / гипертрофия желудочков. Однако и другие механизмы в виде измененной экспрессии генов, вегетативной дисфункции играют важную роль в развитии и прогрессировании СН у больных СД [7]. Становится все более ясно, что СД сам вызывает систолическую и диастолическую СН, независимо от сопутствующего заболевания коронарных артерий (КА).
Лечение ИБС у пациентов с СД 2-го типа остается большой проблемой для кардиологов [8]. Несмотря на значительные достижения терапевтических и инвазивных методов лечения, включая имплантацию стентов с лекарственным покрытием, эти пациенты все еще имеют высокую инвалидизацию и смертность в результате прогрессирования атеросклероза и ХСН даже после чрескожной или хирургической реваскуляризации [9]. Рандомизированные клинические исследования сообщают об уровне смертности более 19,6% после операции аортокоронарного шунтирования — маммарокоронарного шунтирования и до 35% после ангиопластики в этой популяции [10].
Однако пока не существует конкретных стратегий профилактики, диагностики и лечения СН у пациентов с СД. Данные об эффективности и переносимости препаратов, используемых при лечении пациентов с СН и СД, являются в основном ограниченным анализом подгрупп в рандомизированных клинических исследованиях с частыми проблемами недостаточной статистической мощности. Тем не менее этот анализ подгрупп последних исследований, проведенный у больных СД, которые были госпитализированы по поводу СН, показал разную эффективность стандартной терапии и большую склонность к развитию побочных эффектов по сравнению с таковыми у пациентов с той же степенью СН, но без СД. Необходимы дальнейшие исследования для разработки целенаправленной терапии у пациентов с сопутствующими СН и СД. Препараты, направленные на изменение метаболизма, являются потенциально многообещающими для лечения СН у больных СД.
У пациентов с СД и ИБС метаболические изменения, происходящие в результате несоответствия между кровоснабжением и метаболическими потребностями сердца, усугубляются метаболическими изменениями, вызванными СД [11, 12]. Энергетическими субстратами кардиомиоцитов служат глюкоза и свободные жирные кислоты (СЖК). При стрессе и ишемии происходит сдвиг метаболизма в сторону использования СЖК, что является неоптимальным с точки зрения использования кислорода. Именно увеличение поглощения и использования СЖК служит одной из основных причин повышенной восприимчивости «диабетического сердца» к ишемии миокарда и значительного снижения функции миокарда для данного количества ишемии по сравнению с «недиабетическим сердцем» [11]. Ожидаемое количество молей АТФ, производимых на 1 моль потребляемого кислорода, на 12% больше при окислении глюкозы, чем при окислении СЖК, поэтому улучшение метаболизма глюкозы может увеличить производство АТФ до 30% [13]. В связи с изложенным модуляция метаболизма миокардиальных СЖК представляет ключевую задачу метаболических вмешательств у пациентов с ИБС и СД.
Ранее было показано, что частичный ингибитор окисления СЖК в миокарде триметазидин обладает антиишемическим свойством, снижая частоту приступов стенокардии, потребность в короткодействующих нитратах, улучшая переносимость физических нагрузок в сочетании с антиангинальными препаратами гемодинамического действия [14, 15]. Триметазидин является ингибитором 3-кетоацилкоэнзим А тиолазы (3-КАТ), который сдвигает получение энергии в кардиомиоците от окисления СЖК к окислению глюкозы путем ингибирования митохондриальной длинноцепочечной 3-КАТ[13]. Кроме того, доказано, что триметазидин ослабляет окислительный стресс [16], уменьшает потребление кислорода и улучшает обмен веществ митохондрий и работу сердца в условиях ишемии [17]. Есть сообщения об ослаблении активности нейтроф...












