Терапия №7-8 / 2018
Функциональное состояние тромбоцитов и реологических свойств крови у больных хронической сердечной недостаточностью с кардиопульмональной патологией
1 ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России;
2 Московский областной перинатальный центр, г. Балашиха
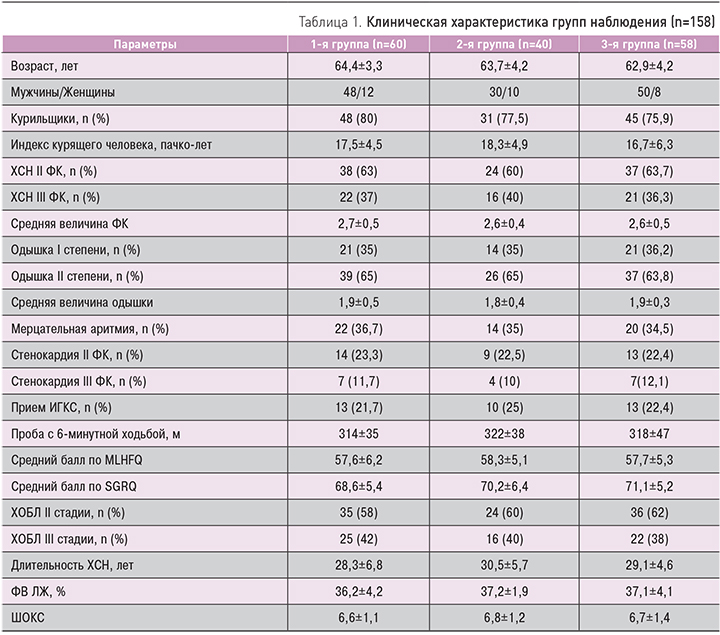
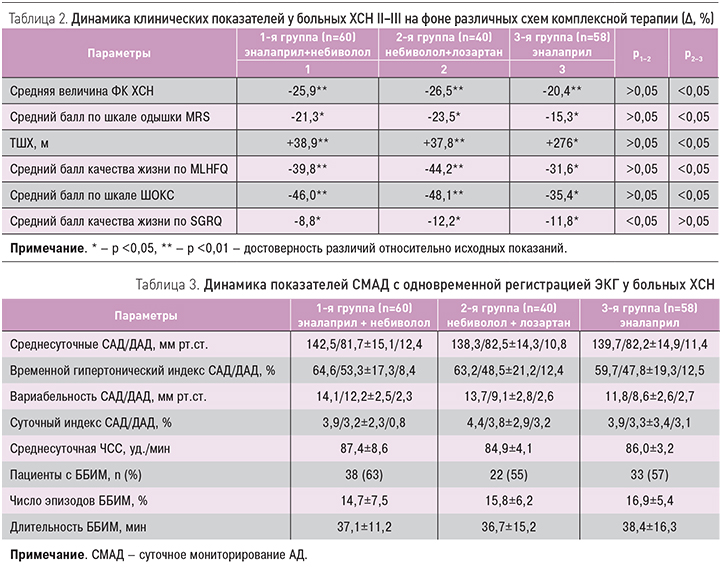
По мнению ряда авторов, сочетание ишемической болезни сердца (ИБС) и хронической обструктивной болезни легких (ХОБЛ) приводит к синдрому взаимного отягощения и требует особого подхода к лечению этой кардиопульмональной патологии, конечным этапом которой является развитие хронической сердечной недостаточности (ХСН). Цель исследования – оценка клинического статуса, качества жизни, изменений тромбоцитарного звена гемостаза и реологических свойств крови при ХСН II–III функционального класса (ФК) у больных ИБС в сочетании с ХОБЛ II–III степени и возможности их коррекции. Материал и методы. Были обследованы 158 больных: 128 (78,8%) мужчин и 30 (21,2%) женщин. Больные 1-й группы в дополнение к базовой терапии получали эналаприл и небиволол, пациенты 2-й группы – небиволол и лозартан, пациенты 3-й группы – стандартную терапию ХСН без добавления небиволола. Результаты. У больных всех групп на фоне проводимой комплексной терапии отмечалось улучшение клинического течения заболевания, качества жизни, что выражалось в уменьшении ФК ХСН, степени одышки, увеличении толерантности к физической нагрузке и улучшении качества жизни. При этом в 1-й и 2-й группах отмечалось достоверно более выраженное уменьшение частоты (-47,1 и -46,9 против -29,9%) и общей длительности (-45,2 и -47,1 против -34,8%) эпизодов ишемии по сравнению с контрольной группой. Также к концу наблюдения во всех группах произошло достоверное снижение агрегационной активности тромбоцитов, которое было более выраженным в 1-й и 2-й группах. Заключение. У больных ХСН ишемического генеза в сочетании с ХОБЛ II–III стадий прием небиволола в сочетании с эналаприлом или лозартаном в равной степени улучшает качество жизни, повышает толерантность к физической нагрузке, уменьшает частоту и продолжительность безболевой ишемии, приводит к нормализации суточного профиля артериального давления, способствует улучшению агрегационной активности тромбоцитов, реологических свойств крови и липидного обмена.
В последние годы клинические наблюдения показали, что чаще всего врачам на практике приходится сталкиваться не с отдельными нозологиями, а с их сочетанием. Согласно эпидемиологическим исследованиям, ишемическая болезнь сердца (ИБС) и хроническая обструктивная болезнь легких (ХОБЛ) в структуре заболеваний старших возрастных групп составляют 60%, причем число больных неуклонно возрастает [1–3].
В развитии ИБС и ХОБЛ важную роль играют общие факторы риска, такие как курение, отсутствие здорового образа жизни, возраст, повышенный уровень холестерина, артериальная гипертензия, ожирение, плохая экологическая обстановка, а также системное воспаление, оксидативный стресс и коагулопатия. Хорошо изучена роль воспаления в развитии атеросклероза. Повышение уровня высокочувствительной фракции С-реактивного белка (СРБ), основного маркера воспаления, способствует повышению риска развития атеросклероза, ИБС и возрастанию бронхиального сопротивления [4, 5]. Кроме того, активация иммунных клеток в атеросклеротической бляшке коронарных сосудов способствует усилению продукции провоспалительных цитокинов (интерлейкин-1β, интерлейкин-6, интерлейкин-8, фактор некроза опухоли α, интерферон γ), повышению числа лейкоцитов, уровней фибриногена и СРБ, что также может приводить к воспалению в бронхах при ХОБЛ [6].
По мнению ряда авторов, сочетание ИБС и ХОБЛ приводит к синдрому взаимного отягощения и требует особого подхода при лечении этой кардиопульмональной патологии, чьим конечным этапом становится развитие хронической сердечной недостаточности (ХСН), при которой смертность составляет более 50% [7–9]. Кроме того, прогрессирование гипоксемии повышает активность симпатоадреналовой и ренин-ангиотензин-альдостероновой систем (РААС), способствует развитию эндотелиальной дисфункции, нарастанию легочной гипертензии, что, наряду с повышением уровня провоспалительных цитокинов, приводит к тромбообразованию и нарушению реологических свойств крови, которые, в свою очередь, влияют на неблагоприятный прогноз больных ХСН с кардиопульмональной патологией [10–13].
Лечение ХСН, ИБС и ХОБЛ по отдельности рассматривалось во многих крупных международных исследованиях (CONSENSUS, SOLVD, CIBIS- 2, 3, MERIFT-HF, SENIORS, ISSIS-4, CEISSIS-3 и др.). Современная терапия ХОБЛ основывается на рекомендациях GOLD (Global Initiativefor Chronic Obstructive Lung Disease) и предполагает использование ингаляционных бронходилататоров длительного действия, ингаляционных глюкокортикостероидов (ИГКС) и их комбинации с целью стабилизации и предупреждения декомпенсации заболевания.
При ведении больных ХСН с низкой фракцией выброса левого желудочка (ФВ ЛЖ) в соответствии с принципами доказательной медицины применяется базисная терапия ингибиторами ангиотензинпревращающего фермента (ИАПФ) или сартанами, β-адреноблокаторами, блокаторами минералокортикоидных рецепторов, а также по потребности диуретиками и сердечными гликозидами. Особых рекомендаций по ведению больных ХСН и кардиореспираторной патологией в настоящее время нет.
К сожалению, в современной литературе нет убедительных данных о влиянии β-адреноблокаторов и блокаторов РААС на состояние тромбоцитарного звена гемостаза и реологических свойств крови у больных ХСН ишемического генеза в сочетании с ХОБЛ. Поэтому изучение этого вопроса представляется актуальным.
Цель настоящего исследования – оценка клинического статуса, качества жизни, изменений тромбоцитарного звена гемостаза и реологических свойств крови при ХСН II–III функциональных классов (ФК) у больных ИБС в сочетании с ХОБЛ II–III степеней и возможности их коррекции.
Материал и методы
В исследовании были включены мужчины и женщины в возрасте 45–75 лет, имеющие ХСН II–III ФК на фоне ИБС и постинфарктного кардиосклероза, страдающие ХОБЛ среднетяжелого и тяжелого течения (в соответствии с GOLD-2013) с дыхательной недостаточностью I–II степеней. Легочный процесс был вне обострения. ФВ ЛЖ по данным эхокардиографии (ЭхоКГ) у всех больных составляла менее 45%.
Для оценки тяжести ХСН использовали классификацию Нью-Йоркской ассоциации кардиологов NYHA (New York Heart Association) и национальные рекомендации по диагностике и лечению ХСН (2013).
Диагноз ХОБЛ ставился на основании рекомендаций международной программы GOLD (2013) и отечественных стандартов по диагностике и лечению больных ХОБЛ (2013) [14, 15].
Количественную оценку выраженности дыхательной недостаточности определяли с помощью шкалы диспноэ MRC (Medical Research Council Dyspnea Scale) – модификации шкалы Флетчера.
В исследование не включались пациенты с ХСН IV ФК по NYHA, дыхательной недостаточностью III cт., острым инфарктом миокарда в течение 6 мес, предшествовавших включению...












