Фарматека №19 (332) / 2016
Клиническая эффективность локальной терапии в комплексном лечении больных остеоартрозом
(1) ФГБОУ ВО «Кировский государственный медицинский университет» Минздрава России, Киров
(2) НУЗ «Отделенческая клиническая больница» на станции Киров, ОАО РЖД, Киров
Изучена клиническая эффективность локальной терапии глюкокортикостероидами (ГКС) в комплексном лечении больных остео-
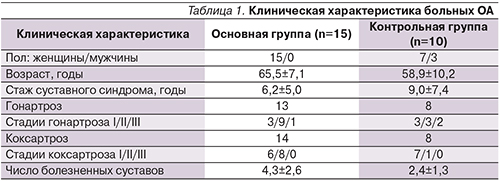
артрозом. Проведено исследование 25 пациентов, 15 из которых дополнительно получали 1–2 инъекции ГКС. В результате локальной терапии на фоне основного лечения достигнуты лучшие успехи положительной динамики клинических и функциональных показателей, а также улучшение показателей качества жизни пациентов.
Введение
Остеоартроз (ОА) – гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходом, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, а также субхондральной кости, синовиальной оболочки, связок, капсулы околосуставных мышц [1]. Вторичные воспалительные процессы, прежде всего синовит, сопровождают течение ОА, формируют клинику болезни и усиливают деструкцию суставных структур. Согласно современным представлениям, ОА является результатом взаимодействия возрастных, гормональных, генетических и средовых факторов. Патогенетические звенья ОА широко представлены в литературе [2–4].
В настоящее время в мире насчитывается более 250 млн больных ОА, при этом с возрастом частота заболевания увеличивается в геометрической прогрессии [2, 5]. Однако в реальности больных различными формами ОА гораздо больше, чем обращающихся за медицинской помощью в государственные лечебно-профилактические учреждения [6].
Социальная значимость данной болезни определяется ростом связанной с ним нетрудоспособноcти, а также снижением качества жизни (КЖ) людей [7, 8]. По снижению КЖ больных ОА далеко опережает желудочно-кишечные, респираторные и сердечно-сосудистые заболевания [9]. Вместе с ишемической болезнью сердца, алкоголизмом, депрессией и диабетом ОА входит в число факторов, наиболее часто обусловливающих продолжительное нарушение здоровья. При гонартрозе снижение КЖ отмечают до 80% пациентов, а инвалидизация составляет от 10 до 21% наблюдений [10]. ОА оказывает негативное психологическое и экономическое воздействие не только на людей, им страдающих, но и на их близких, а также на все общество в целом.
Проблема эффективного лечения ОА приобретает как медико-социальное, так и экономическое значение, т.к. заболевание в ряде случаев приводит к снижению работоспособности, а порой – и к инвалидности людей трудоспособного возраста. Утрата трудоспособности больными ОА пожилого возраста сравнима с таковой у страдающих сердечно-сосудистыми заболеваниями, и выше, чем при других заболеваниях у этого контингента пациентов [11].
Лечение ОА, в т.ч. гонартроза, до сих пор остается трудной задачей. Как правило, пациенты обращаются к врачу на поздних стадиях заболевания [10, 12, 13]. Борьба с воспалительным компонентом ОА – одно из ключевых звеньев терапии. На сегодняшний день терапия ОА до конца не разработана и, к сожалению, радикальным пособием остается эндопротезирование сустава [14].
Искусство врача состоит в создании условий, когда усиливаются целебные свойства медикамента и нивелируются его побочные действия Так как пусковым механизмом, эпицентром и конечным инвалидизирующим субстратом при ОА является сустав, локальная терапия становится патогенетически обоснованной, клинически значимой и психологически привлекательной, потому что притягивает внимание больного к конкретному мест...












