Акушерство и Гинекология №6 / 2014
Клинические значение маркеров липидного и цитокинового статуса пациенток репродуктивного возраста с наружным генитальным эндометриозом
ФГБУ Ростовский научно-исследовательский институт акушерства и педиатрии Минздрава России, Ростов-на-Дону
Цель исследования. Оптимизировать диагностику наружного генитального эндометриоза (НГЭ) у пациенток репродуктивного возраста на основании определения продукции липидов и цитокинов.
Материал и методы. Обследованы 96 пациенток, которые были разделены на 3 клинические группы: I – 28 больных с I–II стадиями НГЭ, II – 46 пациенток с III–IV стадиями заболевания. III контрольную группу составили 22 пациентки без эндометриоза. Всем пациенткам проводилась лапароскопия по общепринятой методике. Определяли содержание липопротеидов, факторов роста, СА-125, эндогенный уровень оксида азота в форме нитрит-аниона, активность нитрооксидсинтазы в сыворотке крови и перитонеальной жидкости (ПЖ).
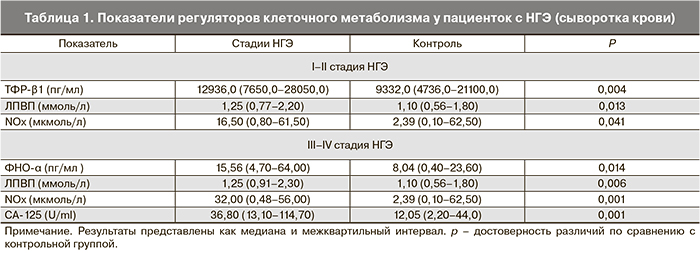
Результаты. У пациенток с различными стадиями НГЭ выявлены изменения молекулярно-клеточных взаимоотношений как на системном (сыворотка крови), так и локальном уровнях (ПЖ).
Заключение. Выявленные изменения во взаимосвязи липидного спектра, факторов роста и ангиогенных соединений являются теоретическим основанием для проведения дополнительных лечебных мероприятий, направленных на нормализацию обменных процессов при НГЭ.
В структуре гинекологической патологии эндометриоз занимает 3-е место после воспалительных заболеваний и миомы матки [1, 2]. В настоящее время серьезной проблемой является высокая частота рецидивов (до 45%) после завершения лечения [3]. Нет четкого понимания этиологии и патофизиологии заболевания, а интерпретация получаемых учеными данных носит противоречивый характер.
Отсутствие надежной неинвазивной диагностики малых форм эндометриоза [4] приводит к увеличению промежутка времени между первым проявлением симптомов боли, бесплодия и хирургическим подтверждением диагноза [5–7].
Эндометриоз – хроническое гинекологическое заболевание, главными клиническими проявлениями которого являются персистирующая боль и бесплодие, представляет собой доброкачественное разрастание вне полости матки ткани, по морфологическим и функциональным свойствам подобной эндометрию [8–10].
Особая роль в развитии наружного генитального эндометриоза (НГЭ) принадлежит процессам, происходящим в перитонеальной полости, приводящим к развитию или регрессу эндометриоидного очага [11]. Известно, что количество перитонеальной жидкости (ПЖ) у женщин с эндометриозом значительно увеличено и характеризуется высоким содержанием активированных макрофагов и продуцируемых ими цитокинов: фактор некроза опухоли-α (ФНО-α) [12], трансформирующий фактор роста-β (ТФР-β) [13], стимулирующих ангиогенез. ТФР-β, обнаруженный в высоких концентрациях в ПЖ больных НГЭ [14], обладает противовоспалительными свойствами и способен ингибировать синтез ФНО-α и других цитокинов, угнетать пролиферацию эндотелиальных клеток и способствовать развитию фиброза [15]. ФНО-α участвует в процессах, приводящих к апоптозу [16], активирует процессы липолиза и подавляет липогенез. Данные о локальной продукции факторов роста при эндометриозе неоднозначны.
ПЖ также содержит большое количество липопротеинов, особенно низкой плотности, которые генерируют окисленные липидные компоненты в составе макрофагальной воспалительной среды [17]. Параоксоназа (ПОН1) ассоциирована с липопротеинами высокой плотности (ЛПВП) и, предположительно, участвует во взаимодействии ЛПВП и липопротеинов низкой плотности (ЛПНП) [18].
Повышение уровня липидов у больных снижает функцию эндотелия и повышает степень окислительного стресса (повышается уровень продуктов окисления). Окислительный стресс обеспечивает условия для воспалительного и спаечного процесса тазовой брюшины, имеющего место при эндометриозе [19].
При этом известно, что хронические воспалительные процессы часто сопровождаются гиперхолестеринемией [15]. Однако механизмы повышения уровня ТФР-β1 при гиперхолестеринемии остаются мало исследованными.
Эти процессы при НГЭ мало изучены, в связи с чем представляется актуальным изучение изменений уровня липопротеинов и влияния их на продукцию цитокинов, а также поиск новых маркеров этого заболевания.
Цель исследования: оптимизировать диагностику НГЭ у пациенток репродуктивного возраста на основании определения продукции липидов и цитокинов.
Материал и методы исследования
Нами проведен проспективный анализ клинических проявлений заболевания и лабораторных исследований у 96 пациенток. Все пациентки были репродуктивного возраста (средний возраст 29,3±0,3 года) и проходили обследование и лечение в отделении гинекологии ФГБУ РНИИАП с 2010 по 2012 гг. В ходе проводимого исследования все больные были разделены на 3 клинические группы: I группу составили 28 больных с I–II стадиями НГЭ по классификации Американского общества фертильности (1985), II группу – 46 пациенток с III–IV стадиями заболевания. III контрольную группу составили 22 пациентки без эндометриоза, проводившие обследование по поводу бесплодия.
Для реализации поставленных задач использовались следующие методы исследования: клинические (анамнез, осмотр), лабораторные, ультразвуковое исследование, эндоскопические (лапароскопия, гистероскопия, кольпоскопия), ги...












