Акушерство и Гинекология №9 / 2018
Курение матери и нарушения метилирования ДНК у детей на ранних стадиях развития
1 ФГБУ Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова, Минздрава России, Москва;
2 VU Университет, Амстердам, Нидерланды;
3 Санкт-Петербургский государственный университет, Санкт-Петербург;
4 ФГБУ Центральный НИИ организации и информатизации здравоохранения Минздрава России, Москва;
5 АО «Международный центр репродуктивной медицины», Санкт-Петербург;
6 Институт общей генетики им. Н.И. Вавилова РАН, Москва;
7 Хьюстонский университет, Техас, США
Проанализированы результаты современных исследований роли метилирования ДНК в эмбриональном развитии человека и влияния табачного дыма при курении матери на эпигенетический статус развивающегося ребенка. Молекулярные механизмы, обеспечивающие связь между материнским курением и его эффектами на развитие и здоровье потомка, особенно отдаленными эффектами, проявляемые в течение всей его жизни, являются объектом активного изучения медицины и биологии. Исследования последних лет в области геномики человека показали, что одним из таких механизмов может являться эпигенетическая регуляция активности генов, а именно устойчивые альтерации в этой системе под влиянием табачного дыма могут обусловливать сопутствующие курению нарушения развития и здоровья. Материнское курение во время беременности оказывает двойной эффект: во-первых, негативно влияет на здоровье женщины, а во-вторых, приводит к непоправимым нарушениям развития плода, сказывается на здоровье и развитии новорожденного, качестве его последующей жизни.
По данным ВОЗ, среди людей среднего возраста курение является одним из лидирующих факторов риска заболеваемости и преждевременной смертности, причем у женщин это второй по значимости фактор риска после высокого артериального давления. Если у взрослых курение приводит к риску развития различных системных заболеваний [1], то во время внутриутробного развития эффекты материнского курения могут приводить к непоправимым нарушениям развития плода и сказываются на здоровье и развитии новорожденного, качестве его последующей жизни. Так, внутриутробное воздействие табачного дыма связывают с недостаточностью легочных функций и повышением астматических симптомов в детстве, низким весом при рождении, орофасциальными расщелинами, синдромом внезапной глухоты у новорожденных, срединным отитом, нейроповеденческими нарушениями и др. [2–7]. Установлено, что курение матери во время беременности действует как экзогенный фактор, который препятствует нормальному внутриутробному развитию плода в дозозависимой манере [8].
Традиционные исследования соотношения влияния наследственности и факторов окружающей среды на индивидуальную вариативность в показателях здоровья и заболеваемости делают акцент на корреляции между заболеванием, внешним воздействием и генотипом. Исследования последних десятилетий в области геномики человека показали, что наряду со структурной вариативностью генома существенную роль в развитии заболеваний и системных нарушений играет эпигенетическая регуляция экспрессии генов, в особенности на ранних стадиях развития [9]. Эпигенетическая регуляция реализуется посредством специальных механизмов, которые контролируют доступность промоторов генов (последовательность нуклеотидов ДНК, узнаваемых РНК-полимеразой и факторами транскрипции, как стартовая площадка для начала транскрипции) и функциональную активность других регуляторных областей генома и включают в себя метилирование ДНК, модификации гистонов, ремоделирование хроматина и редактирование РНК [10]. Исследование этих механизмов является основным объектом эпигенетики (от греч. epi – над, сверху), изучающей закономерности наследуемых изменений в экспрессии генов, которые происходят без изменения последовательности ДНК.
В данном обзоре мы более подробно рассматриваем один из основных эпигенетических механизмов – метилирование ДНК и его роль в эмбриональном развитии человека, а также обсуждаем значимость такого средового фактора, как влияние табачного дыма при курении матери на эпигенетический статус развивающегося ребенка.
Метилирование ДНК как эпигенетический механизм
Одним из основных и наиболее изученных эпигенетических механизмов является метилирование ДНК [10]. Этот механизм регуляции активности генов, участвует в ряде ключевых процессов, включая геномный импринтинг, инактивацию Х-хромосомы [11], подавление транспонируемых элементов в геноме [12] и поддержание активности генома в тканеспецифичной манере [13], обеспечивая структурное и функциональное разнообразие клеток и тканей организма. Метилирование ДНК у человека преимущественно состоит в присоединении метильной группы (CH3) к одному из азотистых оснований – цитозину. Эта модификация в большинстве случаев происходит в динуклеотидной последовательности CpG (С – цитозин и следующий за ним G – гуанин, соединенные остатком фосфорной кислоты – p). Такая последовательность имеет аналогичную в комплементарной цепи двойной спирали ДНК. Это дает возможность после репликации восстанавливать метилирование вновь синтезированной цепи ДНК по образцу одной имеющейся нити (рис. 1). Именно это и обеспечивает возможность наследования в ряду клеточных поколений паттерна ДНК-метилирования. Участки высокой плотности CpG называются CpG островками, или островками метилирования, и обнаруживаются в промоторных областях большинства (свыше 70%) генов человека.
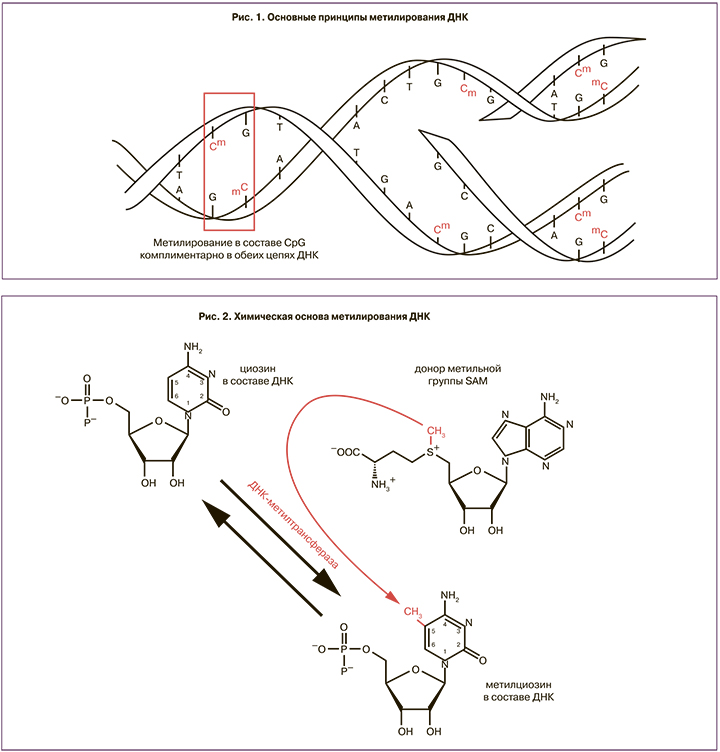
Процесс метилирования осуществляется комплексом ферментов, где одна из основных ролей принадлежит ДНК-метилтрансферазам 1 и 3 (DNMT1 и DNMT3). DNMT1 работает в основном на полуметилированной ДНК, ее функции связаны с восстановлением паттерна метилирования после репликации в соматических клетках организма, что особенно важно для тех тканей, где активные клеточные деления происходят на протяжении всей жизни. Субстратом для семейства DNMT3 служит неметилированная ДНК, и они играют важную роль при установлении тканеспецифичного паттерна метилирования de novo на самых первых этапах развития. DNMT3a и DNMT3b в ходе нормального эмбриогенеза должны начинать работу первыми и устанавливать специфичный рисунок метилирования, необходимый для обеспечения особых структурно-функциональных состояний хроматина в онтогенезе [14]. Требуемое для правильного развития соотношение между метилированными и неметилированными цитозинами поддерживается благодаря сбалансированной активности метилтрансфераз и процесса удаления с молекулы ДНК лишних метильных групп – демет...












