Трудный диагноз в педиатрии №4 / 2016
Лечение детей с заболеваниями внутриклеточной этиологии
Хламидийные и микоплазменные инфекции широко распространены среди взрослых и детей.
Интерес к этим заболеваниям возник в конце 80-х гг. прошлого столетия, когда впервые была установлена этиология хламидийной инфекции у новорожденных, матери которых были инфицированы хламидиями (Chlamydia trachomatis). Именно поэтому долгие годы создавалось мнение, что данная инфекция передается исключительно половым путем, инфицируя беременных и вызывая внутриутробное и интранатальное поражение плода и новорожденного. Вспоминая первые исследования по хламидийной инфекции, которые были начаты в 1989 году в Морозовской больнице, мы (врачи) были очень ограничены в исследовании, в выборе методов. В те годы существовало практически только два метода для диагностики хламидий — иммунофлюоресцентный (ИФ) и иммуноферментный (ИФА), но предназначены они были только для исследования материала в мазках. Основным объектом обследования были исключительно новорожденные дети. Значительно позже, благодаря многочисленным исследованиям, благодаря появлению методов ИФА, ПЦР как у нас в стране, так и за рубежом, были доказаны и описаны другие пути передачи: воздушно-капельный, контактный, гематогенный.
Открыты были и другие виды хламидий C.pneumoniae, С.psittaci. Знания о микоплазменной инфекции также обогащались — появлялось больше данных о M.pneumoniae, M.hominis.
Позже, в 90-е годы, благодаря появившейся возможности обследования детей разных возрастов, расширились представления о клинических формах хламидийной и микоплазменной инфекции. Соответственно были выделены клинические формы — с поражением верхних и нижних дыхательных путей (острый стенозирующий ларингит, бронхит, пневмония, бронхиальная астма), реактивный артрит, уретрит, вульвит, конъюнктивит, лимфаденит и др.
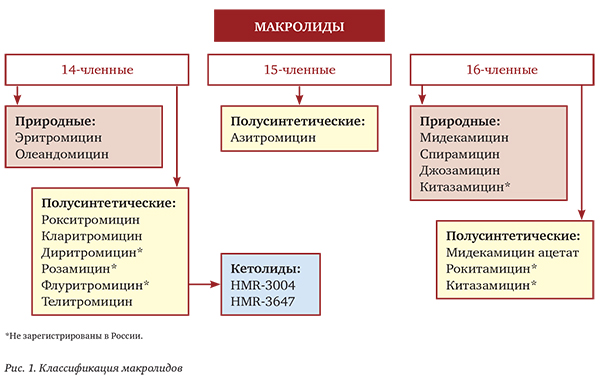
Вот уже несколько десятилетий врачи задают себе вопрос: лечить ли хламидийную и микоплазменную инфекцию? На основании многолетнего опыта наблюдения за детьми с этими инфекциями можно сказать, что в случае слишком коротких курсов антибактериального лечения, недолеченной инфекции велик риск возникновения рецидивов, осложнений, вторичной дисфункции иммунитета, внутрисемейного распространения инфекции. Важно также понимать, что основными антибиотиками в лечении внутриклеточных инфекций являются макролиды, которые нужно назначать своевременно (рис. 1).
Механизм действия макролидов связан с каталитическим пептидил-трансферазным центром 50s-cубъединицы рибосом. Это приводит к нарушению транслокации и транскрипции, подавлению синтеза белка в рибосомах микробных клеток. Макролиды действуют бактериостатически. В высокой концентрации макролиды II поколения могут оказывать бактерицидное действие [1]. В целом спектр действия всех макролидов одинаков. Они эффективны в отношении грамположительных микроорганизмов, грамотрицательных кокков, а именно стрептококка, пневмококка, менингококка, гонококка, трепонем, клостридий, листерий, коринебактерий дифтерии и эритразмы, бациллы сибирской язвы. Макролиды эффективны против пенициллинообразующего стафилококка (за исключением метициллин-резистентного), частично энтерококка, а также некоторых грамотрицательных бактерий — гемофильной палочки, моракселлы (бранхамеллы), а также бордетеллы, хеликобактер, боррелий, внутриклеточных патогенов (хламидий, микоплазм, уреаплазм), гарднерелл, коксиелл, риккетсий. Однако большинство грамотрицательных микроорганизмов природно устойчивы к макролидам. Умеренно чувствительны анаэробы: клостридии, бактероиды, актиномицеты, пропионобактерии, анаэробные кокки. Атипичные микобактерии (M.avium, M.leprae) чувствительны к азитромицину, кларитроцину, рокситромицину [1].
Мидекамицин и кларитромицин превосходят по действию среди всех макролидов в отношении грамположительных микроорганизмов. Среди всех макролидов микоплазмы M.hominis наиболее чувствительны к мидекамицину.












