Фарматека №18 (311) / 2015
Лечение злокачественных новообразований с мутацией гена BRAF V600 с использованием вемурафениба
ФГБУ РОНЦ им.Н.Н.Блохина Минздрава России, Москва
В статье представлены данные клинических исследований, оценивавших эффективность применения ингибитора BRAFвемурафениба пациентами с различными онкологическими заболеваниями. Отмечено высокое преимущество препарата перед другими противоопухолевыми средствами для пациентов с метастатической меланомой кожи. Приведены данные исследований среди различных когорт пациентов с «немеланомными» злокачественными новообразованиями, показавшими активность вемурафенибав отношении пациентов с немелкоклеточным раком легкого, а также пациентов с гистиоцитозом из клеток Лангерганса. Авторы отмечают необходимость дальнейшего изучения биологических факторов, оказывающих влияние на успешность таргетной терапии.
«Нужно научиться стрелять по микробам волшебными пулями», – говорил немецкий ученый, лауреат нобелевской премии Пауль Эрлих в начале прошлого века. Им была сформирована концепция «мишени», которая изначально предназначалась для разработки антибактериальных препаратов. Ученый поставил перед собой задачу изобрести препарат, который будет смертельным для микроорганизмов, но при этом безопасным для человека за счет его воздействия на определенную «мишень», присутствующую лишь в патогенном микроорганизме. И в 1907 г. был получен «Ehrlichschen Präparat 606» – «препарат 606», активный в отношении Treponema pallidum — возбудителя сифилиса, что, несомненно, стало прорывом в лечении этого заболевания. Препарат был назван сальварсаном, что в переводе означает «спасительный мышьяк» (лат. salv(are), спасать+arsen, мышьяк].
 П. Эрлих со своим учеником испытали новый препарат в 1909 г. Дальнейшие исследования показали, что сальварсан не идеален, были даже зафиксированы летальные исходы вследствие его применения. Позже П. Эрлих синтезировал более безопасный неосальварсан [1].
П. Эрлих со своим учеником испытали новый препарат в 1909 г. Дальнейшие исследования показали, что сальварсан не идеален, были даже зафиксированы летальные исходы вследствие его применения. Позже П. Эрлих синтезировал более безопасный неосальварсан [1].
На заре развития лекарственного лечения онкологических заболеваний предполагалось, что эффективные противоопухолевые препараты также будут угнетать рост лишь опухолевых клеток и не оказывать никакого влияния на нормальные ткани. Однако не все так просто, как хотелось бы, и появление лекарственных препаратов подобного «таргетного» действия в онкологии стало возможным лишь в конце XX в. благодаря прогрессу в области молекулярной онкологии.
В 2002 г. H. Davies и соавт. представили данные о наличии активирующей мутации в гене BRAF при различных злокачественных новообразованиях [1]. Такой вид мутации был определен при меланоме кожи, колоректальном раке, глиоме, аденокарциноме легкого, саркоме, опухолях яичника, при раке молочной железы и раке печени. Мутации не были обнаружены при исследовании нейробластомы, рака мочевого пузыря, лейкоза и лимфомы, рака шейки матки, почечно-клеточного рака, рака поджелудочной железы, рака предстательной железы, рака желудка и других видов рака [2].
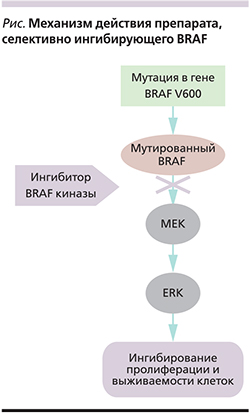
Доклинические и ранние клинические данные подтвердили, что эффект препарата, селективно ингибирующего BRAF, реализуется в опухолях, которые имеют мутацию в гене BRAF (см. рисунок). Воздействие этих молекул на опухолевые клетки с нормальным BRAF, напротив, может сопровождаться патологической активацией каскада BRAF–MEK–ERK и провоцировать рост меланомы. По этой причине перед началом терапии ингибиторами BRAF необходимо обязательно проводить тестирование образца опухоли пациента на BRAF-мутацию.
В 2011 г. вемурафениб (BRAFi – ингибитор BRAF) был зарегистрирован в США и странах Европейского Союза для лечения пациентов с метастатической меланомой кожи (мМК). В 2013 г. вемурафениб получил одоб...












