Терапия №6 / 2018
Марфаноидная внешность как предиктор нарушений сердечного ритма у лиц различных возрастных групп
ФГБОУ ВО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России
Вопросы диагностики и прогнозирования развития нарушений ритма сердца (НРС) остаются достаточно актуальной проблемой современной медицины. Повышенный интерес обусловлен, с одной стороны, связью НРС с риском внезапной смерти, а с другой – высокой частотой выявления НРС у лиц без органических заболеваний сердечно-сосудистой системы [1]. Выделение предикторов, свидетельствующих о высоком риске развития аритмий, – актуальная задача практической кардиологии. На сегодняшнее время к факторам, которые характеризуют так называемую электрическую нестабильность миокарда (ЭНМ), относят около двух десятков различных показателей, однако особое внимание уделяется тем параметрам, которые могут быть оценены без использования инвазивных методов исследования. К таким показателям относят снижение показателей вариабельности и патологические значения турбулентности (ТРС) ритма сердца, увеличение продолжительности и дисперсии интервала QT. Основным методом оценки названных параметров является холтеровское мониторирование (ХМ) электрокардиограммы (ЭКГ). В настоящее время разработаны алгоритмы оценки этих параметров, определение их включено в международные рекомендации для стратификации риска у лиц с органическими заболеваниями сердца [2].
В качестве одной из возможных причин НРС называют наследственные нарушения (дисплазии) соединительной ткани (ННСТ), которые, согласно рекомендациям Российского кардиологического общества (РКО), принято делить на классифицируемые; к ним относятся достаточно редкие генетически детерминированные заболевания [синдромы Марфана (СМ), Элерса–Данло, пролапса митрального клапана (ПМК) и др.] и неклассифицируемые (в русскоязычной литературе часто называемые дисплазиями соединительной ткани). Диагностика классифицируемых ННСТ опирается на международные согласованные критерии, которые регулярно пересматриваются [3–6].
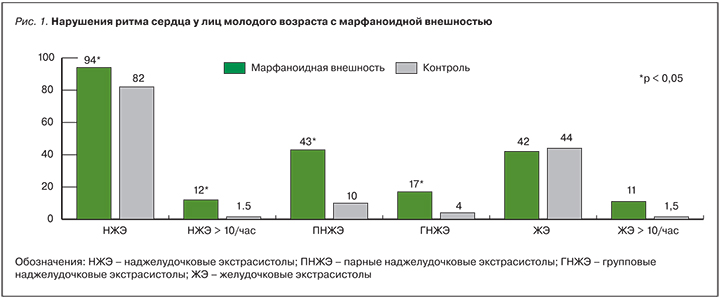
Характер НРС при классифицируемых ННСТ изучен достаточно хорошо. Так, для пациентов с СМ и ПМК характерна повышенная частота наджелудочковых (НЖЭ) и желудочковых (ЖЭ) экстрасистол, нередко у таких пациентов выявляются пробежки желудочковой тахикардии [7, 8]. Высокая частота сердечных аритмий при этих ННСТ сопровождается признаками ЭНМ – удлинением интервала QT, патологическими значениями ТРС [9, 10].
Критерии выявления неклассифицированных ННСТ до сих пор являются несогласованными. Наиболее разумным, с нашей точки зрения, является подход, изложенный в рекомендациях РКО [11, 12], авторы которых предлагают выделять диспластические фенотипы (ДФ) на основе схожести фенотипических признаков. Наиболее распространенным и изученным на сегодняшний день ДФ является марфаноидная внешность (МВ) [13]. Алгоритм диагностики МВ, изложенный в Рекомендациях [11, 12], основан на выявлении не менее четырех любых костных признаков (КП) дизэмбриогенеза. В 2017 г. нами были уточнены диагностические критерии МВ с учетом специфичности отдельных признаков [14]. К наиболее специфичным КП мы отнесли килевидную и воронкообразную деформации грудной клетки, высокое арковидное нёбо, арахнодактилию (включающую симптомы запястья и большого пальца), долихостеномелию (ДСМ), оцениваемую при выполнении хотя бы одного коэффициента: размах рук/рост >1,03 и соотношение верхнего сегмента тела к нижнему












