Терапия №4 / 2015
Молекулярные механизмы регуляции массы тела как мишени патогенетической терапии ожирения
ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова», кафедра эндокринологии, г. Москва
Распространенность ожирения и ассоциированных с ним заболеваний сопоставимы с масштабами эпидемии. Наряду с изменением образа жизни, фармакотерапия является неотъемлемым элементом программы ведения больных с ожирением. Мишенями лекарственных препаратов являются ключевые звенья центральной нервной системы, участвующие в регуляции энергообмена. В данной статье описаны основные механизмы центральной и периферической регуляции аппетита. Приведены современные принципы лекарственной терапии ожирения, дана характеристика основных препаратов.
В настоящее время в мире 2,1 млрд человек имеет избыточную массу тела, индекс массы тела (ИМТ) от 25 до 29,9 кг/м2, в том числе 671 млн – ожирение (ИМТ ≥30 кг/м2). Темпы распространения ожирения стремительно растут. За последние три десятилетия распространенность избыточной массы тела и ожирения возросла на 27,5% у взрослых, на 47,1% – у детей. В Российской Федерации избыточная масса тела отмечается у 59,2% населения, непосредственно ожирения – 24,1%; в США – 67,4 и 33,3%, в Великобритании – 63,6 и 25,8% соответственно [1]. По данным Всемирной организации здравоохранения, ожирение предопределяет развитие до 44% всех случаев сахарного диабета (СД) 2 типа, до 23% – ишемической болезни сердца, до 41% – рака различной локализации [2].
В 2013 г. Американская медицинская ассоциация (American Medical Association, AMA) сочла необходимым подтвердить статус ожирения как хронического мультифакторного заболевания (в противовес определений ожирения как «состояния», «патологии», «нарушения» либо «фактора риска»). В 2014 г. статус ожирения как самостоятельного заболевания был задекларирован в регуляторных документах, рекомендациях Американской ассоциации клинических эндокринологов (American Association of Clinical Endocrinologists, AACE) и Американской коллегии эндокринологов (American College of Endocrinology, ACE). Соответственно, за последние годы приоритет научных исследований существенно изменился: акцент сместился от изучения последствий ожирения на идентификацию причин, уточнение патогенеза, разработку эффективной профилактики и терапии ожирения как самостоятельного заболевания. Помимо изменения характера питания, снижения двигательной активности, в качестве причин широкой распространенности ожирения рассматриваются генетические и эпигенетические факторы, увеличение возраста материнства, брачная ассортативность, эндокринные дизрапторы, глобальные изменения климата, нарушения циркадианных ритмов и состава кишечного микробиома [3]. Все эти факторы в конечном итоге нарушают механизмы регуляции энергетического баланса. Лекарственные средства, назначаемые для лечения ожирения, оказывают свой эффект с вовлечением как минимум одного из звеньев энергобаланса: 1) уменьшения суточного калоража либо всасывания нутриентов; 2) повышения энергозатрат [4]. Механизм действия большинства препаратов – как зарегистрированных, так и находящихся на стадии клинических исследований – преимущественно центральный; мишенями являются ключевые структуры центральной нервной системы, участвующие в регуляции аппетита.
ОСНОВНЫЕ ПРИНЦИПЫ РЕГУЛЯЦИИ ЭНЕРГЕТИЧЕСКОГО БАЛАНСА
Масса тела определяется балансом между потреблением энергии и ее расходом. Несмотря на ежедневную вариабельность состава пищи и физических нагрузок, у взрослого здорового человека масса тела остается стабильной на протяжении многих лет. При ожирении поступление энергии превышает ее затраты [5]. В регуляции энергетического баланса задействованы центральные и периферические механизмы. Центральный контроль реализуется с участием эффекторных систем головного мозга (нейропептиды, моноамины, опиоиды, эндоканнабиноиды и др.). Периферическая регуляция обеспечивается сигналами, исходящими от гормонов, характеризующих объем жировых депо (лептин, инсулин), ряда других гормонов желудочно-кишечного тракта (глюкагоноподобный пептид-1, грелин и т.д.), нутриентов (глюкоза, свободные жирные кислоты и др.). Центральная нервная система получает информацию о состоянии энергетического статуса организма от периферических органов с помощью метаболических, эндокринных и нейрональных сигналов. На основании анализа поступившей информации формируются адекватные реакции, обеспечивающие долгосрочную (поддержание массы тела) и краткосрочную (инициация либо прекращение приема пищи) регуляцию энергообмена. За реализацию гомеостатических механизмов отвечают гипоталамус и стволовые отделы головного мозга. Эти отделы мозга тесно взаимодействуют с кортико-лимбическими структурами, осуществляющими гедонистический контроль пищевого поведения (его когнитивные, мотивационные и эмоциональные составляющие элементы) [5–7] (рис. 1).
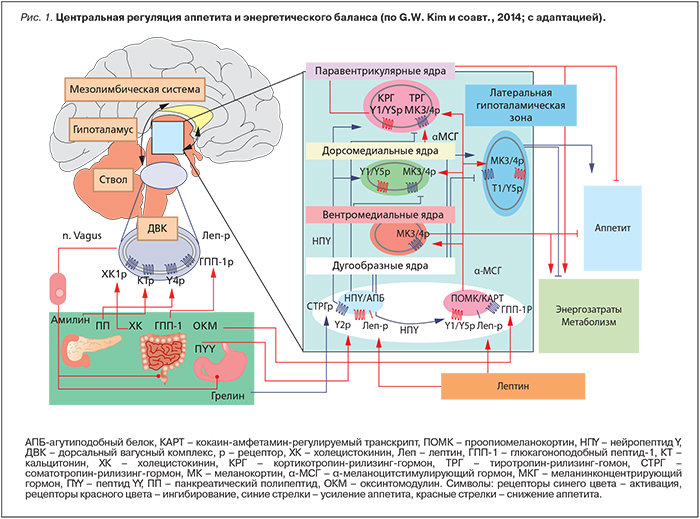
Дугообразным ядрам гипоталамуса принадлежит приоритет в интеграции сигналов, регулирующих энергетический гомеостаз. Привилегированность дугообразных ядер в гомеостатическом контроле энерг...












