Фарматека №12 (365) / 2018
Нейроэндокринные опухоли: общая характеристика и особенности тактики ведения
Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина, Москва, Россия
Нейроэндокринные опухоли (НЭО) – группа редких опухолей, которые могут развиваться в любых органах, имеют свои уникальные особенности происхождения, течения и диагностики. Развитие визуальных, иммуногистохимических методов диагностики, идентификация основных биохимических маркеров способствовали увеличению выявляемости НЭО в мире. Выбор метода лечения зависит от локализации, распространенности процесса и функционального статуса опухоли.
Введение
Нейроэндокринные опухоли (НЭО) – группа редких опухолей, которые могут развиваться в любых органах, имеют свои уникальные особенности происхождения, течения и диагностики. НЭО объединяют разнородную группу опухолей, способных вырабатывать и запасать биологически активные вещества (гормоны, пептиды, нейропередатчики), экспрессировать нейроэндокринные маркеры, что является их основной характеристикой и нередко сопровождается яркими симптомами болезни.
Представления о НЭО развивались в течение длительного времени, которое потребовалось для накопления достаточного материала и формирования определенной концепции о природе данных опухолей.
Развитие визуальных, иммуногистохимических методов диагностики, идентификация основных биохимических маркеров, эффективный анализ большой выборки эпидемиологических данных, генетические исследования свидетельствуют о неуклонном росте заболеваемости и необходимости поиска новых подходов к диагностике и лечению НЭО.
В настоящее время наиболее перспективным решением служит корпоративное, или полидисциплинарное, взаимодействие между различными научными направлениями и медицинскими специальностями.
Для решения современных проблем эпидемиологии, диагностики и лечения НЭО в 2009 г. создано междисциплинарное сообщество МОЛНЭО (Медицинское общество по лечению нейроэндокринных опухолей), основным направлением деятельности которого и являются концентрация, анализ и пропаганда знаний о НЭО различных локализаций.
Эпидемиология НЭО
В России в настоящее время начал функционировать Регистр базы данных по заболеваемости НЭО, который также демонстрирует рост заболеваемости, аналогичный международным статистическим данным. Анализ базы данных SEER (Surveillance, Epidemiology and End Results) показал, что заболеваемость НЭО в 2010 г. достигла 5,25/100 тыс. в год. Несмотря на то что частота встречаемости НЭО составляет всего 1–2 случая на 100 тыс., при аутопсии данный показатель выше и равен 8,4 на 100 тыс. населения. Частота обнаружения НЭО при аутопсии свидетельствует о том, что их распространенность существенно выше регистрируемой [2, 3].
НЭО – это чаще всего медленнорастущие новообразования, диагностируемые на поздних стадиях [1].
Бронхопульмональные НЭО составляют до 3% всех злокачественных новообразований этой локализации и порядка 25% всех НЭО. Большая часть НЭО представлена опухолями органов желудочно-кишечного тракта (ЖКТ), включая поджелудочную железу (ПЖ). Эти новообразования составляют до 2% всех злокачественных новообразований пищеварительной системы и более 60% всех НЭО. Наиболее частыми локализациями в этой группе являются подвздошная кишка (17,1%), прямая кишка (16,3%), желудок (5,4%) и аппендикс (4,7%). Встречаются также НЭО редких локализаций (производных эмбрионального нервного гребешка, нейроэктодермы и эндодермы), частота которых составляет порядка 15% всех НЭО. Потому НЭО могут выявляться в эндокринных (феохромоцитома и параганглиома, медуллярный рак щитовидной железы, опухоли паращитовидных желез и передней доли гипофиза) и других органах (вилочковая, молочная, предстательная железы, почки, яичники, кожа).
Высокодифференцированные НЭО
I. НЭО пищеварительного тракта
Согласно классификации Всемирной организации здравоохранения (ВОЗ, 2010), НЭО высокой степени дифференцировки подразделяются на высокодифференцированные (ВД) НЭО (NET) G1 и G2.
Для НЭО пищеварительного тракта митотический индекс NET G1<2, Ki-67≤2%, для NET G2 митотический индекс=2–20, Ki-67=3–20%.
Группа ВД НЭО характеризуется низким пролиферативным потенциалом, способностью секретировать разнообразные биологически активные вещества и низкой чувствительностью к химиотерапии.
К этой группе могут быть отнесены:
- карциноиды различного происхождения (эмбриогенетически развивающиеся в производных передней, средней и задней кишки);
- опухоли из хромаффинных клеток (феохромоцитома);
- медуллярная карцинома щитовидной железы.
Классификация высокодифференцированных НЭО основана на диагностических факторах, представленных в табл. 1.
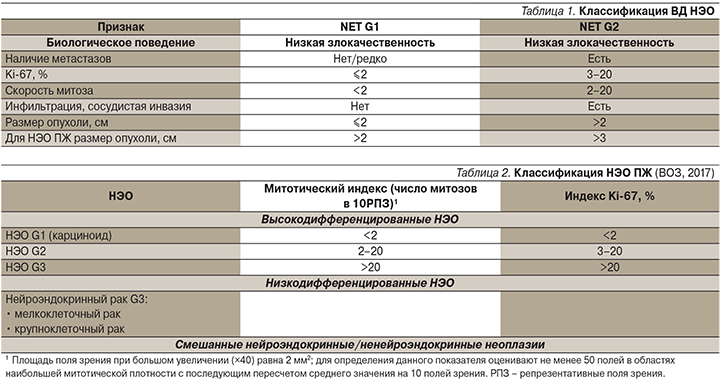
Важно: чем выше индекс Ki-67, тем хуже прогноз!
Для НЭО панкреатической локализации в 2017 г. была впервые выделена группа G3 (ВД НЭО, демонстрирующие повышенную пролиферативную активность; табл. 2). В настоящее время увеличивается количество публикаций с использованием новой классификации НЭО ЖКТ.
Отдельную группу составляют нейроэндокринные карциномы (НЭК) G3, внутри которых выделяют крупно- и мелкоклеточный рак. Степень дифференцировки наряду с индексом пролиферации и спектром генетических мутаций должна стать основным составляющим в разграничении между НЭК G3 и НЭО G3.
II. НЭО легких и тимуса ВД опухоли:
- типичный карциноид, низкий митотический индекс <2>
- атипичный карциноид, высокий митотический индекс...












