Кардиология №8 / 2016
Непосредственные результаты коронарного шунтирования у больных с мультифокальным атеросклерозом: гендерные особенности
ФГБНУ НИИ комплексных проблем сердечно-сосудистых заболеваний, Кемерово
С учетом результатов ряда исследований сложилось мнение, что по сравнению с мужчинами у женщин коронарное шунтирование (КШ) приводит к большему числу периоперационных осложнений и повышенной смертности [1—4]. Однако данная точка зрения подтверждается не всеми авторами. При анализе сопоставимой по возрасту выборки женщин и мужчин, подвергнутых операции КШ, не отмечено влияния пола пациента на периоперационную летальность [5, 6]. Кроме того, наличие мультифокального атеросклероза (МФА) является одним из факторов, неблагоприятно влияющих на прогноз у различных категорий больных с сердечно-сосудистыми заболеваниями [7, 8], в том числе при операциях реваскуляризации миокарда и на крупных сосудах [9—11]. Ввиду высокой распространенности МФА в российской популяции понятен повышенный интерес исследователей к данной проблеме [10, 12—14]. Однако следует отметить, что практически не уделяется внимания гендерным различиям по распространенности МФА у больных ишемической болезнью сердца (ИБС), а также мало изучено влияние МФА и пола на структуру сердечно-сосудистых осложнений (ССО) при операции КШ. Это послужило основанием для проведения настоящего исследования, цель которого — оценить влияние гендерных особенностей МФА на непосредственные результаты КШ у больных ИБС.
Материал и методы
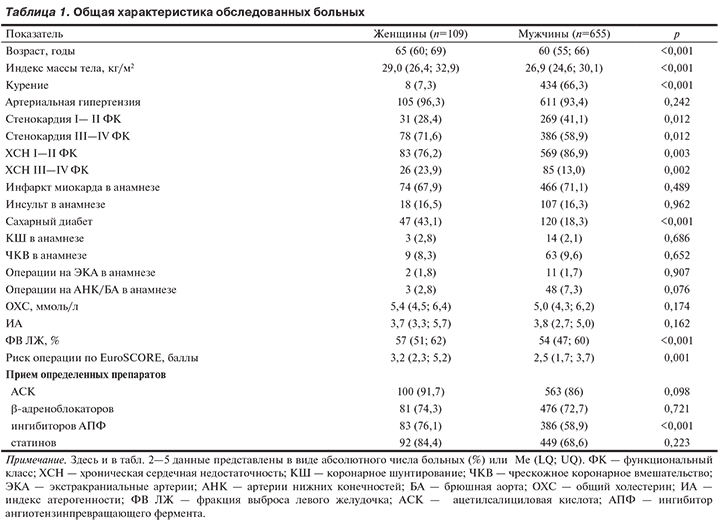
Проведен ретроспективный анализ 764 историй болезни пациентов с МФА, находившихся на обследовании и лечении в клинике сердечно-сосудистой хирургии с 1 января 2006 г. по 31 декабря 2011 г., перед выполнением плановых операций КШ. Некоторым больным были показаны этапные хирургические вмешательства на периферических артериальных бассейнах (экстракраниальных артериях, брюшной аорте, артериях нижних конечностей — АНК). У 8% пациентов ранее были выполнены сосудистые операции. Последовательность вмешательств обсуждали коллегиально с учетом риска, связанного как с реваскуляризацией миокарда, так и некардиальной операцией. В зависимости от половой принадлежности были сформированы 2 группы: 1-я группа — 109 женщин, медиана возраста 65 (60; 69) лет, 2-я группа — 655 мужчин, медиана возраста 60 (55; 66) лет.
Исследуемые группы были сопоставимы по основным антропометрическим показателям, наличию факторов риска (ФР) развития атеросклероза и атеротромботических осложнений в анамнезе, выраженности клинической симптоматики заболевания и наличию сопутствующей патологии, получаемой терапии, данным лабораторного и инструментального обследований. В группах проведена оценка распространенности МФА, а также количества реваскуляризаций миокарда и периферических артериальных бассейнов в анамнезе.
Операцию КШ выполняли на основании результатов коронарографии (КГ). Всем больным проводили эхокардиографию (ЭхоКГ) с оценкой фракции выброса левого желудочка (ФВ ЛЖ). Верификацию атеросклеротического поражения каротидного бассейна, АНК, брюшной аорты осуществляли с применением цветового дуплексного сканирования, в случае выявления стенозов более 50% выполняли ангиографическое исследование. Критерием МФА служило гемодинамически значимое поражение двух артериальных бассейнов и более. Из лабораторных показателей оценивали уровень общего холестерина и индекс атерогенности.
При анализе периоперационного этапа учитывали риск, связанный с вмешательством, по шкале EuroSCORE, длительность искусственного кровообращения (ИК) и пережатия аорты, количество операций с ИК и накладываемых шунтов. В группах оценивали частоту развития следующих периоперационных осложнений: инфаркта миокарда (ИМ), острого нарушения мозгового кровообращения, транзиторной ишемической атаки, пароксизмов фибрилляции предсердий и желудочковой тахикардии, пневмонии, обострения хронического бронхита, тромбоэмболии легочной артерии, кровотечений, пневмоторакса, гидроторакса, гидроперикарда, диастаза грудины, дисфункции желудочно-кишечного тракта, раневой инфекции, тромбоза глубоких вен, острой сердечной недостаточности (СН), дыхательной недостаточности, острой почечной недостаточности (ОПН), синдрома полиорганной недостаточности, повторного КШ, а также смерти в стационаре. Дополнительно с помощью логистического регрессионного анализа выделены предикторы развития периоперационных осложнений и летальных исходов.
Работа выполнена в соответствии с Хельсинкской деклаpацией, одобрена локальным Этическим комитетом.












