Фарматека №15 (209) / 2010
Новые препараты в лечении хронического гепатита С
1 сентября 2010
Обсуждаются перспективы лечения хронического гепатита С (ХГС) с использованием нового класса препаратов, обладающих прямым противовирусным действием. Наиболее перспективным представляется сочетание ингибиторов протеазы или полимеразы с пегилированным интерфероном альфа и рибавирином, что, как показали результаты II фазы клинических исследований, значительно увеличивает эффективность лечения больных ХГС. В статье приведены результаты исследований телапревира, R7227 и R7128 у больных ХГС.
Cочетание пегилированногоинтерферона альфа (ПЭГ-ИФН) и рибавирина (РБВ)в настоящее время представляетсобой стандарт в лечении хронического гепатита (ХГС) и обеспечивает стойкий вирусологический ответ(СВО) в среднем в 50–60 % случаев.Эффективность лечения определяется главным образом генотипом HCV (40–50 % при инфицировании генотипом 1 и 70–80 % – α генотипом 2/3), атакже исходным уровнем виремии и еединамикой в ходе лечения, возрастом,расой, генетическим полиморфизмомгена IL-28B, выраженностью фиброзапечени, приверженностью пациента лечению и некоторыми другими фак-торами. Индивидуализация лечения(оптимизация длительности терапии и доз препаратов в зависимости от вышеперечисленных факторов), повышениеприверженности пациента лечению(своевременная профилактика и коррекция нежелательных явлений, психологическая поддержка) обеспечивают повышение его эффективности, нов целом почти у 40 % пациентов с ХГСпротивовирусная терапия оказывается неэффективной.
В настоящее время изучается рядпрепаратов с различным механизмомдействия (иммуномодуляторы, терапевтические вакцины, новые молекулыинтерферонов, ингибиторы репликации вируса и блокаторы проникновения вируса в клетку). Наибольшийинтерес сегодня представляют препараты с прямым противовирусным действием, которые подавляют или блокируют ключевые внутриклеточные этапы репликации вируса, преждевсего ингибиторы протеазы и полимеразы вируса.
Механизм действия ингибиторов протеазы связан с блокадой расщепления вирусного полипротеина на структурные и неструктурные компоненты,необходимые для функционированиявируса, а ингибиторов полимеразы –с нарушением репликации вирусной РНК.
Наиболее изученным к настоящемувремени ингибитором протеазы является телапревир, который проходит III фазу клинических исследований.
Телапревир (VX-750) представляетсобой производное α-кетоамида, соединенное ковалентной обратимой связью с протеазой NS3/NS4A.
В США и Европе подведены итогидвух крупных рандомизированныхисследований (PROVE-1 и PROVE-2)эффективности телапревира в различных дозах и сочетаниях с ПЭГ-ИФН альфа-2а (Пегасис) и РБВ (Копегус) у не леченных ранее больных, инфицированных генотипом 1 HCV (рис. 1) [1, 2].
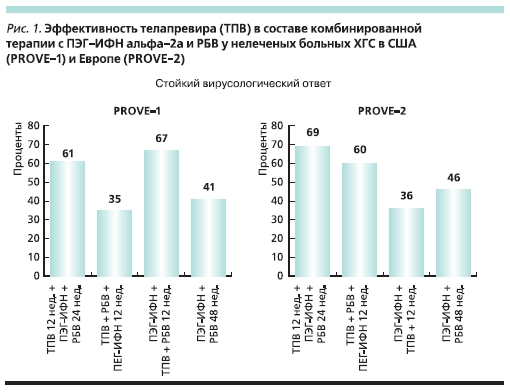
В группе больных, получавших телапревир в течение первых 12 недель в дополнение к ПЭГ-ИФН и РБВ в течени...












