Акушерство и Гинекология №10 / 2013
Новые возможности лечения гиперплазии эндометрия натуральным микронизированным прогестероном
ФГБУ Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова Минздрава России, Москва
Цель исследования. Определить эффективность различных схем циклического применения микронизированного прогестерона (МП) при простой гиперплазии эндометрия (ПГЭ) и возможные механизмы реализации его лечебного воздействия.
Материал и методы. Проведено клинико-лабораторное обследование и лечение 64 пациенток (средний возраст − 40,8±7,02 года, средний ИМТ 27,3±2,1) с ПГЭ путем применения МП в дозе 400 мг/сутки по 14- (1-я группа, n=31) и 21-дневной (2-я группа, n=33) схемам. Биопсия с морфологическим и иммуногистохимическим исследованием эндометрия проводилось до гормонотерапии и после 6 месяцев ее применения. Оценивали уровень экспрессии эстрогеновых (ER-α), прогестероновых рецепторов (PgR), регуляторов пролиферации (Ki67) и апоптоза (BIRC5). В качестве контроля исследованы образцы эндометрия фазы пролиферации (n=8) и секреции (n=7).
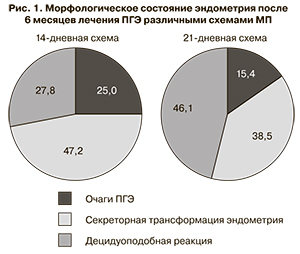
Результаты. Регрессия ПГЭ под воздействием 6 месячного курса МП в 1-й группе составила 75%, во 2-й – 84,6% (р>0,05), секреторная трансформация эндометрия – в 47,2% и 38,5% случаев, децидуоподобная реакция – в 46,1% и 27,8%. Независимо от схемы терапии лечение МП сопровождалось снижением экспрессии ER-α и PgR , уменьшением экспрессии маркера пролиферации Ki67 и ингибитора апоптоза BIRC5. Изменения указанных показателей были в 2–4 раза более выражены при децидуоподобной реакции эндометрия, чем при секреторной трансформации.
Заключение. Эффективность 14- и 21-дневной схем вагинального применения 400 мг МП в лечении ПГЭ сопоставима. Значительное снижение экспрессии рецепторов половых стероидных гормонов, понижение пролиферативной активности, активацию апоптоза, вероятно, можно рассматривать в качестве патофизиологических механизмов действия МП. Выявлена взаимосвязь со степенью выраженности ответной реакции эндометрия на гормональное воздействие (секреторная трансформация или децидуоподобная реакция).
Эндометрий – одна из наиболее сложных в структурно-функциональном отношении тканей женского организма, ее уникальность проявляется в реализации многочисленных функций, включающих защиту от инвазии инфекционных агентов, создание адекватных условий для имплантации и способность к отторжению при отсутствии наступления беременности. В обеспечении этих функций участвуют различные типы клеток (эпителиальные, стромальные, эндотелиальные), находящиеся под циклическим контролем яичниковых стероидов и паракринным влиянием биологически активных веществ [1]. Гормональный дисбаланс, проявляющийся длительным воздействием эстрогенов на фоне прогестерондефицитного состояния, продолжает рассматриваться в качестве одной из ведущих причин нарушений эпителиально-стромального взаимодействия структурных компонентов эндометрия. Это сопровождается формированием спектра морфологических изменений, лежащих в широком диапазоне – от пролиферации эндометрия при отсутствии его секреторной трансформации до возникновения различных типов гиперплазии (ГЭ) [2]. ГЭ клинически манифестируется непрогнозируемыми маточными кровотечениями, зачастую имеет рецидивирующее течение [3]. Однако многие вопросы терапии и профилактики ГЭ все еще далеки от окончательного решения, международные рекомендации тактики ведения пока не определены.
В настоящее время прогестагены рассматриваются как наиболее признанный вид гормонотерапии ГЭ [4,5]. Особенно эффективно локальное применение левоноргестрела (ЛНГ) в виде внутриматочной системы (ВМС) [6]. Этот вид терапии, очевидно, оптимален при сочетанных гиперпластических процессах эндо- и миометрия и предраковых состояниях. При ПГЭ не всегда есть необходимость в непрерывном режиме долгосрочной гормонотерапии ЛНГ. За рубежом накоплен достаточный положительный опыт перорального применения медроксипрогестерон ацетата (МПА) и мегестрол ацетата при ГЭ. Эффективность циклического приема оценивается в 60 – 70%, непрерывного – приближается к 100% [6, 7]. Надо признать, что эти препараты в Россию поступают только в высоких (онкологических) дозировках, не подходящих для лечения ГЭ. Практикующему врачу в нашей стране доступны другие прогестагены: дидрогестерон и натуральный микронизированный прогестерон (МП), который может применяться как перорально, так и вагинально. В клинической практике препарат используется с начала 1980-х годов, в основном для гормональной поддержки беременности [8]. В гинекологии, область применения его более скромная. МП в основном применяется при функциональной недостаточности желтого тела и для защиты эндометрия при проведении заместительной гормонотерапии. Научные публикации об эффективности МП при ГЭ в доступной литературе не встретились. В настоящее время есть возможность оценить эффект препарата не только морфологически, но и иммуногистохимически (ИГХ), определяя экспрессию рецепторов половых стероидов, маркеры пролиферации и апоптоза. Этому существенному вопросу посвящено настоящее сообщение.
Цель исследования – определить эффективность различных схем циклического применения МП при простой ГЭ (ПГЭ) и возможные механизмы реализации его лечебного воздействия.
Материал и методы исследования
В основу работы положены результаты комплексного клинико-лабораторного обследования и лечения 64 женщин в возрасте от 18 до 50 лет, (средний возраст − 40,8±7,02 года, средний ИМТ 27,3±2,1) с ПГЭ. Исследование одобрено этическим комитетом ФГБУ Научный центр акушерства, гинекологии и перинаталогии им. академика В.И. Кулакова Минздрава России.
Показаниями к проведению гистероскопии и кюретажа эндометрия являлись маточные кровотечения различного характера, редко случаи подозрения на патологию эндометрия по данным УЗИ. Более половины пациенток − 38 (59,4%) находились в репродуктивном возрасте, остальные 26 (40,6%) − в пременопаузе. У 56,2% пациенток, несмотря на проведение традиционной гормонотерапии (КОК, прогестагенами, аГнРГ), ГЭ имела рецидивирующий характер. Среднее число ранее произведенных диагностических выскабливаний составило 3,2.
 Для лечения ПГЭ был применен МП в суточной дозе 400 мг перорально или вагинально, по 14- и 21-дневной схемах. В соответствие с этим были выделены 2 группы: 1-я – 31 человека, 2-я – 33. Лечение МП сопровождалось появлением нежелательных эффектов. В течение первого месяца перорального приема МП 58 (90,6%) пациенток предъявили жалобы на головокружение и сонливость, снижающее работоспособность, в связи с этим им было рекомендовано локальное применение препарата. Терапию продолжили 58 пациенток (26 из 1-й группы и 32 – из 2-й), 2 выбыли из исследования из-за дискомфорта во влагалище при местном применении препарата, 4 – по причинам, не связанным с приемом МП. Применение 14- дневной схемы не сопровождалось нарушениями менструального цикла, 21-дневной схема вызвала межменструальные кровяные выделения из половых путей ...
Для лечения ПГЭ был применен МП в суточной дозе 400 мг перорально или вагинально, по 14- и 21-дневной схемах. В соответствие с этим были выделены 2 группы: 1-я – 31 человека, 2-я – 33. Лечение МП сопровождалось появлением нежелательных эффектов. В течение первого месяца перорального приема МП 58 (90,6%) пациенток предъявили жалобы на головокружение и сонливость, снижающее работоспособность, в связи с этим им было рекомендовано локальное применение препарата. Терапию продолжили 58 пациенток (26 из 1-й группы и 32 – из 2-й), 2 выбыли из исследования из-за дискомфорта во влагалище при местном применении препарата, 4 – по причинам, не связанным с приемом МП. Применение 14- дневной схемы не сопровождалось нарушениями менструального цикла, 21-дневной схема вызвала межменструальные кровяные выделения из половых путей ...












