Фарматека №14 (327) / 2016
Новый метод прогнозирования необходимости внутривенной регидратации у детей с ротавирусным гастроэнтеритом в условиях стационара
ФГАУ «Научный центр здоровья детей» Минздрава РФ, Москва
Острые гастроэнтериты (ОГЭ) являются одной из частых причин госпитализации в мире среди детей в возрасте до 5 лет. Первой линией в терапии ОГЭ является пероральная регидратация, что обусловлено основными симптомами заболевания: рвотой и диареей, которые приводят к обезвоживанию. В соответствии с рекомендациями ВОЗ, детям с легкой и умеренной степенями дегидратации показана исключительно пероральная регидратация, в то время как тяжелая степень дегидратации является абсолютным показанием к парентеральной регидратации. Однако части детей с умеренным обезвоживанием может потребоваться парентеральная регидратация из-за неукротимой рвоты, отказа от питья и/или продолжающейся диареи, что не всегда возможно прогнозировать на момент поступления ребенка в стационар и оценить по имеющимся шкалам. Представлены результаты исследования, проведенного с целью разработать предиктивную шкалу для оценки необходимости парентеральной регидратации при ОГЭ. Основой для данного инструмента явилась ранее созданная шкала Vesikari для ретроспективной оценки тяжести ОГЭ. Разработанная шкала оценки необходимости в парентеральной регидратации в остром периоде дала удовлетворительные результаты в выборе метода регидратации, особенно в группе детей с умеренным обезвоживанием. Использование данной шкалы будет способствовать уменьшению длительности госпитализации за счет своевременно назначенной парентеральной регидратации.
Обоснование
Острые гастроэнтериты (ОГЭ) – одна из частых причин госпитализаций детей в возрасте до 5 лет [1].
В большинстве случаев причиной ОГЭ у детей являются вирусы, в частности ротавирусная инфекция (РВИ) [2, 3]. В странах, где не внедрена обязательная вакцинопрофилактика против РВИ, частота госпитализаций по причине РВИ может достигать 40% от всех гастроэнтеритов (по данным 1986−2000 гг.) [4]. Нозокомиальная РВИ обусловливает 50–70% госпитальных гастроэнтеритов и увеличивает пребывание в стационаре от 4 до 12 суток [1]. РВИ может стать причиной тяжелого обезвоживания вплоть до летального исхода. Так, по данным Всемирной организации здравоохранения (ВОЗ, 2008), у детей в возрасте до 5 лет РВИ обусловила 453 тыс. случаев смерти в странах с низкими доходами населения [5].
В подавляющем большинстве случаев лечение ОГЭ не требует назначения антибактериальной терапии, и первой линией в терапии гастроэнтерита как вирусной, так и бактериальной этиологии является регидратация. По рекомендации ВОЗ, детям с легким и умеренным обезвоживанием показана исключительно пероральная регидратация, в то время как наличие признаков тяжелой дегидратации служит абсолютным показанием к проведению парентеральной регидратации [6]. Однако части детей с умеренным обезвоживанием не удается проведение адекватной пероральной регидратации из-за серийной рвоты, отказа от питья, продолжающейся диареи. Эффективность пероральной регидратации невозможно прогнозировать на момент поступления в стационар по имеющимся шкалам, что обусловливает создание предиктивной шкалы для оценки необходимости проведения парентеральной регидратации при ОГЭ.
За основу разрабатываемого инструмента была взята шкала клинической оценки тяжести ротавирусного гастроэнтерита T. Vesikari, созданная исключительно для ретроспективной оценки тяжести эпизода РВИ в группах вакцинированных и невакцинированных детей и не предназначенная для помощи в выборе лечения [7].
Цель исследования: разработать предиктивную шкалу для оценки необходимости проведения парентеральной регидратации при ОГЭ у детей.
Материал и методы
На базе отделения диагностики и восстановительного лечения Научного центра здоровья детей (Москва) в период с 2013 по 2015 г. проведено пилотное ретроспективное нерандомизированное исследование с проспективной группой. В ретроспективную группу были включены 100 детей (из них 44% девочек, 66% мальчиков) в возрасте от 4 месяцев до 5 лет с острым ротавирусным гастроэнтеритом без сопутствующей патологии. Проспективную группу составили 20 детей (из них 30% девочки, 70% мальчики) с ОГЭ ротавирусной этиологии. На основании клинико-анамнестических данных проведен пошаговый статистический анализ возможности прогнозирования необходимости парентеральной регидратации на ретроспективной группе. Далее разработанная шкала проверена на проспективной группе из 20 детей.
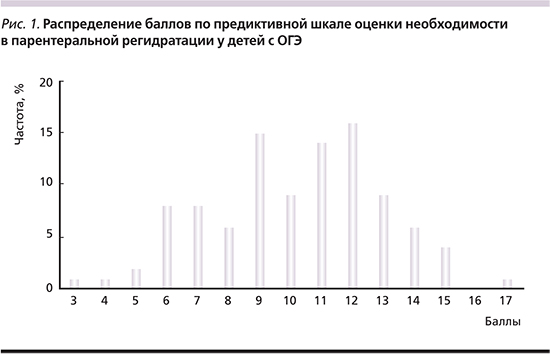
Лечение детей осуществляли в соответствии со стандартами, рекомендованными ESPGHAN (European Society of PediatricGastroenterology, Hepatology and Nutrition) [1] и ВОЗ [6]. Пероральная регидратация осуществляется гипоосмолярным солевым раствором (245 мОсм/л). В зависимости от степени дегидратации и возможности проведения пероральной регидратации дети получали парентеральную регидра...












