Фарматека №6 (339) / 2017
Новый подход к купированию болевого синдрома при синдроме раздраженного кишечника
Кафедра пропедевтики внутренних болезней и гастроэнтерологии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России, Москва
Представлены результаты неинтервенционного сравнительного клинического исследования в параллельных группах для оценки эффективности и безопасности применения препарата, содержащего комплекс антител к фактору некроза опухоли α, мозгоспецифическому белку S-100, гистамину (кАТ), в терапии синдрома раздраженного кишечника (СРК) по сравнению с тримебутином. Полученные данные позволяют рекомендовать кАТ к широкому применению в терапии СРК, что положительно отразится на купировании клинических проявлений заболевания, в первую очередь болевого синдрома.
Функциональная патология органов пищеварения представляет большой интерес для медицинского сообщества. Одним из самых изученных заболеваний такого рода является синдром раздраженного кишечника (СРК) [11–14], при котором, согласно Римским критериям IV пересмотра (2016), наблюдается рецидивирующая абдоминальная боль как минимум 1 день в неделю на протяжении последних 3 месяцев, ассоциированная с 2 или более из числа следующих признаков: связана с дефекацией, ассоциирована с изменением частоты, а также формы стула. Данные симптомы должны наблюдаться не менее 6 месяцев назад [1].
Отличием определения СРК от Римских критериев-III является замена слов «уменьшается после дефекации» на «связано с дефекацией», т.к. далеко не все пациенты отмечают уменьшение боли после дефекации, многие отмечают ее усиление. Также из определения исключен термин «дискомфорт», поскольку не все языки мира содержат данное слово, что создает трудности в интерпретации своего состояния пациентом и жалоб пациента врачом, а это в свою очередь может приводить врача на ошибочный диагностический путь. В Римских критериях-IV уточнены временные рамки, в течение которых должны наблюдаться симптомы: теперь это не реже 1 раза в неделю вместо 3 дней в месяц, как было в критериях III. Таким образом, сегодня отличительной чертой СРК является именно боль в животе, а не «околоболевые» ощущения [2].

Следует подчеркнуть, что все функциональные заболевания желудочно-кишечного тракта (ЖКТ), и в частности СРК, существенно снижают качество жизни пациентов. Боль является, пожалуй, главным фактором в течении заболевания, остро переживаемая пациентом и тем самым оказывающая мощное влияние на его оценку своего состояния и качество жизни. В связи с этим купирование болевого синдрома является важнейшей и неотъемлемой частью качественного лечения больных СРК. Кроме абдоминальной боли в патогенезе СРК принимают участие расстройства моторной функции кишечника, висцеральная гиперчувствительность, нарушения состава кишечной микробиоты. Коррекция указанных нарушений, несомненно, вносит существенный вклад в успех лечения.
Однако, несмотря на непрекращающиеся научные изыскания на тему СРК, вопросы лечения данного расстройства остаются сложными и дискутабельными. Дело в том, что до сегодняшнего дня не было универсального средства, которое воздействовало бы на все звенья патогенеза СРК. Врач вынужден был назначать как минимум 2 препарата – спазмолитик и средство, влияющее на нарушения стула: слабительное или закрепляющее. Необходимость приема нескольких препаратов снижает приверженность пациентов лечению и как следствие – ведет к низкой эффективности последнего.
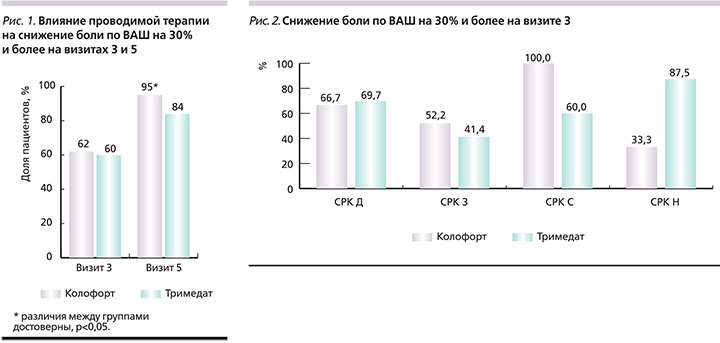
На отечественный фармакологический рынок не так давно вышел новый препарат российского производства, содержащий комплекс антител к трем компонентам – релиз-активные антитела к мозгоспецифическому белку S-100, фактору некроза опухоли α и гистамину (кАТ). Сочетание трех активных компонентов разрывает «порочные круги» патогенеза СРК и позволяет купировать клиническую симптоматику, в частности боль и нарушения стула, нормализует висцеральную гиперчувствительность и повышает качество жизни. Кроме того, за счет наличия релиз-активных антител к мозгоспецифическому белку S-100, обладающих анксиолитическим действием, кАТ нормализует эмоциональный фон пациентов, который часто бывает снижен.

Результаты проведенных ранее доклинических и клинических испытаний свидетельствуют в пользу эффективности и безопасности кАТ и его компонентов в лечении гастроинтестинальной патологии воспалительного и функционального характера, а также купирования при его применении соматоформных нарушений и психоневрологических расстройств на фоне соматических и неврологических заболеваний [3–6].
Эффективность кАТ была подтверждена в ходе двойного слепого плацебо-контролируемого рандомизированного исследования [7].
Также заслуживает внимания тримебутин – агонист опиатных рецепторов. Применение тримебутина на протяжении нескольких десятков лет для лечения различных функциональных расстройств ЖКТ подтверждает его эффективность и безопасность.
Тримебутин связывается с мю-, каппа- и дельта-опиатными рецепторами, при этом не обладая специфичностью к какому-то одному их виду. Являясь нормокинетиком, препарат оказывает двойной ре...












