Фарматека №5 / 2019
Обострение хронической обструктивной болезни легких: роль и место антибиотиков
Российская медицинская академия непрерывного профессионального образования, Москва, Россия
Хроническая обструктивная болезнь легких (ХОБЛ) – широко распространенное хроническое заболевание, течение которого характеризуется периодически возникающими обострениями, являющимися основной причиной обращения больных за медицинской помощью, госпитализаций, летальных исходов. Ключевое место в развитии обострений ХОБЛ занимают бактериальные возбудители, что определяет целесообразность использования в данной клинической ситуации антимикробных препаратов. Современные подходы к антибактериальной терапии обострений ХОБЛ рассматриваются в представленной статье.
Для цитирования: Романовских А.Г., Синопальников А.И., Белоцерковская Ю.Г., Смирнов И.П. Обострение хронической обструктивной болезни легких: роль и место антибиотиков. Фарматека. 2019;26(5):61–69. DOI: https://dx.doi.org/10.18565/pharmateca.2019.5.61-69
Введение
Хроническая обструктивная болезнь легких (ХОБЛ) остается одной из важнейших проблем современного здравоохранения. Согласно прогнозам экспертов, к 2030 г. заболевание займет третье место среди причин смертности в мире [1]. ХОБЛ представляет собой гетерогенное заболевание, к характерным чертам которого относятся стойкие респираторные симптомы и бронхиальная обструкция, возникающие в результате патологии дыхательных путей и/или альвеол. Наиболее частой причиной данных изменений служит значимое воздействие повреждающих частиц и газов [2]. Течение заболевания характеризуется периодически возникающими обострениями, приводящими к более быстрому прогрессированию заболевания и являющимися ведущей причиной обращения больных ХОБЛ за медицинской помощью, госпитализаций и летальных исходов [3, 4]. Только в США затраты, связанные с заболеванием, превышают 50 млрд долл. в год, большинство из которых приходится на лечение обострений [5]. Как свидетельствуют результаты проведенных исследований, отмечается слабая корреляция между нарушениями вентиляционной функции легких и частотой обострений ХОБЛ, лучшим предиктором развития будущих обострений является их частота в прошлом [6]. Согласно современным представлениям, бóльшая часть обострений ХОБЛ имеет инфекционную природу, вместе с тем показания к назначению антимикробных препаратов (АМП) и их выбор в данной клинической ситуации зачастую служат предметом дискуссий. Обсуждению этих вопросов и посвящена представленная статья.
Этиология и патогенез
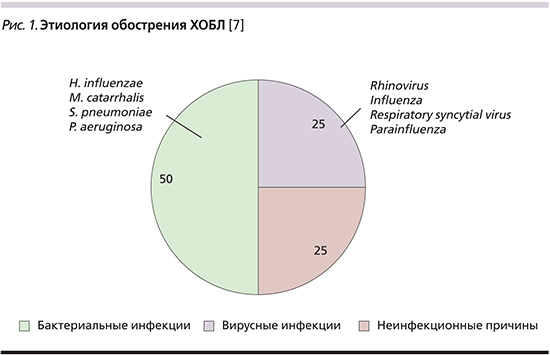
Результаты проведенных исследований свидетельствуют, что до 70−80% случаев обострений ХОБЛ обусловлены бактериальной и вирусной инфекцией респираторного тракта (рис. 1). Основные неинфекционные причины обострения: воздействие аэрополлютантов окружающей среды, низкая приверженность пациентов лечению, декомпенсация сердечной деятельности, ошибочное назначение лекарственных препаратов и др. Ключевое место в развитии инфекционных обострений ХОБЛ занимают бактериальные возбудители, среди которых ведущая роль принадлежит нетипируемой Haemophilus influenzae, Streptococcus pneumoniae, Moraxella catarrhalis, при тяжелой ХОБЛ – Pseudomonas aeruginosa [8].
Структура возбудителей в значительной степени коррелирует с имеющимися у пациента нарушениями вентиляционной функции легких. При выраженной бронхиальной обструкции из образцов мокроты пациентов чаще выделяются пенициллинорезистентные S. pneumoniae (ПРП), β-лактамазопродуцирующие штаммы H. influenzae. Наличие бронхоэктазов ассоциируется с колонизацией бронхиального дерева P. aeruginosa, особенно в сочетании с крайне тяжелыми нарушениями бронхиальной проходимости. Этиологическое значение представителей семейства Enterobacteriaceae и Staphylococcus aureus, несмотря на частое выделение данных возбудителей при бактериологическом исследовании образцов мокроты пациентов с обострением ХОБЛ, остается неясным. Роль «атипичных» бактерий (Chlamydophila pneumoniae и Mycoplasma pneumoniae) в развитии обострений заболеваний представляется достаточно скромной: согласно результатам проведенных исследований, данные микроорганизмы ответственны менее чем за 5% обострений [8].
Следует отметить, что взгляды на роль бактериальной инфекции в патогенезе обострений ХОБЛ неоднократно менялись: от признания ведущей роли инфекционных агентов в возникновении обострений заболевания до отрицания причинно-следственной связи между выявлением бактерий в секрете дыхательных путей и усилением выраженности симптомов. Известно, что структурные изменения бронхов, а также нарушение местного противоинфекционного иммунитета при ХОБЛ создают условия для колонизации бактериальных агентов на поверхности эпителия дыхательных путей (в нормальных условиях дыхательные пути дистальнее гортани стерильные), результатом чего является прогрессирование эндобронхиального воспаления. В предшествующие годы преходящее усугубление клинических проявлений заболевания преимущественно объяснялось периодически возрастающей «микробной нагрузкой» на дыхательные пути. Вместе с тем получены и доказательства того, что возникновение обострений ХОБЛ ассоциируется с «приобретением» пациентом новых штаммов бактерий, к которым организм еще не приобрел действенного противоинфекционного иммунитета. Развитие иммунологических реакций в этом случае и является фактором, приводящим к появлению клинической картины обострения заболевания [9]. Необходимо отметить, что при микробиологическом исследовании образцов мокроты невозможно разграничить «колонизирующие» микроорганизмы и микроорганизмы, ответственные за развитие обострений, что ограничивает диагностическую ценность данного метода диагностики и определяет нецелесообразность его рутинного использования при обострении ХОБЛ. Исследование рекомендуется при наличии у пациента факторов риска инфекции, вызванной P. aeruginosa, неэффективности антибактериальной терапии (АБТ) в случае существующей уверенности в инфекционной этиологии обострений, при наличии или угрозе возникновения острой дыхательной недостат...












