Фарматека №1 / 2021
Оценка способности бензидамина гидрохлорида подавлять планктонные клетки, а также растущие и зрелые биопленки клинически значимых микроорганизмов
1) Государственный научный центр прикладной микробиологии и биотехнологии, Оболенск, г.о. Серпухов, Московская область, Россия;
2) Анджелини Фарма Рус, Москва, Россия;
3) Международная ассоциация клинических фармакологов и фармацевтов, Москва, Россия;
4) Первый Московский государственный медицинский университет им. И.М. Сеченова, Москва, Россия
Обоснование. Биопленки представляют собой серьезную во всем мире проблему для здоровья из-за того, что они открывают дополнительные возможности для бактерий и грибов сопротивляться антимикробным препаратам. На сегодняшний день в России зарегистрировано большое количество антимикробных препаратов, однако данные об изучении их антагонистической активности в отношении биопленок ограничены. Особый интерес из-за широкого клинического применения представляет местный противовоспалительный препарат с антимикробными свойствами – бензидамин.
Цель исследования: сформировать коллекцию клинически значимых микроорганизмов (грамположительных бактерий, грамотрицательных бактерий и дрожжеподобных грибов), изучить чувствительность их планктонных и биопленочных культур к антимикробному препарату бензидамина гидрохлорид.
Методы. Определение минимальных подавляющих концентраций бензидамина гидрохлорида против тест-культур микроорганизмов методом серийных разведений в жидких и плотных питательных средах.
Результаты. Создана коллекция тест-штаммов, клинически значимых микроорганизмов, возбудителей инфекционных заболеваний ротовой полости: грамотрицательных бактерий, грамположительных бактерий и дрожжеподобных грибов. Получены новые данные о чувствительности клинически значимых микроорганизмов к бензидамину гидрохлориду.
Выводы. Показано, что планктонные культуры и формирующие биопленки тест-штаммы Pseudomonas aeruginosa, Moraxella catarrhalis, Haemophilus influenzae, Gardnerella vaginalis, Staphylococcus spp., Streptococcus pneumoniae, Candida spp. чувствительны к бензидамину гидрохлориду в концентрации, соответствующей таковой в препарате Тантум® Верде 0,15 и 0,3%. Отмечена также ингибирующая активность бензидамина гидрохлорида против зрелых биопленок клинически значимых микроорганизмов в диапазоне концентраций 160–1280 мг/л.
Введение
Бактерии образуют биопленки как способ оградить себя от агрессивных факторов внешней среды и выжить. Поэтому биопленки в природе встречаются очень часто. Еще в 1683 г. А. ван Левенгук наблюдал и описывал биопленки, выделенные с поверхности зубов с помощью своего примитивного микроскопа. Однако тема биопленок не особо интересовала исследователей и практикующих врачей до начала 1970-х гг., когда Н. Хойби обнаружил связь между развитием очагов хронического воспаления и большим титром бактерий у пациентов с муковисцидозом [1]. С тех пор признано, что биопленки могут быть причиной большого числа клинических осложнений распространенных заболеваний [2, 3] и вносят отдельный вклад в течение хронических инфекций [4].
Бактериальные биопленки – это скопление бактерий, прикрепленных к поверхности ткани и/или друг к другу. Вокруг этих бактерий образуется матрикс. Матрикс биопленки состоит из таких веществ, как белки (например, фибрин), полисахариды (например, альгинат) и пр. Оставаясь бездействующими и скрытыми от иммунной системы под матриксом, они могут вызывать локальное повреждение тканей, а затем острую инфекцию. Внутри биопленки бактерии адаптируются к аноксии окружающей среды и ограничению питательных веществ, демонстрируя измененный метаболизм, экспрессию генов и выработку белка, что может приводить к более низкой скорости метаболизма и уменьшению скорости деления клеток [3, 5]. Кроме того, эта адаптация делает бактерии более устойчивыми к противомикробной терапии за счет инактивации противомикробных агентов. При формировании очагов бактерий с биопленками ни врожденный, ни приобретенный иммунный ответы не могут достаточно уничтожать бактерии в биопленках, вместо этого ускоряют повреждение коллатеральных тканей [6]. Следовательно, заболевания, связанные с биопленками, обычно представляют собой стойкие инфекции, которые развиваются медленно, редко разрешаются с помощью собственной иммунной системы и сопровождаются непрогнозируемой реакцией на антимикробную фармакотерапию.
Помимо бактерий грибы рода Candida также могут формировать биопленки, например C. albicans, C. glabrata, C. tropicalis и C. parapsilosis.
C. albicans являются наиболее распространенными грибковыми патогенами человека, вызывающими как инфекции на слизистых оболочках, так и системные инфекции. Это объясняется тем, что C. albicans обладает высокой способностью к адаптации, что позволяет этим микроорганизмам изменять статус комменсального микробного агента на статус агрессивного патогена благодаря имеющемуся у них набора факторов вирулентности. В частности, способность изменять морфологию и образовывать биопленки является центральным звеном в патогенезе C. albicans [7].
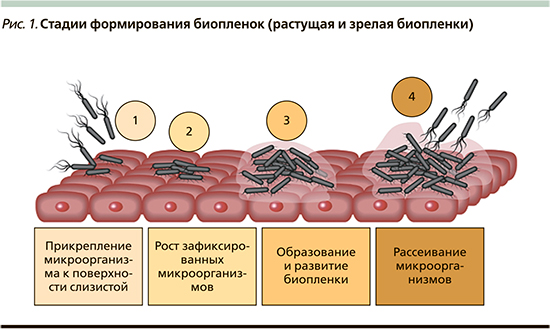
Стоит также отметить, что на сегодняшний день известно о двух типах биопленок – формирующиеся био и зрелые биопленки. Тип биопленки определяется стадией ее формирования. Обычно считается, что формирование биопленки происходит в течение четырех основных стадий: 1) прикрепление бактерий к поверхности, 2) образование микроколоний, 3) созревание биопленки и 4) рассредоточение бактерий, которые затем могут колонизировать новые области [8]. Этот процесс образования биопленок изображен на рис. 1.
Бензидамина гидрохлорид – препарат, относящийся к классу нестероидных противовоспалительных сре...












